Тест в 10 классе «Химический состав клетки»
Тест по биологии по теме «Химический состав клетки» 1 вариант
1) Многоотраслевая наука о живой природе называется
А) физиология В) биология С) экология Д) цитология Е) эмбриология
2) Укажите, какова функция углеводов в организме:
А) ферментативная В) энергетическая С) двигательная Д) защитная Е) источник воды
3) Сигнальную функцию выполняют:
А) липиды В) углеводы С) жиры Д) белки Е) полисахариды
4) В состав РНК входит углевод:
А) дезоксирибоза В) аденин С) глюкоза Д) фруктоза Е) рибоза
5) Белки – это биологические полимеры, мономерами которых являются:
А) нуклеиновые кислоты В) ферменты С) аминокислоты Д) углеводы Е) глюкоза
6) К моносахаридам относится:
А) крахмал В) сахароза С) фруктоза Д) целлюлоза Е) мальтоза
7) При окислении 1 грамма углеводов выделяется энергии:
А) 35,2 кДж В) 38,9 кДж С) 16,7 кДж Д) 27,6 кДж Е) 17,6 кДж
А) аминокислот В) АТФ С) сахарозы Д) ДНК Е) РНК
9) В состав гемоглобина входит:
А) магний В) иод С) железо Д) фосфор Е) кальций
10) Входит в состав плазмы крови:
А) фтор В) бром С) бор Д) натрий Е) медь
11) Процесс удвоения ДНК:
А) транскрипция В) трансляция С) репликация Д) конъюгация Е) редукция
12) Макроэлементов в клетке:
А) 37% В) 98% С) 1,1% Д) 0,02% Е) 76%
13) Растворимость веществ в клетке:
А) транскрипция В) трансляция С) гидрофильность Д) редупликация Е) гидрофобность
14) К дисахаридам относится:
А) гликоген В) сахароза С) глюкоза Д) целлюлоза Е) фруктоза
15) Наука о строении и жизнедеятельности клетки называется:
А) гигиена В) физиология С) цитология Д) анатомия Е) гистология
16) Каталитическую функцию в организме выполняют:
А) белки В) жиры С) углеводы Д) липиды Е) нуклеотиды
17) Основной источник энергии в организме:
А) РНК В) углеводы С) жиры Д) белки Е) ферменты
18) В состав ДНК входит углевод:
А) рибоза В) аденин С) глюкоза Д) фруктоза Е) дезоксирибоза
19) Углеводы – это биологические полимеры, мономерами которых являются:
А) нуклеиновые кислоты В) ферменты С) аминокислоты Д) липиды Е) моносахариды
20) К полисахаридам относится:
А) крахмал В) сахароза С) фруктоза Д) глюкоза Е) мальтоза
21) При окислении 1 грамма жиров выделяется энергии:
А) 35,2 кДж В) 38,9 кДж С) 16,7 кДж Д) 17,6 кДж Е) 27,6 кДж
22) Азотистое основание урацил входит в состав:
А) аминокислот В) АТФ С) сахарозы Д) ДНК Е) РНК
23) В состав хлорофилла входит:
А) магний В) иод С) железо Д) фосфор Е) кальций
24) Входит в состав плазмы крови:
А) фтор В) бром С) бор Д) хлор Е) медь
25) Процесс переписывания информации с ДНК на РНК:
А) транскрипция В) трансляция С) репликация Д) комплементарность Е) редукция
2. Установите соответствие между особенностями и молекулами, для которых эти особенности характерны.
Установите соответствие между особенностями и молекулами, для которых эти особенности характерны.
ОСОБЕННОСТИ МОЛЕКУЛЫ
А) полимер, состоящий из аминокислот 1) ДНК
Б) в состав входит пентоза – рибоза 2) РНК
В) мономеры соединены ковалентными пептид – 3) белок
ными связями
Г) полимер, состоящий из нуклеотидов, которые содержат
азотистые основания – аденин, тимин, гуанин, цитозин
Д) полимер, состоящий из нуклеотидов, которые содержат
азотистые основания – аденин, урацил, гуанин, цитозин
Е) характеризуется первичной, вторичной, третичной структурами
3. Установите последовательность процессов, происходящих при катаболизме.
А) гликолиз
Б) расщепление сложных органических соединений
В) образование 36 – ти молекул АТФ
Г) образование только тепловой энергии
Д) гидролиз
Е) образование 2 – х молекул АТФ
Часть 3.
1. Найдите ошибки в приведенном ниже тексте, исправьте их, укажите номера предложений, в которых они допущены, запишите эти предложения без ошибок.
1. Молекула ДНК состоит из двух спирально закрученных цепей. 2. При этом аденин образует три водородные связи с тимином, а гуанин – две водородные связи с цитозином. 3. Молекулы ДНК прокариот линейные, а эукариот – кольцевые. 4. Функции ДНК: хранение и передача наследственной информации. 5. Молекула ДНК, в отличие от молекулы РНК, не способна к репликации.
2. В состав белка входят 415 аминокислотных остатков. Сколько нуклеотидов молекулы ДНК кодирует данный белок, триплетов и – РНК переносят информацию о структуре этого белка к месту трансляции, молекул т – РНК необходимо для переноса этих аминокислот? Ответ поясните.
Тест по биологии по теме «Химический состав клетки» 2 вариант
1) Строение и жизнедеятельность растений изучает наука:
А) зоология В) ботаника С) экология Д) эмбриология Е) цитология
2) Источником энергии и воды в организме являются:
А) жиры В) белки С) углеводы Д) нуклеотиды Е) моносахариды
3) Ферментативную функцию в организме выполняют:
А) липиды В) углеводы С) жиры Д) белки Е) полисахариды
4) В состав АТФ входит углевод:
А) дезоксирибоза В) аденин С) глюкоза Д) фруктоза Е) рибоза
5) Жиры состоят из:
А) нуклеиновых кислот В) ферментов С) аминокислот Д) углеводов Е) глицерина и жирных кислот
6) К дисахаридам относится:
А) крахмал В) сахароза С) фруктоза Д) целлюлоза Е) глюкоза
7) При окислении 1 грамма липидов выделяется энергии:
А) 35,2 кДж В) 38,9 кДж С) 16,7 кДж Д) 17,6 кДж Е) 27,6 кДж
8) Азотистое основание аденин входит в состав:
А) аминокислот В) АТФ С) сахарозы Д) углеводов Е) липидов
9) В состав гормона щитовидной железы входит:
А) магний В) иод С) железо Д) фосфор Е) кальций
10) Входит в состав зубной эмали:
А) фтор В) бром С) бор Д) натрий Е) медь
11) Процесс синтеза молекулы белка из аминокислот:
А) транскрипция В) трансляция С) репликация Д) комплементарность Е) редукция
12) Микроэлементов в клетке:
А) 37% В) 98% С) 1,1% Д) 0,02% Е) 76%
13) Нерастворимость веществ в клетке:
А) транскрипция В) трансляция С) гидрофильность Д) редупликация Е) гидрофобность
14) К моносахаридам относится:
А) гликоген В) сахароза С) глюкоза Д) целлюлоза Е) лактоза
15) Изучает взаимоотношение организмов с окружающей средой:
А) экология В) биохимия С) цитология Д) археология Е) эмбриология
16) Двигательную функцию в организме выполняют:
А) жиры В) белки С) углеводы Д) нуклеотиды Е) моносахариды
17) Транспортную функцию в организме выполняют:
А) липиды В) углеводы С) жиры Д) белки Е) полисахариды
18) Сколько в составе АТФ остатков фосфорной кислоты :
А) 1 В) 2 С) 3 Д) 4 Е) 5
19) Липиды состоят из:
А) нуклеиновых кислот В) ферментов С) аминокислот Д) углеводов Е) глицерина и жирных кислот
20) К полисахаридам относится:
А) глюкоза В) сахароза С) фруктоза Д) целлюлоза Е) мальтоза
21) При окислении 1 грамма белков выделяется энергии:
А) 35,2 кДж В) 38,9 кДж С) 16,7 кДж Д) 17,2 кДж Е) 27,6 кДж
22) Азотистое основание гуанин входит в состав:
А) аминокислот В) АТФ С) сахарозы Д) липидов Е) РНК
23) Входит в состав зубов и костей:
А) магний В) иод С) железо Д) фтор Е) кальций
24) Входит в состав белков и нуклеиновых кислот:
А) фтор В) азот С) бор Д) натрий Е) медь
25) Процесс удвоения ДНК:
А) транскрипция В) трансляция С) редупликация Д) комплементарность Е) редукция
2.
ФУНКЦИИ ОРГАНОИДЫ КЛЕТКИ
А) синтез глюкозы 1) аппарат Гольджи
Б) сборка комплексных органических веществ 2) лизосома
В) разрушение временных органов у эмбрионов 3) хлоропласт
Г) поглощение и преобразование солнечной энергии
Д) химическая модификация органических веществ
Е) расщепление биополимеров
Установите последовательность реализации генетической информации.
А) и – РНК
Б) признак
В) белок
Г) ген
Д) ДНК
Часть 3.
1. Найдите ошибки в приведенном ниже тексте, исправьте их, укажите номера предложений, в которых они допущены, запишите эти предложения без ошибок.
1. Биосинтез белка осуществляется в три этапа: гликолиз, транскрипция и трансляция. 2. Транскрипция – это синтез и – РНК, который осуществляется в ядре. 3. В процессе транскрипции ДНК подвергается сплайсингу. 4. В цитоплазме на рибосомах идет сборка белковой молекулы – трансляция.
2. Сколько молекул АТФ будет синтезировано в клетках молочнокислых бактерий и клетках мышечной ткани при окислении 30 молекул глюкозы?
Ключ ответов к тесту «Химический состав клетки»
вопроса, тема1 вариант
2 вариант
1
В
В
2
В
А
3
Д
Д
4
Е
Е
5
С
Е
6
С
В7
Е
В
8
Д
В
9
С
В
10
Д
А
11
С
В
12
В
Д
13
С
Е
14
В
С
15
С
А
16
А
В
17
В
Д
18
Е
С
19
Е
20
А
Д
21
В
Д
22
Е
Е
23
А
Е
24
Д
В
25
А
С
Тест Химический состав клетки.
 | Тест по биологии (10 класс) на тему:
| Тест по биологии (10 класс) на тему:Тест Химический состав клетки. 1 вариант. 10 класс.
А1.Какой из химических элементов содержится в клетках в наибольшем количестве:
1.азот
2.кислород
3.углегод
4.водород
А2.Назовите химический элемент, который входит в состав АТФ, всех мономеров белков и нуклеиновых кислот.
1)N 2)P 3)S 4)Fe
А3.Укажите химическое соединение, которое углеводом НЕ является.
1)лактоза 2)хитин 3)кератин 4)крахмал
А4.Как называется структура белка, которая представляет собой спираль из цепочки аминокислот, свернутую в пространстве клубком?
1)первичная 2)вторичная 3)третичная 4)четвертичная
А5.В клетках животных запасным углеводом является:
1.крахмал
2.целлюлоза
3.глюкоза
4.гликоген
А6.Основным источником энергии для новорожденных млекопитающих является:
1.глюкоза
2.крахмал
3.гликоген
4.лактоза
А7. Укажите группу химических элементов, содержание которых в клетке составляет в сумме 98%.
1) Н, О, S, P 2) Н, С, О, N 3) N, P, H, О 4) С, Н, К, Fe
А8. Какая часть молекул аминокислот отличает их друг от друга?
- радикал 2) карбоксильная группа 3) аминогруппа 4) белок
А9. Какие из углеводов нерастворимы в воде?
- глюкоза 2) крахмал 3) фруктоза 4) рибоза
А10. В каком ответе все названные химические соединения являются белками?
1) сахароза, инсулин, урацил 2) фенилаланин, глюкагон, пепсин 3) глюкоза, фруктоза, гликоген 4) каталаза, глюкагон, кератин
А11. Молекулы жиров образуются:
1)из глицерина,высших карбоновых кислот
2) из глюкозы
3)из аминокислот,воды
4) из этилового спирта,высших карбоновых кислот
А12. Какое значение имеют жиры у животных?
1)теплорегуляция 2)источник энергии 3)источник воды 4)все перечисленное
Часть В ( выберите три верных ответа из шести предложенных)
В1. Какие функции в клетке выполняют углеводы?
- Каталитическую 4) структурную
- Энергетическую 5) запасающую
- Двигательную 6) сократительную
В2. В2. Вид химических связей, которые формируются при образовании различных структур белка:
В2. Вид химических связей, которые формируются при образовании различных структур белка:
1) водородные 2) ковалентные 3) ионные 4) гидрофобные 5) пептидные 6) металлические
В3. Установите соответствие между строением и функцией органического вещества и его видом:
СТРОЕНИЕ И ФУНКЦИИ ВЕЩЕСТВА
А. состоят из остатков молекул глицерина и жирных кислот 1. липиды
Б. состоят из остатков молекул аминокислот 2. Белки
В. Участвуют в терморегуляции
Г. Защищают организм от чужеродных веществ
Д. образуются за счет пептидных связей.
Е. Являются наиболее энергоемкими.
С1. Перечислите не менее 3 свойств воды, и их значение в клетке.
Часть А – 1 балл (максимальное количество 12 баллов)
Часть В – 2 балла (максимальное количество 6 баллов)
Часть С – 3 балла (максимальное количество 3 балла)
Итого : 21 балл
Критерии оценивания:
19 -21 балл – «5»
13 – 18 баллов – «4»
9 – 12 баллов – «3»
1 – 8 баллов – «2»
Тест Химическая организация клетки. 2 вариант. 10 класс
2 вариант. 10 класс
А1.На долю четырех химических элементов приходится 98%всего содержимого клетки. Укажите химический элемент, НЕ относящийся к ним.
1)О 2)Р 3)С 4)N
А2.У детей развивается рахит при недостатке:
1.марганца и железа
2.кальция и фосфора
3.меди и цинка
4.серы и азота
А3.Назовите дисахарид.
1)лактоза 2)фруктоза 3)крахмал 4)гликоген
А4. Как называется структура белка, представляющая собой спираль, которую свернута цепочка из аминокислот?
1)первичная 2)вторичная 3)третичная 4)четвертичная
А5.В клетках растений запасным углеводом является:
1.крахмал
2.целлюлоза
3.глюкоза
4.гликоген
А6.Наибольшее количество энергии выделяется при разложении 1 грамма:
1.жира
2.белка
3.глюкоза
4.углеводов
А7.Что является мономером белка?
1)азотистое основание 2)нуклеотид 3)аминокислота 4)урацил
А8. .Сколько из известных аминокислот участвуют в синтезе белков?
1)-20 2)-100 3)-23 4) 15
А9. В состав какого жизненно важного соединения входит железо?
В состав какого жизненно важного соединения входит железо?
- хлорофилла 2) ДНК 3) гемоглобина 4) РНК
А10. Какую долю в среднем составляет в клетке вода?
1)80% 2) 1% 3)20% 4) 50%
А11. Жиры выполняют в клетке функцию:
1)транспортную 2)энергетическую 3)каталитическую 4)информационную
А12. Вещества,хорошо растворим.в воде-называются:
1)гидрофильные 2)амфифильные 3) аморфными 4)гидрофобные
Часть В ( выберите три верных ответа из шести предложенных)
В1. Липиды выполняют функции:
- Ферментативную 4) транспортную
- Энергетическую 5) запасающую
- Гормональную 6) передача наследственной информации
В2. Вода составляет значительную часть клетки,она…
- регулирует процессы жизнедеятельности
- обеспечивает клетку энергией
- придает клетке упругость
- способствует делению клетки
- является универсальным растворителем
- растворяет любые вещества
В3. Установите соответствие между особенностями и молекулами для которых они характерны.
Установите соответствие между особенностями и молекулами для которых они характерны.
ОСОБЕННОСТИ МОЛЕКУЛЫ
А) хорошо растворяются в воде 1) моносахариды
Б) имеют сладкий вкус 2) полисахариды
В) сладкий вкус отсутствуют
Г) глюкоза, рибоза, фруктоза
Д) в воде нерастворимы
Е) крахмал, гликоген, хитин.
С1. Приведите примеры не менее трех химических элементов имеющих значение для организма человека. Ответ поясните.
Часть А – 1 балл (максимальное количество 12 баллов)
Часть В – 2 балла (максимальное количество 6 баллов)
Часть С – 3 балла (максимальное количество 3 балла)
Итого : 21 балл
Критерии оценивания:
19 — 21 балл – «5»
13 – 18 баллов – «4»
9 – 12 баллов – «3»
1 – 8 баллов – «2»
Тест Химический состав и строение клетки (10 класс) по биологии с ответами онлайн
Сложность: знаток.Последний раз тест пройден 3 часа назад.
Материал подготовлен совместно с учителем высшей категории
Опыт работы учителем биологии — более 19 лет.
Вопрос 1 из 10
В основной состав клетки 80 % входит:
- Правильный ответ
- Неправильный ответ
- Пояснение: Вода — наиболее распространенное неорганическое вещество клетки, обладающее уникальными физико-химическими свойствами. В зависимости от вида клетки, она занимает до 80 % ее объема.
- Вы и еще 86% ответили правильно
- 86% ответили правильно на этот вопрос
В вопросе ошибка?
Следующий вопросОтветитьВопрос 2 из 10
Какой ученый увидел клетку с помощью микроскопа?
- Правильный ответ
- Неправильный ответ
- Пояснение: Английский естествоиспытатель и изобретатель Роберт Гук – первый ученый, рассмотревший клетку под микроскопом.

- Вы и еще 78% ответили правильно
- 78% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 3 из 10
Носителями наследственной информации являются:
- Правильный ответ
- Неправильный ответ
- Пояснение: Носителями наследственной информации в природе являются нуклеиновые кислоты. Известно два вида нуклеиновых кислот: ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота).
- Вы и еще 59% ответили правильно
- 59% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 4 из 10
К прокариотам относятся:
- Правильный ответ
- Неправильный ответ
- Пояснение: Прокариоты – одноклеточные живые организмы, не обладающие (в отличие от эукариот) оформленным клеточным ядром.
 К ним относятся только бактерии, в том числе, кишечная палочка.
К ним относятся только бактерии, в том числе, кишечная палочка. - Вы и еще 66% ответили правильно
- 66% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 5 из 10
Растительные клетки, в отличие от животных, имеют:
- Правильный ответ
- Неправильный ответ
- Пояснение: Только растительные клетки имеют твердую оболочку из клетчатки, хлоропласты для проведения процесса фотосинтеза, вакуоли с клеточным соком.
- Вы и еще 68% ответили правильно
- 68% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 6 из 10
Клетки организмов всех царств живой природы имеют:
- Правильный ответ
- Неправильный ответ
- Пояснение: Цитоплазма — полужидкое содержимое клетки, ее внутренняя среда, ограниченная плазматической мембраной.
 Цитоплазма есть во всех клетках живых организмов, она выполняет важную роль – объединяет собой все клеточные структуры, способствует их взаимодействию друг с другом.
Цитоплазма есть во всех клетках живых организмов, она выполняет важную роль – объединяет собой все клеточные структуры, способствует их взаимодействию друг с другом. - Вы и еще 57% ответили правильно
- 57% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 7 из 10
Основным свойством плазматической мембраны является:
- Правильный ответ
- Неправильный ответ
- Пояснение: Основным свойством плазматической мембраны является избирательная проницаемость. Через нее проходят ионы, аминокислоты, глицерол и жирные кислоты, глюкоза. При этом клеточная мембрана пропускает одни вещества, задерживает другие, в зависимости от потребности клеток.
- Вы и еще 62% ответили правильно
- 62% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 8 из 10
Старые органоиды перевариваются:
- Правильный ответ
- Неправильный ответ
- Пояснение: Лизосомы расщепляют питательные вещества, переваривают попавшие в клетку бактерии, выделяют ферменты, удаляют путем переваривания ненужные части клеток и старые органоиды.
- Вы и еще 62% ответили правильно
- 62% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 9 из 10
В рибосомах в отличие от лизосом происходит:
- Правильный ответ
- Неправильный ответ
- Пояснение: Рибосомы – это молекулярные комплексы из белков и РНК, которые синтезируют все клеточные белки. Лизосомы – это мембранные пузырьки (вакуоли), которые содержат пищеварительные ферменты и переваривают клеточную еду.
- Вы ответили лучше 81% участников
- 19% ответили правильно на этот вопрос
В вопросе ошибка?
ОтветитьВопрос 10 из 10
Какой органоид принимает участие в делении клетки?
- Правильный ответ
- Неправильный ответ
- Пояснение: Клеточный центр принимает участие в делении клеток животных и низших растений.
 В начале деления (в профазе) центриоли расходятся к разным полюсам клетки. От центриолей к центромерам хромосом отходят нити веретена деления. В анафазе эти нити притягивают хроматиды к полюсам. После окончания деления центриоли остаются в дочерних клетках, удваиваются и образуют клеточный центр.
В начале деления (в профазе) центриоли расходятся к разным полюсам клетки. От центриолей к центромерам хромосом отходят нити веретена деления. В анафазе эти нити притягивают хроматиды к полюсам. После окончания деления центриоли остаются в дочерних клетках, удваиваются и образуют клеточный центр. - Вы и еще 75% ответили правильно
- 75% ответили правильно на этот вопрос
В вопросе ошибка?
Ответить
Доска почёта
Чтобы попасть сюда — пройдите тест.
ТОП-5 тестовкоторые проходят вместе с этимТест «Химический состав и строение клетки» с ответами составлен в соответствии с действующей программой, утвержденной министерством. Данная подборка тестов поможет качественно подготовиться к проверочной работе. Вопросы касаются химической организации и строения растительных и животных клеток, проверяют знание органических и неорганических веществ клеточных структур.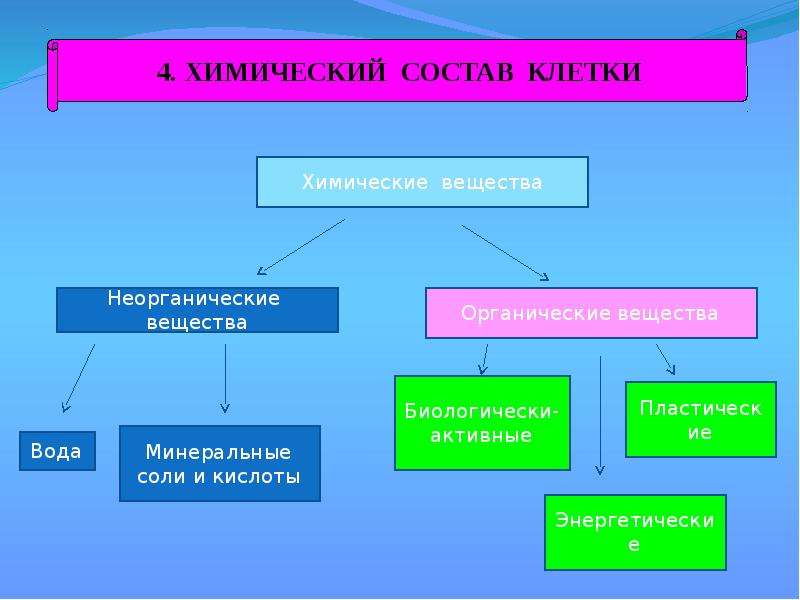
С помощью вопросов теста можно быстро проверить свои знания по теме. Задания удобно просматривать в онлайн режиме с любого доступного устройства. Тесты, проверяющие понимание особенностей животных и растительных клеток, будут полезны при подготовке к ЕГЭ.
Тест по биологии «Химический состав клетки» (10 класс) поможет быстро и качественно оценить знания данной темы, станут отличным помощником для тех, кто хочет подтянуть биологию.
Рейтинг теста
Средняя оценка: 3.7. Всего получено оценок: 891.
А какую оценку получите вы? Чтобы узнать — пройдите тест.
Тест 5. Биология. 10 класс. Химический состав клетки – белки, нуклеиновые кислоты и АТФ.
α-спираль, прошитая водородными связями
последовательность аминокислотных остатков в полипептидной цепи
взаимное расположение нескольких белковых цепей
пространственная конфигурация α-спирали, образованная за счет ковалентных полярных, неполярных и ионных связей
Тест «Химический состав клетки» 10класс
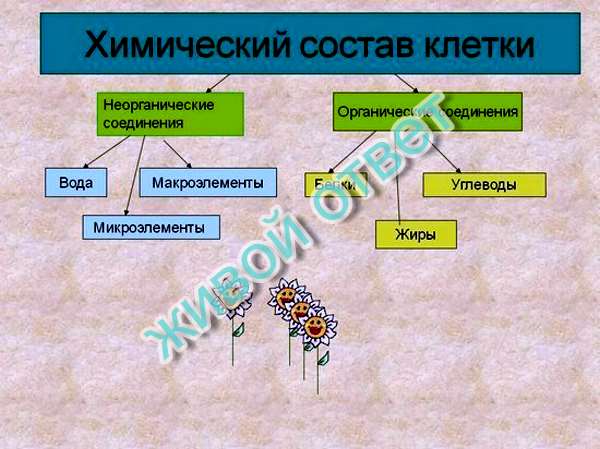
Химический состав клетки
1 . какое из свойств воды обусловлено её полярностью?
какое из свойств воды обусловлено её полярностью?
А) теплопроводимость б) теплоёмкость
в) способность растворят г) способность растворять полярные соединения
неполярные соединения
2. при замерзании воды расстояние между её молекулами:
а) уменьшается б) увеличивается г) не изменяется
3. какие химические связи возникают между атомами в молекуле воды?
А) ковалентно-неполярные б) ковалентно-полярные в) ионные г) водородные
4. какое из названных биохимических соединений не является биополимером?
А) белок б) глюкоза в) ДНК г) целлюлоза
5. в клетках животных запасающим углеводом является:
а) целлюлоза б) крахмал в) глюкоза г) гликоген
6. в каком из соединений химические связи между молекулами наиболее прочны?
А) в целлюлозе б) в гликогене в) в крахмале
7. способность верблюдов хорошо переносить жажду объясняется тем, что жиры6
способность верблюдов хорошо переносить жажду объясняется тем, что жиры6
а) сохраняют воду в организме б) выделяют воду при окислении
в) создают теплоизолирующий слой, уменьшающий испарение
8. наибольшее количество энергии выделяется при расщеплении 1г:
а) жира б) глюкозы в) белков
9. изменяемыми частями аминокислоты является:
а) аминогруппа и карбоксильная группа б) радикал в) карбоксильная группа
г) радикал и карбоксильная группа
10. первичная структура белка удерживается:
а) водородными связями б) пептидными связями в) гидрофобными связями
г) дисульфидными связями
11. порядок расположения нуклеотидов в молекуле ДНК определяет:
а) вторичную и третичную структуру белка б) первичную структуру
в) четвертичную структуру г) все структуры белка
12. какую функцию выполняет и-РНК?
какую функцию выполняет и-РНК?
А) перенос аминокислот на рибосомы б) снятие и перенос информации с ДНК
В) формирование рибосом г) все перечисленные функции
13. если цепь ДНК содержит 28% нуклеотида А, то чему примерно должно равняться количество нуклеотида Г?
а) 14% б) 22% в) 28% г) 44%
14. ферментативную функцию в организме выполняют:
а) углеводы б) нуклеиновые кислоты в) аминокислоты г) белки
15. от последовательности аминокислот в молекуле белка зависит:
а) сложность белковой молекулы
б) количественный аминокислотный состав молекулы белка
в) индивидуальность белков организма
г) размер молекулы
16. информация о последовательности аминокислот в молекуле белка переносится к месту синтеза:
А) ДНК б) т-РНК в) р-РНК г) и-РНК
17. аденин образует комплементарную связь с:
аденин образует комплементарную связь с:
а) гуанином б) аденином в) тимином г) цитозином
18. урацил образует комплементарную связь с:
а) аденином б) тимином в) гуанином г) цитозином
19. комплементарные пары нуклеотидов удерживаются:
а) водородными связями б) ковалентными в) гидрофобными г) дисульфидными
мостиками
20. РНК отличается от ДНК тем, что в её состав входит урацил вместо:
А, Г, Т, Ц
21. ширина двойной спирали ДНК:
100нм, 20нм, 10нм, 2нм
22. в состав белков входит примерно видов аминокислот:
10, 15, 20, 30
23. информация о синтезе одной молекулы белка содержится в:
а) триплете ДНК б) гене в) молекуле ДНК г) рибосоме
24. триплетов сигналов окончания синтеза белка существует:
1, 2, 3, 4
25. перенос аминокислот к месту синтеза белка осуществляет:
перенос аминокислот к месту синтеза белка осуществляет:
а) ДНК б) р-РНК в) т-РНК г) и-РНК
26. укажите химическое соединение, которое играет большую роль в поддержании осмотического давления в клетке:
а) белок б) АТФ в) NaCl г) жир
Тест по биологии «Химический состав клетки»
Заслуга Шлейдена и Шванна в том, что они…
сформулировали основные идеи клеточной теории
опровергли идеи Вихрова
открыли клеточное строение растений и животных
В 1838-1839гг. трудами М.Шлейдена и Т.Шванна были обобщены сведения по изучению растительных и животных клеток, что явилось окончательным обоснованием клеточной теории.
Содержание какого химического элемента в клетке больше чем остальных.
водорода
углерода
кислорода
Содержание кислорода в клетке больше чем остальных химических элементов в клетке (65-75% от массы клетки).
В норме в клетках поддерживается…
кислая реакция
слабощелочная реакция
щелочная реакция
Являясь компонентами буферных систем организма, ионы определяют их свойства — способность поддерживать рН на постоянном уровне (близко к нейтральной реакции), несмотря на то, что в процессе обмена веществ непрерывно образуются кислые и щелочные продукты. Буферная система млекопитающих поддерживает рН внутриклеточной жидкости в пределах 6,9 — 7,4 (слабощелочная реакция).
Вода способна образовать гидрат-ионы потому, что…
молекулы воды соединены водородными связями
молекулы воды полярны и вода легко диссоциирует
нет ответа
Благодаря полярности своих молекул вода выступает в роли стабилизатора структуры. Вода обладает способностью распадаться (диссоциировать) на два иона: (H+ + OH-).
Аминокислоты — это…
кислоты
основания
нуклеотиды
Аминокислоты — относительно низкомолекулярные соединения, в состав которых, кроме углерода, кислорода, водорода, входят азот в виде одной или двух аминогрупп и одна или две карбоксильные группы. Карбоксильные группы придают молекулам кислотные свойства, а аминогруппы свойства оснований. Благодаря амфотерным свойствам аминокислоты в клетке играют роль буферных соединений.
Какое из соединений не построено из аминокислот?
гемоглобин
инсулин
гликоген
Гликоген — сложный углевод (полисахарид), подобный крахмалу. Молекулы построены из остатков одного из видоизменений (изомеров) глюкозы.
Изменяемой частью аминокислоты является…
карбоксильная группа
аминогруппа
радикал
В состав всех аминокислот входят амино- и карбоксильные группы. Боковые же цепи (радикалы) аминокислот различаются. Химическая природа радикалов разнообразна: от атома водорода до циклических соединений. Именно радикалы определяют структурные и функциональные особенности аминокислот.
Мономерами ДНК и РНК являются…
азотистые основания
нуклеотиды
дезоксирибоза и рибоза
Нуклеиновые кислоты являются биополимерами, состоящими из мономеров — нуклеотидов. Нуклеотиды, входящие в состав ДНК, содержат дезоксирибозу, остаток фосфорной кислоты и одно из четырёх азотистых оснований. Молекула РНК — полимер, состоящий из одной цепочки. Мономерами РНК являются нуклеотиды, состоящие из рибозы, остатка фосфорной кислоты и одного из четырёх азотистых основания (тимин заменён на урацил).
Денатурировать могут…
все структуры белка
только вторичная и первичная
только третичная и четвертичная
Денатурация — процесс нарушения нативной (естественной) структуры белка. Денатурировать могут все структуры белка.
Активность фермента определяется…
наличием в нём водородных связей
строением его активного центра
количеством аминокислот в его составе
Активный центр — определённая, специфическая для каждого фермента группа аминокислот, которые осуществляют преимущественно реакции гидролиза.
Самая крупная РНК.
рибосомальная
матричная
транспортная
Самая крупная РНК синтезируется в основном в ядрышке и составляет примерно 85% всех РНК клетки. Они входят в состав рибосом и участвуют в формировании активного центра рибосомы.
Из перечисленных ниже белков защитную функцию выполняет…
актин
казеин
интерферон
Специфические белки выполняют защитную функцию. Они предохраняют организм от вторжения чужеродных организмов и от повреждения. Так, интерфероны — универсальные противовирусные белки (блокируют синтез вирусного белка в инфицированной клетке).
К рецепторным белкам из перечисленных относится…
родопсин
ботулин
инсулин
Родопсин — светочувствительный пигмент (хромопротеин) фоторецепторных клеток сетчатки глаза позвоночных — является в настоящее время одним из наиболее изученных мембранных белков.
Углеводы синтезируются из…
углекислого газа и воды
кислорода и углекислоты
углекислого газа и водорода
Углеводы синтезируются из неорганических веществ (воды и углекислого газа) в процессе фотосинтеза, происходящего в хлоропластах зелёных растений.
К дисахаридам из перечисленных относится…
фруктоза
лактоза
целлюлоза
Лактоза — молочный сахар. Источник углеводов для детёнышей млекопитающих, в том числе человека. Молоко содержит около 5% лактозы. Состав: глюкоза + галактоза.
Следующий вопросПодробный ответ
Химический состав клетки. 10 класс
Тренировочные тесты ЕГЭ. Биология.
Тема: Химический состав клетки. 10 класс
Часть А
1. Живые организмы нуждаются в азоте, так как он служит
1.составным компонентом белков и нуклеиновых кислот 2.основным источником энергии 3.структурным компонентом жиров и углеводов 4.основным переносчиком кислорода
2. Вода играет большую роль в жизни клетки, так как она 1.участвует во многих химических реакциях 2. обеспечивает нормальную кислотность среды 3. ускоряет химические реакции 4.входит в состав мембран
3. Основным источником энергии в организме являются:
1)витамины 2.ферменты 3. гормоны 4.углеводы
4.Органические вещества в клетке перемещаются к органоидам по
1.системе вакуолей 2.лизосомам 3.митохондриям 4.эндоплазматической сети
4.В клетках каких организмов содержится в десятки раз больше углеводов, чем в клетках животных?
1. бактерий-сапротрофов 2.одноклеточных 3.простейших 4.растений
5.В клетке липиды выполняют функцию:
1) каталитическую 2)транспортную 3.информационную 4.энергетическую
6.В клетках человека и животных в качестве строительного материала и источника энергии используются 1.гормоны и витамины 2.вода и углекислый газ 3.неорганические вещества 4.белки, жиры и углеводы
7 Жиры, как и глюкоза, выполняют в клетке функции: 1)строительную 2.информационную 3.каталитическую 4. энергетическую
8. Укажите какую форму имеет вторичная структура молекулы белка
9.В состав ферментов входят :
1.нуклеиновые кислоты 2.белки 3.молекулы АТФ 4.углеводы
10.Четвертичная структура молекул белка формируется в результате взаимодействия :
1. аминокислот и образования пептидных связей 2.нескольких полипептидных нитей 3.участков одной белковой молекулы за счет водородных связей 4.белковой глобулы с мембраной клетки
11.Какую функцию выполняют белки, вырабатываемые в организме при проникновении в него бактерий или вирусов? 1)регуляторную 2.сигнальную 3.защитную 4.ферментативную
12.Разнообразные функции в клетке выполняют молекулы
1)ДНК 2) белков 3)иРНК 4) АТФ
13.Какую функцию выполняют белки, ускоряющие химиче ские реакции в клетке?
1)гормональную 2)сигнальную 3.ферментативную 4.информационную
14.Программа о первичной структуре молекул белка зашифрована в молекулах
1)тРНК 2) ДНК 3)липидов 4) полисахаридов
15.В молекуле ДНК две полинуклеотидные нити связаны с помощью
1комплементарных азотистых оснований 2.остатков фосфорной кислоты 3.аминокислот 4.углеводов
16. Связь, возникающая между азотистыми основаниями двух комплементарных цепей ДНК, —
1)ионная 2) пептидная 3)водородная 4) ковалентная полярная
17.Благодаря свойству молекул ДНК воспроизводить себе подобных,
1.формируется приспособленность организма к среде оби тания
2.у особей вида возникают модификации 3.появляются новые комбинации генов
4.наследственная информация передается от материнской клетки к дочерним
18.Молекулы ДНК представляют собой материальную основу наследственности, так как в них закодирована информация о структуре молекул 1.полисахаридов2.белков 3)липидов 4)аминокислот
19. В молекуле ДНК 100 нуклеотидов с тимином, что составляет 10% от общего количества. Сколько нуклеотидов с гуанином?
1.400 2. 2003 3. 10004 4. 1800
20. Наследственная информация о признаках организма сосредоточена в молекулах
1.тРНК 2. ДНК 3.белка 4.полисахаридов
21. Рибонуклеиновые кислоты в клетках участвуют в
1.хранении наследственной информации 2.биосинтезе белков
3.биосинтезе углеводов 4.регуляции обмена жиров
22.Молекулы и-РНК, в отличие от т-РНК,
1.служат матрицей для синтеза белка 2.служат матрицей для синтеза тРНК
3.доставляют аминокислоты к рибосоме 4.переносят ферменты к рибосоме
23.Молекула и-РНК осуществляет передачу наследственной информации
1.из ядра к митохондрии 2.из одной клетки в другую
3.из ядра к рибосоме 4.от родителей потомству
24.Молекулы РНК, в отличие от ДНК, содержат азоти стое основание
1)аденин 2)гуанин 3.урацил 4. цитозин
25.Рибоза, в отличие от дезоксирибозы, входит в состав 1)ДНК 2) иРНК 3)белков 4) полисахаридов
26.Процесс денатурации белковой молекулы обратим, если не разрушены связи
1)водородные 2.пептидные 3.гидрофобные 4.дисульфидные
27.АТФ образуется в процессе 1.синтеза белков на рибосомах 2.разложения крахмала с образованием глюкозы 3.окисления органических веществ в клетке 4.фагоцитоза
28.Мономером молекулы белка служит
1) азотистое основание 2) моносахарид 3) аминокислота 4) липиды
29.Большинство ферментов являются
1) углеводами 2) липидами 3) аминокислотами 4) белками
30.Строительная функция углеводов состоит в том, что они
1) образуют целлюлозную клеточную стенку у растений 2) являются биополимерами
3) способны растворяться в воде 4) служат запасным веществом животной клетки
31. Важную роль в жизни клетки играют липиды, так как они 1) являются ферментами
2)растворяются в воде 3)служат источником энергии 4)поддерживают постоянную среду в клетке
32.Синтез белков у эукариот происходит: 1. на рибосомах 2. на рибосомах в цитоплазме
3.на клеточной мембране 4. на микрофиламентах в цитоплазме.
33. Первичная, вторичная и третичная структуры молекулы характерны для:
1.гликогена 2.аденина 3.аминокислоты 4.ДНК.
Часть В
1.В состав молекулы РНК входит
А)рибоза Б)гуанин В) катион магния Г) дезоксирибоза Д) аминокислота Е) фосфорная кислота
Запишите ответ в виде последовательности букв в алфавитном порядке (без пробелов и других символов).
2.Установите соответствие между функцией соединения и биополимером, для которого она характерна. В нижеприведенной таблице под каждым номером, определяющим позиции первого столбца, запишите букву, соответствующей позиции второго столбца.
ФУНКЦИЯ
1) хранение наследственной информации БИОПОЛИМЕР А)белок Б) ДНК
2} образование новых молекул путем самоудвоения
3) ускорение химических реакции
4) является обязательным компо нентом мембраны клетки
5) обезвреживание антигенов
Запишите в таблицу получившуюся последовательность букв и перенесите в бланк ответов (без пробелов и других символов).
3.Установите соответствие между функцией соединения и биополимером, для которого она характерна. В нижеприведенной таблице под каждым номером, определяющим позиции первого столбца, запишите букву, соответствующей позиции второго столбца.
ФУНКЦИЯ
1) образование клеточных стенок БИОПОЛИМЕР А) полисахарид Б) нуклеиновая кислота
2) транспортировка аминокислот
3) хранение наследственной информации
4) служит запасным питатель ным веществом
5) обеспечивает клетку энергией
Запишите в таблицу получившуюся последовательность букв и перенесите в бланк ответов (без пробелов и других символов).
Часть С
1.В одной цепочке молекулы ДНК имеется 31% адениловых остатков, 25% тимидиловых остатков и 19% цитидиловых остатков. Рассчитайте, каково процентное соотношение нуклеотидов в двухцепочечной ДНК.
2.Найдите ошибки в приведенном тексте, исправьте их, укажите номера предложений, в которых они сделаны, запишите эти предложения без ошибок.
1. Белки — это биологические полимеры, 2. Мо номерами белков являются аминокислоты. 3. В состав белков входит 30 равных аминокислот. 4. Все аминокислоты могут синтезироваться в организме человека и животных. 5. Аминокислоты соединяются в молекуле белка нековалентными пептидными связями.
3.Содержение нуклеотидов в цепи иРНК следущее: А-35%, Г-27%,Ц-18%, У-20%. Определите процентный состав нуклеотидов участка 2-цепочечной молекулы ДНК, являющегося матрицей для этой иРНК.
4.Сколько молекул АТФ будет синтезировано в клетках эукариот при полном окислении фрагмента молекулы крахмала, состоящего из 10 остатков глюкозы?5.Какова роль белков в организме?
6.Найдите ошибки в приведенном тексте. Укажите номера предложений, в которых они сделаны. Объясните их. 1. Все присутствующие в организме белки — ферменты.2. Каждый фермент ускоряет течение нескольких химических реак ций. 3. Активный центр фермента строго соответствует конфигурации субстрата, с которым он взаимодействует. 4. Активность ферментов не зависит от таких факторов, как температура, рН среды, и других факторов.
7. Найдите ошибки в приведенном тексте. Укажите номера предложений, в которых они допущены, объясните их.
1. Информационнная РНК синтезируется на молекуле ДНК. 2. Ее длина не зависит от объема копируемой информации. 3. Количество и-РНК в клетке составляет 85% от всего количества в клетке.
4. В клетке существует три вида тРНК. 5. Каждая тРНК присоединяет определенную аминокислоту и экспортирует ее к рибосомам. 6. У эукариот т-РНК намного длиннее, чем и-РНК.
8.Укажите номера предложений, в которых допущены ошибки. Объясните их.
1. Углеводы представляют собой соединения углерода и водород
2. Различают три основных класса углеводов — моносахариды, сахариды и полисахариды.
3. Наиболее распространенные моносахариды — сахароза и лактоза.
4. Они растворимы в воде и обладают сладким вкусом.
5. При расщеплении 1 г глюкозы выделяется 35,2 кДж энергии
9. В чем сходство и различие РНК,ДНК,АТФ?
10 Почему глюкоза не выполняет в клетке запасающую роль?
Напишите на обратной стороне бланка или на отдельном листе краткий ответ, включающий не менее двух элементов.
11.Почему крахмал относят к биополимерам и какое свойство крахмала обуславливает его запасающую функцию в клетке?
Органические соединения | Химия жизни
1.4 Органические соединения (ESG49)
Учащиеся будут изучать углеводы, липиды, белки и нуклеиновые кислоты под следующими заголовками:
- Молекулярный состав : основные элементы, составляющие класс соединений.
- Структурный состав : как мономеры соединяются вместе с образованием полимеров.
- Биологическая роль : важность этих молекул для животных и растений.
- Химический тест : как определить присутствие каждого класса соединений.
Есть также объяснение ферментов в разделе белков. Этот раздел главы содержит наиболее практическую работу, поэтому следует уделить много времени рассмотрению этого раздела.
Органическое соединение — это соединение, молекулы которого содержат C и обычно по крайней мере одну связь C-C или C-H. Очень маленькие углеродсодержащие молекулы, которые не подчиняются указанным выше правилам, такие как \ (\ text {CO} _ {2} \) и простые карбонаты, считаются неорганическими.Жизнь на Земле была бы невозможна без углерода. Помимо воды, большинство молекул живых клеток основаны на углероде и, следовательно, называются органическими соединениями. Основные классы органических соединений, которые мы рассмотрим в этом разделе, включают углеводы, липиды, белки и нуклеиновые кислоты.
Каждый из этих классов соединений состоит из больших молекул, построенных из малых субъединиц. Самая маленькая из этих субъединиц называется мономером . Несколько мономеров связываются вместе с образованием полимеров .Каждый из этих полимеров характеризуется определенной структурой за счет образующихся химических связей. Эти структуры связаны с функцией соединения в живых организмах. Поэтому мы будем изучать каждый класс соединений под следующими заголовками:
- Молекулярный состав : основные элементы, составляющие класс соединений.
- Структурный состав : как мономеры соединяются вместе с образованием полимеров.
- Биологическая роль : важность этих молекул для животных и растений.
- Химический тест : как определить присутствие каждого класса соединений.
Углеводы (ESG4B)
Молекулярный состав
Углеводы состоят из углерода (C), водорода (H) и кислорода (O).
Рис. 1.6: Молекула глюкозы состоит из углерода (серые сферы), водорода (белые сферы) и кислорода (красные сферы).
Конструкционный состав
Углеводы состоят из мономеров, известных как моносахаридов .Моносахарид, из которого состоит большинство углеводов, — это глюкоза. Другие моносахариды включают фруктозу, галактозу и дезоксирибозу (обсуждается позже). Эти мономеры могут быть соединены гликозидными связями. Когда два моносахарида химически связаны вместе, они образуют дисахаридов . Примером дисахарида является сахароза (столовый сахар), который состоит из глюкозы и фруктозы. Другие диссахариды включают лактозу, состоящую из глюкозы и галактозы, и мальтозу, состоящую из двух молекул глюкозы.Моносахариды и диссахариды часто называют сахарами или простыми углеводами. Несколько моносахаридов объединяются с образованием полисахаридов . Примеры полисахаридов, с которыми вы столкнетесь, включают гликоген, крахмал и целлюлозу. Полисахариды обычно называют сложными углеводами, так как они дольше расщепляются.
Рисунок 1.7: Примеры пищевых источников различных моносахаридов, дисахаридов и полисахаридов.
Роль у животных и растений
Основная функция углеводов — это молекулы хранения энергии и субстраты (исходный материал) для производства энергии.Углеводы расщепляются живыми организмами с выделением энергии. Каждый грамм углеводов обеспечивает около 17 килоджоулей (кДж) энергии. Крахмал и гликоген являются запасными полисахаридами (полимеры, состоящие из мономеров глюкозы) и, таким образом, действуют как хранилище энергии в живых организмах. Крахмал является запасным полисахаридом в растениях, а гликоген — запасным полисахаридом для животных. Целлюлоза содержится в стенках клеток растений и придает им силы. Все полисахариды состоят из мономеров глюкозы, но различие в свойствах этих веществ может быть связано с тем, как молекулы глюкозы соединяются вместе, образуя разные структуры.Ниже представлены изображения гликогена и крахмала.
Рисунок 1.8: Сравнение крахмала и гликогена. Гликоген более разветвлен, чем крахмал.
Химические тесты для определения наличия крахмала
Вещества, содержащие крахмал, приобретают сине-черный цвет в присутствии раствора йода. Таким образом, наблюдаемое изменение цвета является основой химического теста на соединение.
Рис. 1.9: Гранулы пшеничного крахмала, окрашенные раствором йода и сфотографированные с помощью светового микроскопа.
В следующем исследовании мы проверим несколько различных продуктов на наличие крахмала.
Тест на наличие крахмала
(Essential research-CAPS)Aim
Для проверки наличия крахмала.
Аппарат
- кусок картофеля или хлеба
- лист салата
- чашка Петри
- раствор йода
- капельница
- других блюд на ваш выбор
Метод
- Поместите кусочек картофеля или хлеба, лист салата и другие образцы пищи в отдельные чашки Петри.
- С помощью пипетки добавьте несколько капель раствора йода в продукт в каждой чашке Петри.
Рис. 1.10: Схема эксперимента: испытание на наличие крахмала с использованием раствора йода.
Наблюдения
Запишите свои наблюдения.
Картофель или хлеб становятся сине-черными в присутствии раствора йода, а лист салата — нет.
Вопросы
Можно ли этим методом определить , сколько присутствует крахмал ? Поясните свой ответ.
Да. Чем насыщеннее сине-черный цвет, тем выше содержание крахмала. Если присутствует только немного крахмала, полученный цвет выглядит более бледным и пурпурным, чем черный. Если крахмала нет совсем, видны только цвет исходного материала (например, зеленого листа) и желто-коричневый цвет раствора йода.
Посмотрите видео демонстрацию теста на крахмал.
Видео: 2CMK
Посмотрите видео демонстрацию теста на крахмал.
Видео: 2 см
Посмотрите видео демонстрацию теста на крахмал.
Видео: 2CMN
Химический тест для определения присутствия редуцирующих сахаров
Некоторые моносахариды, такие как глюкоза, известны как редуцирующие сахара . Они определяются как сахара, которые могут легко подвергаться реакциям окисления (т.е. терять электрон или приобретать атом кислорода) и действовать как восстановитель . Чтобы проверить углеводы, мы обычно проверяем наличие редуцирующих сахаров с помощью теста Benedict или Fehling .Оба раствора (Бенедикта и Фелинга) содержат сульфат меди, который вступает в реакцию с редуцирующими сахарами, вызывая изменение цвета.
Посмотрите видео демонстрацию теста на глюкозу.
Видео: 2CMP
Тестирование на наличие редуцирующих сахаров
(Essential research-CAPS)Aim
Для проверки наличия сахаров с помощью теста Бенедикта или Фелинга.
Аппарат
- 4 термостойкие пробирки
- 1 стакан
- Горелка Бунзена или водяная баня с горячей водой (+50 \ (^ {\ circ} \) C)
- Штатив для пробирок (при использовании водяной бани)
- раствор глюкозы
- раствор белка или яичного белка
- раствор крахмала
- вода
- Решение Бенедикта ИЛИ Решение Фелинга
- маркер для маркировки пробирок
- термометр
- \ (\ text {10} \) \ (\ text {ml} \) шприц или мерный цилиндр
Меры предосторожности
- Соблюдайте правила техники безопасности (перечисленные в главе 1) при розжиге горелки Бунзена.Не зажигайте его на полке или в замкнутом пространстве. Уберите с места все блокноты, бумаги и излишки химикатов. Соберите длинные волосы, свисающие украшения и свободную одежду и никогда не оставляйте открытое пламя без присмотра, пока оно горит.
- При нагревании пробирок в горячей воде в мензурках убедитесь, что устья пробирок направлены в сторону от вас и других учеников.
- При обращении с пробирками, особенно когда они горячие, используйте держатель для пробирок и надевайте защитные очки.
Метод
Приготовьте водяную баню, наполнив стакан водой до половины. Поместите химический стакан на штатив над пламенем Бунзена, как показано на рисунке 1.11. Это послужит вашей водяной баней.
ПРИМЕЧАНИЕ ДЛЯ УЧИТЕЛЯ: Для этого не обязательно использовать водяную баню. Пробирки можно нагревать напрямую. Однако необходимо иметь водяную баню, если у учителя нет газа и он вынужден использовать электрическую плиту.
Пока вода не достигнет желаемой температуры, выполните следующие инструкции:
- Пометьте пробирки 1–4.
- С помощью шприца или мерного цилиндра добавьте в пробирки следующее:
- Пробирка
- 1: \ (\ text {5} \) \ (\ text {ml} \) раствора крахмала \ (\ text {1} \% \)
- пробирка 2: \ (\ text {5} \) \ (\ text {ml} \) из \ (\ text {10} \% \) раствора глюкозы
- пробирка 3: \ (\ text {5} \) \ (\ text {ml} \) \ (\ text {1} \% \) раствор белка
- пробирка 4: \ (\ text {5} \) \ (\ text {ml} \) вода.
- Добавьте \ (\ text {5} \) \ (\ text {ml} \) раствор Бенедикта в каждую пробирку.{\ circ} \) В.
- Примерно через \ (\ text {5} \) минут, когда в некоторых пробирках произошло изменение цвета, погасите пламя или выньте пробирки из водяной бани.
- Поместите четыре пробирки в штатив для пробирок и сравните цвета.
Рисунок 1.11: Тест на восстановление сахара с использованием теста Бенедикта
Результаты
Создайте таблицу для записи результатов этого эксперимента. Важно наблюдать и записывать любые произошедшие изменения.
| Номер пробирки | Наблюдения в каждой пробирке |
Вопросы
- Какие изменения цвета (если таковые имеются) вы наблюдали после нагрева раствора с Бенедом?
- Три протестированных раствора являются примерами химических веществ, обнаруженных в клетках: глюкоза, крахмал, белок (белок). Какой из образцов дал положительный результат при добавлении раствора Бенедикта и нагревании пробирки?
- Какие изменения произошли в консистенции раствора Бенедикта, кроме цвета?
- Какие выводы можно сделать по результатам расследования?
- Почему в пробирку 4 попала вода?
Ответы
- Содержимое пробирки 2 становится желто-оранжевым, остальные остаются синими.
- Только глюкоза.
- Он стал немного гуще / свернулся.
- Любое другое тестируемое нами вещество, которое также становится желто-оранжевым при нагревании с раствором Бенедикта, содержит глюкозу или редуцирующий сахар.
- Это контроль, чтобы показать, что раствор Бенедикта вступает в реакцию с другим веществом в пробирке, а не с водой, в которой была растворена глюкоза.
Посмотрите видео-демонстрацию теста на снижение содержания сахара.
Видео: 2CMQ
Посмотрите видео-демонстрацию теста на снижение содержания сахара.
Видео: 2CMR
Липиды (ESG4C)
Молекулярный состав
Липиды содержат углерод (C), водород (H) и кислород (O), но содержат меньше кислорода, чем углеводы. Примеры липидов в рационе включают кулинарные масла, такие как подсолнечное и оливковое масло, сливочное масло, маргарин и сало. Многие орехи и семена также содержат большое количество липидов.
Конструкционный состав
Триглицериды — один из наиболее распространенных типов липидов.Молекулы триглицеридов состоят из глицерина и трех жирных кислот (рис. 1.12). Хвосты жирных кислот состоят из множества атомов углерода, соединенных вместе. Количество атомов углерода в цепях жирных кислот может быть разным.
При рисовании органических молекул легко запутаться, выписывая все буквы C и H для углерода и водорода соответственно. Ученые преодолевают это, вытягивая углеродную основу и исключая водород. Углерод всегда будет образовывать 4 связи с другими атомами, поэтому легко вычислить, сколько должно быть атомов водорода.Углерод обозначен точкой, а связи между молекулами углерода обозначены линиями, соединяющими точки.
Рис. 1.12: Молекула триглицерида.
Роль у животных и растений
Липиды являются важным запасом энергии и содержат 37,8 килоджоулей (кДж) энергии на грамм. Липиды триглицеридов расщепляются с высвобождением глицерина и жирных кислот. Глицерин можно преобразовать в глюкозу и использовать в качестве источника энергии, однако большая часть энергии, обеспечиваемой липидами, происходит за счет разрушения цепей жирных кислот.Некоторые жирные кислоты являются незаменимыми питательными веществами, которые не могут вырабатываться организмом и должны потребляться в небольших количествах. Заменимые жирные кислоты могут вырабатываться в организме из других соединений.
Липиды важны для пищеварения и транспортировки основных витаминов, помогают защитить органы тела от шока и помогают поддерживать температуру тела. Липиды также играют важную роль в клеточных мембранах.
Вы узнаете о важной роли, которую липиды играют в клеточных мембранах, из следующей главы, посвященной основным единицам жизни .
Насыщенные и ненасыщенные жиры
Углерод может образовывать четыре связи с другими атомами. Большинство атомов углерода в цепи жирной кислоты связано с двумя соседними атомами углерода и с двумя атомами водорода. Когда каждый атом углерода в цепи жирной кислоты образует четыре одинарные связи и имеет максимальное количество атомов водорода, цепь жирной кислоты называется насыщенной , потому что она «насыщена» атомами водорода. Однако иногда два соседних атома углерода образуются из двойной связи. В этом случае каждый атом углерода, участвующий в двойной связи, присоединен только к одному водороду.Жирные кислоты, которые имеют двойные связи углерод-углерод, известны как ненасыщенные , потому что двойная связь может быть «разорвана» и может образоваться дополнительная связь с водородом. Двойные связи сильнее одинарных, и они придают цепи жирной кислоты изгиб. Эти изгибы означают, что молекулы не могут плотно упаковываться вместе, и липиды более текучие. Вот почему ненасыщенные жиры имеют тенденцию быть жидкими при комнатной температуре, а насыщенные жиры — твердыми. Жирная кислота цепи с множеством двойных связей называются полиненасыщенными жирными кислотами.
Рис. 1.13: Жирные кислоты могут быть насыщенными, мононенасыщенными или полиненасыщенными в зависимости от количества присутствующих двойных связей. Двойные связи приводят к «перегибам» в цепи жирных кислот.
Холестерин
Холестерин — это органическое химическое вещество, известное как стерол . От вас не требуется понимать его молекулярный состав или структурный состав. Это важный компонент клеточных мембран. Основные пищевые источники холестерина включают сыр, яйца, свинину, птицу, рыбу и креветки.Холестерин переносится через организм с помощью белков крови, известных как липопротеинов . Липопротеин — это любая комбинация липида и белка.
Холестерин переносится с кровью через организм липопротеинами высокой плотности , липопротеинами низкой плотности и триглицеридами.
- Липопротеины низкой плотности (ЛПНП) : Липопротеины низкой плотности переносят холестерин по всему телу. В нем более высокая доля холестерина по сравнению с белком.Его часто называют «плохим» холестерином, потому что более высокий уровень ЛПНП связан с сердечными заболеваниями.
- Липопротеины высокой плотности (ЛПВП) : Липопротеины высокой плотности — самые маленькие из липопротеинов. Он имеет высокую долю белка по сравнению с холестерином и поэтому часто известен как «хороший» холестерин. ЛПВП переносит холестерин от клеток в печень, где он расщепляется или выводится из организма в виде отходов.
Вы узнаете больше о том, как холестерин может закупорить артерии и привести к сердечным заболеваниям, в главе о транспортных системах у животных
Высокий уровень ЛПНП может вызвать сердечные заболевания.Холестерин накапливается в кровеносных сосудах, по которым кровь идет от сердца к тканям и органам тела, называемым артериями. Это приводит к затвердеванию и сужению этих сосудов, что препятствует транспортировке крови и потенциально может привести к сердечному приступу. Самый большой вклад в количество холестерина в крови — это тип жиров, которые вы едите. Насыщенные жиры менее полезны, чем ненасыщенные, поскольку они увеличивают количество холестерина ЛПНП в крови.
Тест на липиды
Тест на липиды основан на том факте, что липиды оставляют полупрозрачное «жирное пятно» на коричневых бумажных пакетах, в то время как нелипидные вещества этого не делают.
Посмотрите видео, демонстрирующее тест на липиды.
Видео: 2CMS
Translucent означает, что объект пропускает свет.
Тест на наличие липидов
(Essential research-CAPS)Aim
Для проверки на наличие липидов.
Аппарат
- кусок бумаги или бумажный пакет «рыба с жареным картофелем»
- пищевые продукты, например, картофель фри, кусок горячего мяса и т. Д.
- 10 мл растительного масла (положительный контроль)
- 10 мл воды (отрицательный контроль)
Метод
- Положительный контроль : добавьте кулинарное масло в коричневый бумажный пакет, пока оно не впитается.Часть бумаги, впитывающая масло, должна быть полупрозрачной по сравнению с той, которая не пропускает масло.
- Отрицательный контроль : смочите бумагу водой. Бумага может стать влажной и намокшей, но она не должна стать полупрозрачной.
- Экспериментальные образцы : испачкайте коричневый бумажный пакет исследуемым продуктом питания и поднесите его к свету. Если он полупрозрачный, как и в положительном контроле, пищевой продукт содержит липид.
Наблюдения
Запишите свои наблюдения, отмечая все ключевые различия между контролем и экспериментальным образцом.
Бумага стала полупрозрачной, когда на нее поместили маслянистую пищу, так же, как полупрозрачное пятно на бумаге, содержащей растительное масло. Бумага, содержащая воду, была влажной, но легко высыхала и никогда не была полупрозрачной, поэтому мы можем сделать вывод, что еда содержала масла или липиды, а не воду.
Альтернативные методы определения липидов
Альтернативный метод проверки наличия липидов в образце — это измельчение или растворение образца в этаноле. Жиры и липиды растворяются в спирте.После приготовления раствора этанола есть два способа проверить, содержит ли этот образец липиды:
- Отфильтруйте раствор этанола через фильтровальную бумагу: липидов, растворенных в этаноле, сделают фильтровальную бумагу полупрозрачной. Как только спирт испарится, останется полупрозрачное пятно.
- Добавьте образец этанола в воду: липидов не растворяются в воде. Следовательно, если раствор этанола содержит липиды, липиды выпадут в осадок из раствора при смешивании с водой, в результате чего раствор станет молочным.
Белки (ESG4D)
Молекулярный состав
Белки содержат углерод (C), водород (H), кислород (O), азот (N) и могут содержать другие элементы, такие как железо (Fe), фосфор (P) и серу (S).
Конструкционный состав
Белки состоят из аминокислот . Существуют \ (\ text {20} \) распространенные аминокислоты, из которых состоят все белки в живых организмах. Девять из них считаются незаменимыми аминокислотами , поскольку они не могут синтезироваться в организме из других соединений и должны быть получены с пищей.Аминокислоты связаны вместе пептидными связями с образованием пептидов . Длинная пептидная цепь образует белок, который складывается в очень специфическую трехмерную форму. Эта трехмерная форма полностью определяется идентичностью и порядком аминокислот в пептидной цепи. Мы часто называем четырьмя различными уровнями структуры белка (рис. 1.14):
Поскольку последовательность аминокислот определяет способ сворачивания белка, если вы начнете с определенной пептидной цепи, вы всегда получите одну и ту же трехмерную структуру!
- Первичная структура : Это относится к последовательности аминокислот, соединенных пептидными связями с образованием полипептидной цепи.Некоторые белки содержат менее сотни аминокислот, а другие — несколько тысяч.
- Вторичная структура : это первый уровень трехмерного складывания. Он полностью управляется водородной связью . Водородная связь обычно приводит к тому, что области намотки цепи и другие области образуют листы.
- Третичная структура : это второй уровень трехмерного фолдинга и общая окончательная форма белковой молекулы.Вторичные структуры и неструктурированные области цепи дополнительно складываются в глобулярную форму за счет гидрофобных взаимодействий (неполярные области, пытающиеся покинуть воду в клеточной среде) и электростатических взаимодействий (полярные и заряженные области, желающие взаимодействовать с водной средой). и друг друга).
- Четвертичная структура : Некоторые белки являются сложными: две или более пептидных цепей складываются в свои третичные структуры, затем эти полные структуры связываются вместе посредством гидрофобных и электростатических взаимодействий с образованием конечного белка.
Рисунок 1.14: Первичный, вторичный, третичный и четвертичный уровни структуры белка
Роль у животных и растений
Белки играют важную роль в нескольких важнейших биологических функциях. Белки содержатся в волосах, коже, костях, мышцах, сухожилиях, связках и других структурах и выполняют ключевые структурные и механические функции. Белки также важны для клеточной коммуникации и иммунной системы. Белки также могут действовать как запас энергии при расщеплении в процессе пищеварения.Каждый грамм белка может быть расщеплен, чтобы высвободить 17 кДж энергии. Определенные белки, называемые ферментами , играют важную роль в катализе клеточных реакций, которые являются частью метаболизма.
Белки необходимы для любой диеты. Недостаток белка приводит к болезни, называемой квашиоркор (рис. 1.15) или маразм (рис. 1.16). Маразм вызывается общим дефицитом питания (голоданием), а квашиоркор — именно недостатком белка.
Рисунок 1.15: Ребенок, страдающий от квашиоркора | Рисунок 1.16: Ребенок, страдающий маразмом |
Мясо или овощи: какой источник белка лучше?
И животный белок, и белок овощей полезны для здоровья. Но каждый тип содержит другие питательные вещества. Итак, какой «пакет» питательных веществ — мясо или овощи — лучше для здоровья?
- 180-граммовый стейк содержит 40 г белка, НО также содержит 38 г жира, что больше, чем рекомендуемая диета
- Из такого же количества лосося получается 34 г белка и 18 г жира.
- В стакане вареной чечевицы содержится 18 г белка и 1 г жира.
Тест на белки
Тест Biuret Test для использования белков включает тестирование на наличие пептидной связи. Реагент биурета — это реагент на основе меди, который становится пурпурным при связывании с белком в щелочном растворе (рис. 1.17). Чем больше присутствует пептидных связей, тем больше интенсивность пурпурного цвета, что указывает на более высокую концентрацию белка.
Наличие белка также можно определить с помощью реагента Миллона .Реагент Миллона реагирует с аминокислотами тирозина, обычными для большинства белков, и приводит к образованию красновато-коричневого осадка при нагревании.
В таблице 1.5 ниже приведены основные тесты и их ожидаемые результаты в присутствии и в отсутствие белка.
Посмотрите видеодемонстрацию теста биурета на белок.
Видео: 2CMT
| Тестовый реагент | Положительный результат | Отрицательный результат |
| Биуретовый реагент | Фиолетовый / фиолетовый цвет | 902 902 902 902 902 красный коричневый цветбелый цвет |
Таблица 1.5: Наблюдаемые изменения цвета при тестировании на присутствие белка.
Тест на наличие белков
(Essential research-CAPS)ПРЕДУПРЕЖДЕНИЕ: реагент Миллона
Реагент Миллона очень ядовит. Его использование в классе не рекомендуется, если нет альтернативы или если учитель не уверен в его использовании. {\ circ} \) C)
- два с раствором альбумина (положительный контроль)
- два с сахарной водой (отрицательный контроль)
- пробирок с образцами для исследования на наличие белка
- пробирка с реагентом Миллона
- пробирка с раствором для биуретовой пробы
( ПРИМЕЧАНИЕ: Реагент Миллона и раствор Биурета в этом эксперименте должны быть приготовлены для вас вашим учителем).
Метод
Тест на белок с реактивом Миллона
ВНИМАНИЕ! Реагент Миллона очень токсичен! Избегайте вдыхания его паров.
- С помощью пипетки или пипетки добавьте несколько капель реагента Миллона в пробирку, содержащую альбумин.
- С помощью пипетки или пипетки добавьте несколько капель реагента Миллона в пробирку, содержащую сахарную воду.
- Используя пипетку или пипетку, добавьте несколько капель реагента Миллона в пробирку, содержащую образцы ваших продуктов, которые нужно протестировать.
- Нагрейте смеси в кипящей воде в течение 5 минут.
- Обратите внимание на любые изменения цвета.
Тест на белок с помощью теста Biuret
- С помощью капельницы или пипетки добавьте несколько капель раствора биурета в пробирку, содержащую альбумин.
- С помощью пипетки или пипетки добавьте несколько капель раствора Биурета в пробирку, содержащую сахарную воду.
- Используя пипетку или пипетку, добавьте несколько капель раствора Биурета в пробирку, содержащую образцы продуктов для тестирования.
- Обратите внимание на любые изменения цвета.
Рисунок 1.17: Биуретовый тест: это ожидаемое изменение цвета, если присутствует белок
Наблюдения
Запишите свои наблюдения, отмечая все ключевые различия между положительным контролем, отрицательным контролем и экспериментальными образцами
Наблюдения: Реагент Миллона
Белок приобретает кирпично-красный цвет и становится твердым. Красноватый цвет указывает на положительный результат теста на белок. Вода с сахаром не становится красной — она остается прозрачной, что свидетельствует об отсутствии белков.Любые образцы пищевых продуктов, которые становятся красновато-коричневыми при нагревании с реактивом Миллонса, также содержат белки.
Наблюдения: биуретовый тест
Белок становится фиолетовым, что указывает на присутствие белков. Вода с сахаром остается синего цвета добавленного сульфата меди — она не становится фиолетовой, что указывает на отсутствие белков. Любые образцы пищевых продуктов, которые становятся фиолетовыми при добавлении химикатов Biuret, содержат белок.
Посмотреть видео-демонстрацию эксперимента по тестированию белков:
Видео: 2CMV
Ферменты (ESG4F)
Ферменты — это белковые молекулы, которые помогают протекать химическим реакциям в живых организмах.Термин фермент имеет особое значение: фермент — это биологический катализатор, который ускоряет скорость химической реакции, но не используется в самой химической реакции. Разберем это определение подробнее.
Узнайте, что такое ферменты и как они работают.
Видео: 2CMW
Биологический : Ферменты — это белковые молекулы, состоящие из длинных цепочек аминокислот. Они складываются в уникальные трехмерные структуры с областью, известной как активный центр , где происходят реакции.
Катализатор : Ферменты ускоряют химические реакции, не расходясь сами по себе. Все химические реакции требуют определенного минимального количества энергии. Эта энергия известна как свободная энергия активации . Ферменты снижают энергию активации, тем самым ускоряя химические реакции (рис. 1.18).
Рис. 1.18: Ферменты снижают энергию активации, тем самым ускоряя протекание реакций.
Ферменты не расходуются в реакциях, которые они катализируют : они не изменяют равновесия реакций, поэтому они катализируют как прямые, так и обратные реакции.Направление, в котором протекает реакция, определяется концентрацией субстратов и продуктов реакции.
Ферменты могут участвовать в реакциях разрушения или наращивания молекул. Реакции разложения известны как катаболических реакций. Нарастающие реакции известны как анаболических реакций.
Модель действия фермента «замок и ключ»
Ферменты очень специфичны в отношении катализируемых ими реакций.Специфичность зависит от связей, образованных между активным центром фермента и его субстратом. Активные сайты имеют определенную форму, которая позволяет связывать очень специфический субстрат. Высокоспецифичный характер связывания фермента с субстратом сравнивают с «замком и ключом», где фермент выступает в качестве «замка», а субстрат — в качестве «ключа» (рис. 1.19). Субстрат связывает активный центр с образованием комплекса фермент-субстрат. Происходит реакция, затем продукт покидает активный центр, поскольку он больше не соответствует «замку» так же, как субстрат.Фермент остается неизменным.
Рис. 1.19: Эта диаграмма иллюстрирует «ключ-замок» модель действия фермента.
Исследование действия биологических стиральных порошков
(Essential research-CAPS)Цель
Для проверки работы ферментов в биологических стиральных порошках.
Аппарат
- два яйца всмятку (яйца, сваренные вкрутую, содержат денатурированные белки, не оставляющие пятен)
- два стакана
- биологический стиральный порошок (с ферментами)
- Небиологический стиральный порошок (старый тип стирального порошка)
- вода
- две мерные ложки
Метод
- Пометьте 3 стакана «Био», «Небио» и «Контроль», которые будут содержать биологический стиральный порошок, небиологический стиральный порошок и воду (отрицательный контроль) соответственно.
- В стакане с надписью «Био» растворите \ (\ text {5} \) \ (\ text {g} \) биологический стиральный порошок в \ (\ text {30} \) \ (\ text {ml} \) вода.
- В стакане с надписью «Non-Bio» растворите \ (\ text {5} \) \ (\ text {g} \) небиологический стиральный порошок в \ (\ text {30} \) \ (\ text { мл} \) воды.
- Налейте \ (\ text {30} \) \ (\ text {ml} \) водопроводной воды в контрольный стакан.
- Выньте небольшое количество яичного желтка.
- Поместите по чайной ложке с яичным желтком в каждый стакан.
- Оставьте ложки в мензурках на 1-2 часа.
- Наблюдайте за своими результатами.
Результаты
- Запишите свои наблюдения.
- Предложите причину ваших наблюдений.
- Напишите заключение на расследование.
Результаты
Яичный желток в биологическом стиральном порошке медленно растворяется с ложки. Яичный желток в небиологическом стиральном порошке частично поднимается с ложки, но не распадается и не растворяется в воде.В контрольном стакане изменений нет — желток остается на ложке.
Причины наблюдений
Ферменты биологического стирального порошка разбили яичный желток на более мелкие молекулы, которые отрываются от ложки и растворяются в воде. Этого не произошло ни с небиологическим порошком, ни с контролем.
Заключение
Биологические стиральные порошки лучше, чем небиологические стиральные порошки, удаляют органические пятна с одежды.
Ферменты в повседневной жизни
Свойства ферментов контролировать реакции широко используются в коммерческих целях. Примеры некоторых из этих применений перечислены ниже:
- Биологические стиральные порошки содержат ферменты, такие как липазы (расщепляет липиды) и протеазы (расщепляет белок), которые помогают разлагать пятна, вызванные продуктами питания, кровью, жиром или жиром. Эти биологические стиральные порошки экономят энергию, поскольку они эффективны при низких температурах.
- Размягчители для мяса содержат ферменты, полученные из таких фруктов, как папайя или ананас. Когда эти ферменты используются в мясных смягчителях, они смягчают мясо.
- Молоко без лактозы производится в первую очередь для людей с непереносимостью лактозы. У людей с непереносимостью лактозы отсутствует фермент лактаза, который переваривает лактозу (молочный сахар). Лактоза предварительно переваривается путем добавления в молоко лактазы.
Факторы, влияющие на действие ферментов
1.Температура
У человека ферменты лучше всего работают в \ (\ text {37} \) \ (\ text {° C} \) (рис. 1.20). Это оптимальная температура. При очень высоких температурах белки денатурируют ; это означает, что водородное, гидрофобное и электростатическое взаимодействия, которые приводят к трехмерной форме белка, разрушаются, превращая белок в его первичную структуру, длинную цепочку аминокислот. Когда белок денатурируется, изменяется форма его активного центра, а также остальная часть формы белка.Субстрат больше не может соответствовать активному центру фермента, и химические реакции не могут происходить. Низкие температуры могут замедлить или даже деактивировать ферменты, поскольку низкая температура означает меньшую доступную кинетическую энергию, так что даже более низкая энергия активации, которую допускает фермент, недоступна. Первый график показывает влияние температуры на активность фермента.
2. pH
Активность фермента чувствительна к pH. Ферменты имеют оптимальный pH, как показано на графике, но они могут эффективно функционировать в пределах диапазона pH.Эффективность фермента резко падает, когда pH выходит за пределы оптимального диапазона. Фермент может денатурироваться при воздействии pH за пределами диапазона pH, поскольку pH влияет на заряд некоторых аминокислот и, следовательно, влияет на электростатические взаимодействия, удерживающие вместе третичную структуру. Второй график показывает влияние pH на активность фермента.
Оптимальный pH и температура для фермента будут определяться видом живого существа, в котором он находится. Оптимальная температура ферментов в организме человека составляет 37 ° C.Бактерии, которые живут в компостных кучах, имеют ферменты с оптимальным диапазоном значений в 40, а бактерии, называемые гипертермофилами (любители очень высоких температур), которые живут в горячих источниках, имеют ферменты с оптимальными температурами выше 80 ° C.
Рис. 1.20: Графики, показывающие влияние температуры и pH на активность фермента соответственно.
В следующем исследовании будет изучено влияние температуры на активность фермента каталазы. Перекись водорода потенциально токсична, поэтому живые ткани содержат фермент каталаза, который расщепляет его на нетоксичные соединения, а именно воду и кислород.Вы изучите влияние фермента каталазы на расщепление перекиси водорода. Далее вы изучите влияние pH и температуры на активность ферментов.
Изучение влияния каталазы из куриной печени на перекись водорода
(Essential research-CAPS)Цель
Для демонстрации действия каталазы на перекись водорода.
Аппарат
- Мерные цилиндры 10 мл
- пипетка
- \ (\ text {3} \% \) Раствор перекиси водорода
- скальпель
- щипцы
- остаток
- куриная печень комнатной температуры
- Печень куриная отварная
- печень куриная замороженная
- стержень для перемешивания
Метод
Следуйте инструкциям ниже:
- Отрежьте два квадратных куска весом 0.1 г образца свежей печени и поместите каждый в отдельный мерный цилиндр на 10 мл.
- Используйте чистый мерный цилиндр для измерения 3 мл воды. Перелейте в один из цилиндров, содержащих свежую печень. Это ваш негативный контроль.
- Используйте чистый мерный цилиндр для измерения 3 мл перекиси водорода. Перелейте в оставшийся цилиндр, содержащий свежую печень. Это ваш положительный контроль.
- Подождите четыре минуты, а затем измерьте и запишите высоту образовавшихся пузырьков кислорода в каждом баллоне.
Вопросы
- Назовите три переменные, которые должны оставаться стабильными на протяжении этих экспериментов, и объясните, почему они должны оставаться стабильными.
- Какая реакция происходит?
- Как бы вы могли сделать этот эксперимент более точным?
- Какие еще факторы влияют на скорость реакции, кроме температуры?
Ответы
- Факторы остались прежними: [любые три из следующих]
- Используйте одинаковое количество куриной печени в каждом мерном цилиндре, чтобы контролировать количество присутствующего фермента.
- Используйте 3 мл воды и 3 мл перекиси водорода в двух разных цилиндрах, чтобы количество жидкости оставалось постоянным.
- Дайте двум цилиндрам одинаковое время для прохождения реакции, чтобы можно было надежно сравнить барботажные колонки.
- Содержимое обоих мерных цилиндров должно иметь одинаковую температуру, чтобы температура не мешала исследуемой реакции.
- Это катаболическая реакция / реакция разложения, поскольку перекись водорода распадается на кислород (пузырьки) и воду (оставшаяся жидкость).Реакция также является экзотермической, поскольку мерный цилиндр нагрелся — во время реакции выделялось тепло.
- Повышение точности:
- Заливайте жидкость в оба цилиндра одновременно.
- Более точно отмерьте количество куриной печени.
- Должна быть возможность вычислить объем кислорода, выделяемого при пропускании его через воду, и более точно рассчитать объем кислорода, используя принцип вытеснения. В существующем методе часть кислорода улетучивалась в воздух, когда пузырьки лопались, поэтому измерение высоты является приближением объема выделившегося кислорода.
- Другие факторы, влияющие на скорость реакции:
- Количество фермента в печени.
- Количество доступного субстрата.
- pH среды.
- Состояние куриной печени — если она не свежая, некоторые ферменты могут быть неактивными.
- Температура печени и жидкости.
Каковы наилучшие условия для фермента каталазы? Что происходит, когда фермент или живую ткань помещают в перекись водорода? Узнайте в этом видео.
Видео: 2CMX
Исследование влияния каталазы из куриной печени на перекись водорода — ЧАСТЬ B
Цель
Для демонстрации влияния температуры на активность каталазы.
Метод
- Добавьте 3 мл перекиси водорода в три отдельных градуированных мерных цилиндра на 10 мл. Пометьте один цилиндр «печень куриная замороженная»; второй — «вареная куриная печень» и третий — «куриная печень комнатной температуры».
- Вырежьте по 0,1 г квадрата из замороженной и вареной куриной печени комнатной температуры.Положите кусочки печени в мерный цилиндр с соответствующей маркировкой с перекисью водорода.
- Оставьте кусочки печени на четыре минуты и измерьте высоту образовавшихся пузырьков.
Вопросы
- Объясните причины различий, наблюдаемых для трех измерительных цилиндров.
- Назовите зависимые и независимые переменные в этом эксперименте.
- Как бы вы могли сделать этот эксперимент более точным?
- Какие выводы вы сделаете из своих наблюдений?
Ответы
- Печень при комнатной температуре реагирует очень быстро и производит большое количество больших пенистых белых пузырьков, потому что ферменты очень активны — они близки к своей оптимальной температуре и легко расщепляют перекись водорода на воду и кислород.Замороженная печень сначала реагирует очень медленно и образует очень мало пузырьков, поскольку ферменты неактивны при таких низких температурах — им не хватает энергии активации. Когда реакция выделяет тепло, фермент немного позже ускоряется и образует более крупные пузырьки с большей скоростью, но никогда не так быстро, как при комнатной температуре. Вареная печень не проявляет никакой реакции — пузырьки не образуются, потому что ферменты денатурировались при кипячении. Их форма изменилась, и они вообще не могут катализировать реакцию.
- Зависимой переменной является скорость реакции, то есть количество образовавшегося кислорода, которое было измерено как высота барботажной колонны.
- Независимая переменная — температура — печень была комнатной температуры или была замороженной или вареной.
- Более точно измерьте количество печени и объем перекиси водорода и держите их одинаковыми.
- Убедитесь, что все 3 мерных цилиндра идентичны — одинаковой ширины.
- Залейте перекись водорода в баллоны одновременно.
- Улавливайте количество выделившегося кислорода и используйте принцип вытеснения для более точного расчета объема газа.
- Температура влияет на активность ферментов. Ферменты наиболее активны при температуре, близкой к их оптимальным температурам, но они денатурируют и не могут функционировать, если температура слишком высока. При очень низких температурах ферменты не могут эффективно функционировать из-за недостатка энергии активации — они работают очень медленно.
Нуклеиновые кислоты (ESG4G)
Нуклеиновые кислоты, такие как ДНК и РНК, представляют собой большие органические молекулы, которые являются ключевыми для всех живых организмов. Строительные блоки нуклеиновых кислот называются нуклеотидами . Каждый нуклеотид состоит из сахара, фосфата и азотистого основания. Нуклеотиды соединены фосфодиэфирными связями , которые соединяют фосфат одного нуклеотида с сахаром другого. Нити фосфат-сахар-фосфат-сахар образуют «основу», на которой выставлены азотсодержащие основания.Следовательно, нуклеиновые кислоты представляют собой полимеров , состоящих из множества нуклеотидов. ДНК представляет собой двухцепочечный полимер из-за образования водородных связей между азотистыми основаниями двух комплементарных цепей. РНК — одноцепочечный полимер. Нуклеиновые кислоты не нужно получать с пищей, потому что они синтезируются с использованием промежуточных продуктов метаболизма углеводов и аминокислот.
Нуклеиновые кислоты включают:
- Дезоксирибонуклеиновая кислота ( ДНК ): содержит «инструкции» по синтезу белков в форме генов.ДНК находится в ядре каждой клетки, а также в меньших количествах присутствует в митохондриях и хлоропластах.
- Рибонуклеиновая кислота ( РНК ): важна для передачи генетической информации от ДНК для образования белков. Он находится на рибосомах, в цитоплазме и ядре.
также можно найти внутри хлоропластов и митохондрий.
Рисунок 1.21: Схематическая диаграмма ДНК и РНК: ДНК двухцепочечная, а РНК одноцепочечная.
Структура и функция ядра будут подробно объяснены в следующей главе: Основные единицы жизни .
Химические тесты для идентификации биомолекул
Основные химические компоненты клеток можно разделить на четыре основные категории — углеводы, белки, липиды и нуклеиновые кислоты. Другие химические вещества, такие как вода, соли и минералы, также присутствуют и жизненно важны для живых клеток. Ниже описаны характерные тесты для идентификации каждого из четырех основных классов биологических молекул.
Тест на сложные углеводы (полисахариды)Углеводы, такие как крахмал, обнаруживаются путем смешивания образца с 2–4 каплями йода или раствора Люголя. Если в растворе присутствует крахмал, цвет раствора изменится от желто-коричневого до темно-фиолетового. Изменение цвета происходит из-за химической реакции между большой молекулой углеводов и ионами йода. Считается, что заряженные ионы йода притягиваются к небольшим зарядам на молекулах крахмала (полисахарида), и это вызывает наблюдаемое нами изменение цвета.
Результаты йодной пробы: положительный результат — пробирка слева, отрицательный результат — пробирка справа
Тест на (уменьшение) простых сахаров (моносахаридов)
Наличие более мелких углеводов, таких как глюкоза, может можно определить с помощью решения Бенедикта. В растворе Бенедикта есть ионы меди (Cu 2+ ), которые имеют голубой цвет. Когда этот раствор нагревают в присутствии сахаров, таких как глюкоза, ионы меди изменяются и меняют цвет от светло-зеленого до ржавого оранжево-коричневого.
Тест на белки
Присутствие белков можно определить путем смешивания раствора с биуретовым тестовым раствором (или реагентом). Тестовый раствор биурета представляет собой смесь ионов меди (Cu 2+ ), гидроксида натрия (NaOH) и тартрата калия-натрия (KNaC 4 H 4 O 6 ). Если присутствуют белки, между ионами меди и молекулами белка происходит химическая реакция. В результате химической реакции раствор биурета меняет цвет с голубого на пурпурный, если присутствуют белки.
Тест на липиды
Присутствие липидов можно определить с помощью индикатора Судан III. Индикаторы Судана — это окрашенные жиролюбивые молекулы. При тестировании раствора на липиды вы получаете два результата: следует искать:
1. Получается ли расслоение слоев (вода & lipid) ?,
и
2. Мигрирует ли краситель к одному из слоев?
Если все смеси растворимы в воде (липиды отсутствуют), то Судан IV образует мелкие мицеллы / капли и рассеиваются по всему раствору.При положительном результате липидный слой находится поверх водного слоя, а липидный слой будет иметь красно-оранжевый цвет
Тест на нуклеиновые кислоты
Тест на дифениламин (Dische) используется для определения присутствия нуклеиновые кислоты. Наличие ДНК сделает прозрачный раствор синим. Чем больше ДНК присутствует, тем темнее цвет. Другая нуклеиновая кислота, РНК, станет зеленой.
Мониторинг молекулярного состава живых клеток, подвергшихся воздействию электрических импульсов, с помощью оптических методов без меток
Культура клеток
Для этого исследования были использованы два разных типа клеток.Клетки MDCK использовали в случае THz-ATR, тогда как клетки haMSC использовали в случае комбинационного рассеяния. Проницаемость обеих клеточных линий также исследовали с помощью флуоресцентной микроскопии. Выбор клеточных линий был основан на нашей предыдущей опубликованной работе с клетками MDCK для терагерцовых экспериментов 31 и haMSC для экспериментов комбинационного рассеяния 21 . Выбор этих клеток был продиктован, чтобы упростить сравнение с нашими предыдущими исследованиями. Ни в коем случае выбор клеток не был продиктован из-за особой чувствительности клеток к той или иной технологии, исследованной во время работы, о которой здесь сообщается.Оба типа клеток выращивали в увлажненной атмосфере при 37 ° C и 5% CO. 2 в среде Игла, модифицированной Дульбекко (DMEM), с добавлением 10% сыворотки (фетальная телячья сыворотка для MDCK и фетальная бычья сыворотка для haMSC) и 1% пенициллина. –Стрептомицин (Life Technologies).
Для терагерцовых экспериментов MDCK наносили с плотностью 30 000 ячеек / см 2 на окно из высокоомного кремния (HR-Si) диаметром 3 мм и диаметром 37 мм, которое является оптимальной подложкой для терагерцовых экспериментов в геометрия ослабленного полного внутреннего отражения 30,31 и помещена в чашку Петри диаметром 60 мм.Клетки выращивали от 3 до 5 дней до полного слияния. Затем часть ячеек удаляли, царапая их на одной половине окна HR-Si, которое использовалось в качестве эталона. Перед экспериментами культуральную среду заменяли 2 мл забуференной минимальной среды (HBSS с 10 мМ буфером HEPES, без Ca 2+ ). Терагерцовые эксперименты проводились при комнатной температуре (21 ° C), где было подтверждено, что терагерцовый сигнал стабилен в течение более 4 часов в контрольных экспериментах без µsPEF.
Из-за непрозрачности для видимого света носителей HR-Si, что делает их несовместимыми со стандартной микроскопией, для экспериментов по флуоресценции, используемых для сравнения с экспериментами в терагерцовом диапазоне, клетки готовили точно в тех же условиях, но выращивали в стандартные чашки Петри 35 мм. Никаких различий в морфологии или пролиферации клеток между культурой на окнах HR-Si и чашках Петри замечено не было. Эти эксперименты с флуоресцентной микроскопией также проводили при комнатной температуре (21 ° C).
Для рамановских экспериментов клетки haMSCs высевали с плотностью 5000 клеток / см 2 на подложку из CaF 2 (Crystran, Poole), помещенную на дно чашки Петри диаметром 35 мм. Клетки выращивали в течение ночи. Перед рамановскими экспериментами среду заменяли 2 мл физиологического раствора, NaCl 154 мМ (Б. Браун). Этот физиологический раствор обычно используется для получения CRMS на живых клетках 34 . Из-за большой продолжительности регистрации комбинационного рассеяния, они были выполнены при 4 ° C, чтобы избежать влияния эффектов процесса повторного запечатывания мембраны 22 .Для сравнения флуоресцентных экспериментов с рамановскими экспериментами клетки выращивали точно в тех же условиях, а записи выполняли при комнатной температуре (21 ° C).
Генератор импульсов и условия импульсов
Коммерчески доступный генератор электрических импульсов (Cliniporator ™, IGEA, Италия) использовался для обработки клеток 8 импульсами по 100 мкс, подаваемыми с частотой повторения 1 Гц. Величина электрического поля составляла 500, 750, 1000, 1250 или 1500 В / см в зависимости от эксперимента.Для подачи электрических импульсов на присоединенные ячейки в различных системах визуализации использовалась самодельная система электродов на основе двух параллельных пластинчатых электродов из нержавеющей стали, разделенных фиксированным расстоянием 4 мм или 8 мм для рамановских и терагерцовых экспериментов соответственно. Расстояние между электродами 8 мм было выбрано таким образом, чтобы исключить возмущение светового пятна диаметром 2,5 мм луча ТГц-НПВО. Поскольку максимальное выходное напряжение генератора импульсов составляло 1000 В, расстояние в 8 мм между пластинчатыми электродами ограничивало максимальную величину подаваемого электрического поля до 1250 В / см.Поэтому величина электрического поля 1500 В / см использовалась только для рамановских экспериментов. Клинипоратор был соединен с пластинчатыми электродами зажимами из крокодиловой кожи. Подача электрических импульсов осуществлялась при 4 ° C для рамановских экспериментов и при комнатной температуре (21 ° C) для остальных экспериментов (флуоресценция и терагерц). Как упоминалось в нашей предыдущей работе, после доставки µsPEF 21 не было замечено никакого эффекта нагрева, изменения pH или образования пузырьков.
CRMS и обработка спектров
Рамановские эксперименты проводились в экспериментальных условиях, подробно описанных в Azan et al. . 21 . Вкратце, конфокальный рамановский микроспектрометр LabRam ARAMIS (Horiba Jobin Yvon) с лазером непрерывного излучения 532 нм был использован для получения рамановских спектров живых клеток haMSC. Мощность образца составляла около 20 мВт, что, как известно, не токсично для клеток 35,36,37 . Перед любым измерением конфокальный рамановский микроспектрометр был откалиброван с образцом кремния с использованием полосы 520 см -1 и проверена мощность лазера. Рамановские подписи были получены в области отпечатков пальцев (600–1800 см, -1 ).Время сбора данных было зафиксировано на двух накоплениях по 30 с (всего 60 с). Образец помещали на пьезоэлектрический столик XY для исследования нескольких мест. Во время рамановских измерений клетки поддерживали при 4 ° C с помощью регулятора температуры T95 (Linkam Scientific Instrument Ltd). Рамановская сигнатура физиологического раствора была получена для того, чтобы иметь возможность удалить этот фоновый сигнал из измеренных спектров. Всего было собрано 264 рамановских спектра.
Измеренные спектры комбинационного рассеяния были предварительно обработаны, как подробно описано в Azan et al. . 21 . Вкратце, проверка качества выполнялась для каждого отдельного собранного спектра комбинационного рассеяния, что означает, что измеренные спектры с отношением сигнал / шум (SNR) ниже 10 были исключены из набора данных. Затем спектры сглаживали с использованием фильтра Савицки-Голея (12 точек, полином 2-го порядка) и удаляли базовые линии и фоновые сигналы физиологического раствора. Наконец, спектры были нормализованы с использованием метода стандартной нормальной дисперсии (SNV). Были рассчитаны средние нормированные спектры для каждого состояния электрического импульса.Также рассчитывалась разница между средними нормализованными спектрами при определенных условиях электрических импульсов и средними нормализованными спектрами контроля (ложное воздействие, 0 В / см). Многовариантный анализ, основанный на методе частичных наименьших квадратов (PLS), был проведен на комбинированном наборе данных с централизованным средним значением. Величина электрического поля использовалась в качестве наблюдаемой переменной для анализа PLS. Показатели латентной переменной 1 (LV1), полученные в результате анализа, были использованы при последующей обработке данных.
Терагерцовое полное отражение и специальная обработка данных
Терагерцовый сигнал был сгенерирован и обнаружен с помощью классической терагерцовой спектроскопии во временной области (THz-TDS) 30 .Эта установка генерирует почти линейно поляризованный суб-одноцикловый терагерцовый импульс с центром около 0,5 ТГц и расширением до 2 ТГц. В качестве сигнала выбрана максимальная амплитуда терагерцового импульса, поскольку она демонстрирует наиболее сильную модификацию между ячейками и свободной поверхностью пятна. Кроме того, устройство с терагерцовым ослаблением полного отражения (THz-ATR) представляет собой полностью терагерцовую равнобедренную призму HR-Si (R> 10 кОм см, n = 3,42) с углом основания 42 °. Этот угол падения обеспечивает условия полного внутреннего отражения.Для визуализации клеток кремниевая призма была закрыта окном HR-Si толщиной 3 мм, на котором клетки были ранее выращены. Дополнительная кольцевая крышка позволяла удерживать клетки в их буферной среде и очень точно перемещать субстрат. В таких условиях слой ячеек зондировался исчезающей волной с продольной протяженностью около 20 мкм, генерируемой на поверхности окна HR-Si 30 . Смещение опоры позволяло получать изображения пиксель за пикселем с поперечным разрешением 2.5 мм. Сборы были сделаны с силиконовым пластырем, наполовину покрытым клеточным слоем, и наполовину свободным от клеток в качестве эталона, все купание в клеточной среде. Для кинетических изменений, наблюдаемых после подачи электрических импульсов, о которых сообщается в этой статье, сигналы трех пикселей в области слоя ячеек и двух в эталонной области были получены вдоль линии примерно за 15 с, чтобы получить значение относительного сигнала THz-ATR. . Этот сигнал был нормализован по его значению до подачи электрических импульсов, чтобы получить нормализованный относительный сигнал THz-ATR, Δ THz в процентах.Без каких-либо возмущений сигнал THz-ATR был стабильным в течение нескольких часов при комнатной температуре (21 ° C). Указанный относительный сигнал THz-ATR регистрировался каждые 30 с в течение 40 минут после подачи электрических импульсов, оптимизированный в соответствии с настройкой ATR-THz и динамикой сигнала. Вариации регистрируемых терагерцовых сигналов от клетки к эталонным областям происходят из-за изменений цитозольных концентраций молекул. Точнее, относительная разница сигналов THz-ATR между клетками и их внешней средой пропорциональна массовой концентрации всех внутриклеточных молекул, от ионов и метаболитов до белков 31,38 (см. Также дополнительную информацию).Это приводит к относительной разнице около 8%. Мы также проверили влияние терагерцового излучения на жизнеспособность клеток, поместив клетки обратно в культуру после воздействия терагерцового излучения в отсутствие доставки µsPEF: в течение следующих 24 часов клетки росли нормально.
Флуоресцентная микроскопия (включая предварительную обработку и обработку данных)
Во всех экспериментах по флуоресценции использовали Hoechst 33,342 для окрашивания ядра клетки с целью локализации всех клеток, проницаемых или нет.YO-PRO-1 использовали в качестве классического флуоресцентного маркера электропермеабилизации клеток 32 . Перед экспериментами по флуоресценции клетки окрашивали в присутствии 370 нМ Hoechst 33,342 в течение 30 минут при 37 ° C и 5% CO 2 . После двух промывок фосфатно-солевым буфером (PBS) к клеткам добавляли YO-PRO-1 в конечной концентрации 1 мкМ. Те же самые буферы и остальные конкретные экспериментальные условия (подложки, электроды, объем буфера и т. Д.), Использованные соответственно для рамановских и терагерцовых экспериментов, также использовались в экспериментах по флуоресценции и проводились при комнатной температуре.Флуоресцентные и светлопольные изображения получали с помощью инвертированного микроскопа Observer Z1 (Zeiss). Изображения были получены с фиксированным временем экспозиции 300 мс как для зеленого (YO-PRO-1; λ ex = 475 нм, λ em = 530 нм), так и для синего (Hoechst 33,342; λ ex = 365 нм, λ em = 445 нм) и 40 мс для канала светлого поля. Микроскоп управлялся программой Zen Blue 2 Zeiss.
В случае сравнения модальностей флуоресценции и комбинационного рассеяния изображения были получены через 10 мин после подачи электрических импульсов.Впоследствии интенсивность флуоресценции YO-PRO-1 (I Fluo ) была автоматически извлечена из местоположения ядра клетки, помеченного красителем Hoechst 33,342.
В случае сравнения методов флуоресценции и THz-ATR, двухканальные флуоресцентные изображения получали каждые 20 с в течение не менее 20 минут, оптимизированные в соответствии с настройкой и динамикой сигнала. Перед подачей электрических импульсов было получено 4 изображения. Единственное различие между экспериментами THz-ATR и экспериментами с покадровой флуоресценцией заключалось в субстрате: HR-Si, используемый для экспериментов THz-ATR, был заменен стандартной чашкой Петри для культивирования клеток для экспериментов по флуоресценции.Разница диэлектрической проницаемости кремния (11,7) и пластика (2,2) не влияет на распределение электрического поля, создаваемого электродами, поскольку среда ячейки является проводящей. Все остальные параметры эксперимента или процессы подготовки образцов оставались неизменными. В конце экспериментов по флуоресценции изменений морфологии клеток замечено не было. Кроме того, клетки росли нормально, если их возвращали в культуру, что свидетельствует об отсутствии фототоксичности. В этих экспериментальных условиях мы также проверили отсутствие фотообесцвечивания YO-PRO-1 и Hoechst 33,342.В каждом изображении флуоресценции мы выбрали 5 областей интереса (ROI), включая клетки, и усреднили сигналы флуоресценции по этим областям интереса, чтобы получить общий сигнал флуоресценции YO-PRO-1 клеток \ (F_ {cell} \). Также мы выбрали фоновый ROI без ячейки для эталонного сигнала YO-PRO-1 \ (F_ {ref} \). Чтобы компенсировать временные изменения лампы, используемой при измерениях флуоресценции, мы вычислили нормализованное отношение \ (S_ {fluo} = F_ {cell} / F_ {ref} \). Два сигнала флуоресценции, линейно изменяющиеся с интенсивностью лампы, \ (S_ {fluo} \) затем не зависели от интенсивности.Однако это может привести к большему ненужному колебанию отношения, когда \ (F_ {ref} \) очень низкое, по сравнению с методом, использующим разницу \ (F_ {cell} — F_ {ref} \). К счастью, в наших измерениях это не так, поскольку \ (F_ {ref} \) намного выше шума обнаружения камеры. Метод нормализации отношения дал лучший результат, сильно ограничив влияние флуктуации мощности света на количественную оценку интенсивности флуоресценции, не создавая дополнительных флуктуаций.Наконец, относительный сигнал флуоресценции \ (I_ {Fluo} \ left (t \ right) \) был рассчитан как относительное изменение между \ (S_ {fluo} \ left (t \ right) \) после подачи электрических импульсов. и \ (S_ {fluo} \) (t <0) перед доставкой, как
$$ I_ {Fluo} \ left (t \ right) = \ frac {{S_ {Fluo} \ left (t \ right) — S_ {Fluo} \ left ({t <0} \ right)}} {{S_ {Fluo} \ left ({t <0} \ right)}}.
$Обработка данных для сравнения различных приборов
Для того, чтобы выполнить количественное и качественное сравнение между различными модальностями (комбинация комбинационного рассеяния против флуоресценции и терагерцового диапазона против флуоресценции), были определены различные параметры.Нормированный относительный сигнал комбинационного рассеяния Δ Raman и нормализованный сигнал флуоресценции Δ Fluo использовали для сравнения модальностей комбинационного рассеяния и флуоресценции. Аналогичным образом, изменение во времени нормализованного относительного сигнала THz-ATR Δ THz (t) и изменение во времени нормализованного сигнала относительной флуоресценции Δ Fluo (t) использовали для сравнения THz-ATR с модальностью флуоресценции. Эти параметры определялись следующими уравнениями:
$$ \ Delta_ {Raman} = \ frac {{I_ {Raman} — {<} I_ {Raman \; Control} {>}}} {{{<} I_ {Raman \; Control} {>}}} $$
где I Raman был баллом LV1, а Raman Control > был средним баллом LV1 контрольной группы (0 В / см),
$$ \ Delta_ {Fluo} = \ frac {{I_ {Fluo } — {<} I_ {Fluo \; Control} {>}}} {{{<} I_ {Fluo \; Control} {>}}} $$
где I Fluo — это нормализованная интенсивность флуоресценции YO-PRO-1 на клетку, а Fluo Control > — средняя нормализованная интенсивность флуоресценции YO-PRO-1 контрольной группы (0 В / см), а
$$ \ Delta_ {THz} \ left (t \ right) = \ frac {{S_ {THz} \ left (t \ right)}} {{S_ {THz} (t <0)}} $$
где
$$ S_ {THz} \ left (t \ right) = \ frac {{E_ {THz} \ left ({{\ text {cell}}} \ right) — E_ {THz} \ left ({{ \ text {buffer}}} \ right)}} {{E_ {THz} \ left ({{\ text {buffer}}} \ right)}} $$
и где \ (E_ {THz} \) — пиковая амплитуда отраженного сигнала THz-ATR от устройства ATR.{{- \ frac {t} {{\ tau_ {THz}}}}}} \ right) $$
где C THz и τ THz были связаны со значением плато THz-ATR и постоянной времени THz-ATR, соответственно. C Fluo и τ Fluo сравнивали соответственно с C THz и τ THz , чтобы выполнить количественное и качественное сравнение между модальностями флуоресценции и THz-ATR.
2.3 Биологические молекулы — Концепции биологии — 1-е канадское издание
К концу этого раздела вы сможете:
- Опишите, почему углерод имеет решающее значение для жизни
- Объясните влияние незначительных изменений аминокислот на организмы
- Опишите четыре основных типа биологических молекул
- Понимать функции четырех основных типов молекул
Посмотрите видео о белках и белковых ферментах.
Большие молекулы, необходимые для жизни, которые состоят из более мелких органических молекул, называются биологическими макромолекулами . Существует четыре основных класса биологических макромолекул (углеводы, липиды, белки и нуклеиновые кислоты), каждый из которых является важным компонентом клетки и выполняет широкий спектр функций. Вместе эти молекулы составляют большую часть массы клетки. Биологические макромолекулы являются органическими, что означает, что они содержат углерод. Кроме того, они могут содержать водород, кислород, азот, фосфор, серу и дополнительные второстепенные элементы.
Часто говорят, что жизнь «основана на углероде». Это означает, что атомы углерода, связанные с другими атомами углерода или другими элементами, образуют фундаментальные компоненты многих, если не большинства, молекул, уникальных для живых существ. Другие элементы играют важную роль в биологических молекулах, но углерод определенно квалифицируется как элемент «фундамент» для молекул в живых существах. Это связывающие свойства атомов углерода, которые ответственны за его важную роль.
Углерод содержит четыре электрона в своей внешней оболочке.Следовательно, он может образовывать четыре ковалентные связи с другими атомами или молекулами. Простейшая молекула органического углерода — метан (CH 4 ), в котором четыре атома водорода связаны с атомом углерода.
Рис. 2.12. Углерод может образовывать четыре ковалентные связи, образуя органическую молекулу. Самая простая молекула углерода — это метан (Ch5), изображенный здесь.Однако более сложные конструкции изготавливаются с использованием углерода. Любой из атомов водорода можно заменить другим атомом углерода, ковалентно связанным с первым атомом углерода.Таким образом могут быть образованы длинные и разветвленные цепи углеродных соединений (рис. 2.13 a ). Атомы углерода могут связываться с атомами других элементов, таких как азот, кислород и фосфор (рис. 2.13 b ). Молекулы также могут образовывать кольца, которые сами могут связываться с другими кольцами (рис. 2.13 c ). Это разнообразие молекулярных форм объясняет разнообразие функций биологических макромолекул и в значительной степени основано на способности углерода образовывать множественные связи с самим собой и другими атомами.
Рис. 2.13. Эти примеры показывают три молекулы (обнаруженные в живых организмах), которые содержат атомы углерода, различным образом связанные с другими атомами углерода и атомами других элементов. (а) Эта молекула стеариновой кислоты имеет длинную цепочку атомов углерода. (б) Глицин, компонент белков, содержит атомы углерода, азота, кислорода и водорода. (c) Глюкоза, сахар, имеет кольцо из атомов углерода и один атом кислорода.Углеводы — это макромолекулы, с которыми большинство потребителей в некоторой степени знакомо.Чтобы похудеть, некоторые люди придерживаются «низкоуглеводной» диеты. Спортсмены, напротив, часто «нагружаются углеводами» перед важными соревнованиями, чтобы убедиться, что у них достаточно энергии для соревнований на высоком уровне. Фактически, углеводы являются неотъемлемой частью нашего рациона; злаки, фрукты и овощи — все это естественные источники углеводов. Углеводы обеспечивают организм энергией, особенно через глюкозу, простой сахар. Углеводы также выполняют другие важные функции у людей, животных и растений.
Углеводы можно представить формулой (CH 2 O) n , где n — количество атомов углерода в молекуле. Другими словами, соотношение углерода, водорода и кислорода в молекулах углеводов составляет 1: 2: 1. Углеводы подразделяются на три подтипа: моносахариды, дисахариды и полисахариды.
Моносахариды (моно- = «один»; sacchar- = «сладкий») представляют собой простые сахара, наиболее распространенным из которых является глюкоза.В моносахаридах количество атомов углерода обычно составляет от трех до шести. Большинство названий моносахаридов оканчиваются суффиксом -ose. В зависимости от количества атомов углерода в сахаре они могут быть известны как триозы (три атома углерода), пентозы (пять атомов углерода) и гексозы (шесть атомов углерода).
Моносахариды могут существовать в виде линейной цепи или кольцевых молекул; в водных растворах они обычно находятся в кольцевой форме.
Химическая формула глюкозы: C 6 H 12 O 6 .У большинства живых существ глюкоза является важным источником энергии. Во время клеточного дыхания из глюкозы выделяется энергия, которая используется для выработки аденозинтрифосфата (АТФ). Растения синтезируют глюкозу, используя углекислый газ и воду в процессе фотосинтеза, а глюкоза, в свою очередь, используется для удовлетворения потребностей растений в энергии. Избыток синтезированной глюкозы часто хранится в виде крахмала, который расщепляется другими организмами, которые питаются растениями.
Галактоза (входит в состав лактозы или молочного сахара) и фруктоза (содержится во фруктах) — другие распространенные моносахариды.Хотя глюкоза, галактоза и фруктоза имеют одинаковую химическую формулу (C 6 H 12 O 6 ), они различаются структурно и химически (и известны как изомеры) из-за разного расположения атомов в углеродной цепи. .
Рис. 2.14. Глюкоза, галактоза и фруктоза — изомерные моносахариды, что означает, что они имеют одинаковую химическую формулу, но немного разные структуры.Дисахариды (ди- = «два») образуются, когда два моносахарида подвергаются реакции дегидратации (реакции, при которой происходит удаление молекулы воды).Во время этого процесса гидроксильная группа (–ОН) одного моносахарида соединяется с атомом водорода другого моносахарида, высвобождая молекулу воды (H 2 O) и образуя ковалентную связь между атомами в двух молекулах сахара.
Общие дисахариды включают лактозу, мальтозу и сахарозу. Лактоза — это дисахарид, состоящий из мономеров глюкозы и галактозы. Он содержится в молоке. Мальтоза, или солодовый сахар, представляет собой дисахарид, образующийся в результате реакции дегидратации между двумя молекулами глюкозы.Наиболее распространенным дисахаридом является сахароза или столовый сахар, который состоит из мономеров глюкозы и фруктозы.
Длинная цепь моносахаридов, связанных ковалентными связями, известна как полисахарид (поли- = «много»). Цепь может быть разветвленной или неразветвленной, и она может содержать разные типы моносахаридов. Полисахариды могут быть очень большими молекулами. Крахмал, гликоген, целлюлоза и хитин являются примерами полисахаридов.
Крахмал — это хранимая в растениях форма сахаров, состоящая из амилозы и амилопектина (оба полимера глюкозы).Растения способны синтезировать глюкозу, а избыток глюкозы откладывается в виде крахмала в различных частях растений, включая корни и семена. Крахмал, который потребляется животными, расщепляется на более мелкие молекулы, такие как глюкоза. Затем клетки могут поглощать глюкозу.
Гликоген — это форма хранения глюкозы у людей и других позвоночных, состоящая из мономеров глюкозы. Гликоген является животным эквивалентом крахмала и представляет собой сильно разветвленную молекулу, обычно хранящуюся в клетках печени и мышц.Когда уровень глюкозы снижается, гликоген расщепляется с высвобождением глюкозы.
Целлюлоза — один из самых распространенных природных биополимеров. Клеточные стенки растений в основном состоят из целлюлозы, которая обеспечивает структурную поддержку клетки. Дерево и бумага в основном целлюлозные по своей природе. Целлюлоза состоит из мономеров глюкозы, которые связаны связями между определенными атомами углерода в молекуле глюкозы.
Каждый второй мономер глюкозы в целлюлозе переворачивается и плотно упаковывается в виде вытянутых длинных цепей.Это придает целлюлозе жесткость и высокую прочность на разрыв, что так важно для растительных клеток. Целлюлоза, проходящая через нашу пищеварительную систему, называется пищевыми волокнами. Хотя связи глюкозы и глюкозы в целлюлозе не могут быть разрушены пищеварительными ферментами человека, травоядные животные, такие как коровы, буйволы и лошади, способны переваривать траву, богатую целлюлозой, и использовать ее в качестве источника пищи. У этих животных определенные виды бактерий обитают в рубце (часть пищеварительной системы травоядных) и секретируют фермент целлюлазу.В аппендиксе также содержатся бактерии, которые расщепляют целлюлозу, что придает ей важную роль в пищеварительной системе жвачных животных. Целлюлазы могут расщеплять целлюлозу на мономеры глюкозы, которые могут использоваться животным в качестве источника энергии.
Углеводы выполняют другие функции у разных животных. У членистоногих, таких как насекомые, пауки и крабы, есть внешний скелет, называемый экзоскелетом, который защищает их внутренние части тела. Этот экзоскелет состоит из биологической макромолекулы , хитина , азотистого углевода.Он состоит из повторяющихся единиц модифицированного сахара, содержащего азот.
Таким образом, из-за различий в молекулярной структуре углеводы могут выполнять самые разные функции хранения энергии (крахмал и гликоген), а также структурной поддержки и защиты (целлюлоза и хитин).
Рис. 2.15. Хотя их структура и функции различаются, все полисахаридные углеводы состоят из моносахаридов и имеют химическую формулу (Ch3O) n.Зарегистрированный диетолог: ожирение является проблемой для здоровья во всем мире, и многие болезни, такие как диабет и болезни сердца, становятся все более распространенными из-за ожирения.Это одна из причин, почему к зарегистрированным диетологам все чаще обращаются за советом. Зарегистрированные диетологи помогают планировать пищевые продукты и программы питания для людей в различных условиях. Они часто работают с пациентами в медицинских учреждениях, разрабатывая планы питания для профилактики и лечения заболеваний. Например, диетологи могут научить пациента с диабетом, как контролировать уровень сахара в крови, употребляя в пищу правильные типы и количества углеводов. Диетологи также могут работать в домах престарелых, школах и частных клиниках.
Чтобы стать дипломированным диетологом, нужно получить как минимум степень бакалавра в области диетологии, питания, пищевых технологий или в смежных областях. Кроме того, дипломированные диетологи должны пройти программу стажировки под руководством и сдать национальный экзамен. Те, кто занимается диетологией, проходят курсы по питанию, химии, биохимии, биологии, микробиологии и физиологии человека. Диетологи должны стать экспертами в химии и функциях пищи (белков, углеводов и жиров).
Через призму коренных народов (Сюзанна Вилкерсон и Чарльз Мольнар)
Я работаю в колледже Камосун, расположенном в красивой Виктории, Британская Колумбия, с кампусами на традиционных территориях народов леквунгенов и васаней. Подземная луковица для хранения цветка камас, показанная ниже, была важным источником пищи для многих коренных народов острова Ванкувер и всей западной части Северной Америки. Луковицы камас по-прежнему употребляются в пищу как традиционный источник пищи, и приготовление луковиц камас относится к этому текстовому разделу об углеводах.
Рисунок 2.16 Изображение синего цветка камас и насекомого-опылителя. Подземная лампочка камаса запекается в костре. Тепло действует как фермент панкреатическая амилаза и расщепляет длинные цепи неперевариваемого инулина на усвояемые моно- и дисахариды.Чаще всего растения вырабатывают крахмал как запасенную форму углеводов. Некоторые растения, например камас, создают инулин. Инулин используется в качестве пищевых волокон, однако он не усваивается людьми. Если бы вы откусили сырую луковицу камаса, она была бы горькой и имела липкую консистенцию.Метод, используемый коренными народами для того, чтобы сделать камас одновременно удобоваримым и вкусным, заключается в медленном запекании луковиц в течение длительного периода в подземной чаше для костра, покрытой особыми листьями и почвой. Тепло действует как фермент амилаза поджелудочной железы и расщепляет длинные цепи инулина на легкоусвояемые моно- и дисахариды.
Правильно запеченные луковицы камас по вкусу напоминают сочетание печеной груши и вареного инжира. Важно отметить, что, хотя синие камы являются источником пищи, их не следует путать с белыми камасами смерти, которые особенно токсичны и смертельны.Цветки выглядят по-разному, но луковицы очень похожи.
Липиды включают разнообразную группу соединений, объединенных общим признаком. Липиды являются гидрофобными («водобоязненными») или нерастворимыми в воде, поскольку они являются неполярными молекулами. Это потому, что они являются углеводородами, которые включают только неполярные углерод-углеродные или углерод-водородные связи. Липиды выполняют в клетке множество различных функций. Клетки хранят энергию для длительного использования в виде липидов, называемых , жиров .Липиды также обеспечивают изоляцию растений и животных от окружающей среды. Например, они помогают водным птицам и млекопитающим оставаться сухими из-за их водоотталкивающих свойств. Липиды также являются строительными блоками многих гормонов и являются важной составляющей плазматической мембраны. Липиды включают жиры, масла, воски, фосфолипиды и стероиды.
Рис. 2.17. Гидрофобные липиды в мехе водных млекопитающих, таких как речная выдра, защищают их от непогоды.Молекула жира, такая как триглицерид, состоит из двух основных компонентов — глицерина и жирных кислот.Глицерин — это органическое соединение с тремя атомами углерода, пятью атомами водорода и тремя гидроксильными (–OH) группами. Жирные кислоты имеют длинную цепь углеводородов, к которой присоединена кислая карбоксильная группа, отсюда и название «жирная кислота». Количество атомов углерода в жирной кислоте может составлять от 4 до 36; наиболее распространены те, которые содержат 12–18 атомов углерода. В молекуле жира жирная кислота присоединена к каждому из трех атомов кислорода в -ОН-группах молекулы глицерина ковалентной связью.
Фигура 2.18 Липиды включают жиры, такие как триглицериды, которые состоят из жирных кислот и глицерина, фосфолипидов и стероидов.Во время образования этой ковалентной связи высвобождаются три молекулы воды. Три жирные кислоты в жире могут быть похожими или разными. Эти жиры также называют триглицеридами , потому что они содержат три жирные кислоты. Некоторые жирные кислоты имеют общие названия, указывающие на их происхождение. Например, пальмитиновая кислота, насыщенная жирная кислота, получают из пальмы.Арахидовая кислота получена из Arachis hypogaea , научного названия арахиса.
Жирные кислоты могут быть насыщенными и ненасыщенными. В цепи жирной кислоты, если есть только одинарные связи между соседними атомами углерода в углеводородной цепи, жирная кислота является насыщенной. Насыщенные жирные кислоты насыщены водородом; другими словами, количество атомов водорода, прикрепленных к углеродному скелету, максимально.
Когда углеводородная цепь содержит двойную связь, жирная кислота представляет собой ненасыщенную жирную кислоту .
Большинство ненасыщенных жиров являются жидкими при комнатной температуре и называются маслами . Если в молекуле есть одна двойная связь, то он известен как мононенасыщенный жир (например, оливковое масло), а если имеется более одной двойной связи, то он известен как полиненасыщенный жир (например, масло канолы).
Насыщенные жиры, как правило, плотно упаковываются и остаются твердыми при комнатной температуре. Животные жиры со стеариновой кислотой и пальмитиновой кислотой, содержащиеся в мясе, и жир с масляной кислотой, содержащиеся в масле, являются примерами насыщенных жиров.Млекопитающие хранят жиры в специализированных клетках, называемых адипоцитами, где жировые шарики занимают большую часть клетки. У растений жир или масло хранятся в семенах и используются в качестве источника энергии во время эмбрионального развития.
Ненасыщенные жиры или масла обычно растительного происхождения и содержат ненасыщенные жирные кислоты. Двойная связь вызывает изгиб или «перегиб», который препятствует плотной упаковке жирных кислот, сохраняя их в жидком состоянии при комнатной температуре. Оливковое масло, кукурузное масло, масло канолы и жир печени трески являются примерами ненасыщенных жиров.Ненасыщенные жиры помогают повысить уровень холестерина в крови, тогда как насыщенные жиры способствуют образованию бляшек в артериях, что увеличивает риск сердечного приступа.
В пищевой промышленности масла искусственно гидрогенизируются для придания им полутвердого состояния, что приводит к меньшей порче и увеличению срока хранения. Проще говоря, газообразный водород пропускают через масла, чтобы отвердить их. Во время этого процесса гидрирования двойные связи цис -конформации в углеводородной цепи могут быть преобразованы в двойные связи в транс -конформации.Это образует транс -жир из цис--жира. Ориентация двойных связей влияет на химические свойства жира.
Рис. 2.19. В процессе гидрогенизации ориентация двойных связей меняется, в результате чего из цис-жира образуется транс-жир. Это изменяет химические свойства молекулы.Маргарин, некоторые виды арахисового масла и шортенинг являются примерами искусственно гидрогенизированных транс -жиров. Недавние исследования показали, что увеличение транс -жиров в рационе человека может привести к увеличению уровня липопротеинов низкой плотности (ЛПНП) или «плохого» холестерина, что, в свою очередь, может привести к отложению бляшек в организме человека. артерии, что приводит к болезни сердца.Многие рестораны быстрого питания недавно отказались от использования транс -жиров, и теперь в США на этикетках продуктов питания требуется указывать их содержание транс -жиров.
Незаменимые жирные кислоты — это жирные кислоты, которые необходимы, но не синтезируются человеческим организмом. Следовательно, их необходимо дополнять с помощью диеты. Омега-3 жирные кислоты попадают в эту категорию и являются одной из двух известных незаменимых жирных кислот для человека (другая — омега-6 жирные кислоты).Они представляют собой тип полиненасыщенных жиров и называются омега-3 жирными кислотами, потому что третий углерод на конце жирной кислоты участвует в двойной связи.
Лосось, форель и тунец являются хорошими источниками жирных кислот омега-3. Жирные кислоты омега-3 важны для работы мозга, нормального роста и развития. Они также могут предотвратить сердечные заболевания и снизить риск рака.
Как и углеводы, жиры получили широкую огласку. Это правда, что чрезмерное употребление жареной и другой «жирной» пищи приводит к увеличению веса.Однако жиры выполняют важные функции. Жиры служат долгосрочным накопителем энергии. Они также обеспечивают изоляцию тела. Поэтому «здоровые» ненасыщенные жиры в умеренных количествах следует употреблять регулярно.
Фосфолипиды являются основным компонентом плазматической мембраны. Как и жиры, они состоят из цепей жирных кислот, прикрепленных к глицерину или подобной основной цепи. Однако вместо трех жирных кислот есть две жирные кислоты, а третий углерод глицериновой цепи связан с фосфатной группой.Фосфатная группа модифицируется добавлением спирта.
Фосфолипид имеет как гидрофобные, так и гидрофильные участки. Цепи жирных кислот гидрофобны и исключаются из воды, тогда как фосфат гидрофильный и взаимодействует с водой.
Клетки окружены мембраной, которая имеет бислой фосфолипидов. Жирные кислоты фосфолипидов обращены внутрь, вдали от воды, тогда как фосфатная группа может быть обращена либо к внешней среде, либо к внутренней части клетки, которые оба являются водными.
Через призму коренных народов
Для первых народов Тихоокеанского Северо-Запада богатый жиром рыбный оолиган с содержанием жира 20% от веса тела был важной частью рациона нескольких коренных народов. Почему? Потому что жир является наиболее калорийной пищей, и наличие компактного высококалорийного источника энергии с возможностью хранения будет важно для выживания. Характер жира также сделал его важным товаром. Как и лосось, оолиган возвращается в свое русло после долгих лет в море. Его прибытие ранней весной сделало его первым свежим продуктом в году.В цимшианских языках прибытие оолигана… традиционно объявлялось криком «Хлаа ат’иксши халимутхв!»… Что означало: «Наш Спаситель только что прибыл!»
Рисунок 2.20 Изображение приготовленного оолигана. Эта жирная рыба с содержанием жира 20% от веса тела является важной частью диеты коренных народов.Как вы уже узнали, все жиры гидрофобны (ненавидят воду). Чтобы отделить жир, рыбу отваривают, а плавающий жир снимают. Жировой состав улигана состоит из 30% насыщенных жиров (например, сливочного масла) и 55% мононенасыщенных жиров (например, растительных масел).Важно отметить, что это твердая смазка при комнатной температуре. Поскольку в нем мало полиненасыщенных жиров (которые быстро окисляются и портятся), его можно хранить для дальнейшего использования и использовать в качестве предмета торговли. Считается, что его состав делает его таким же полезным, как оливковое масло, или лучше, поскольку он содержит жирные кислоты омега-3, которые снижают риск диабета и инсульта. Он также богат тремя жирорастворимыми витаминами A, E и K.
Стероиды и воски
В отличие от фосфолипидов и жиров, обсуждавшихся ранее, стероиды имеют кольцевую структуру.Хотя они не похожи на другие липиды, они сгруппированы с ними, потому что они также гидрофобны. Все стероиды имеют четыре связанных углеродных кольца, а некоторые из них, как и холестерин, имеют короткий хвост.
Холестерин — стероид. Холестерин в основном синтезируется в печени и является предшественником многих стероидных гормонов, таких как тестостерон и эстрадиол. Он также является предшественником витаминов Е и К. Холестерин является предшественником солей желчных кислот, которые помогают в расщеплении жиров и их последующем усвоении клетками.Хотя о холестерине часто говорят отрицательно, он необходим для правильного функционирования организма. Это ключевой компонент плазматических мембран клеток животных.
Воски состоят из углеводородной цепи со спиртовой (–OH) группой и жирной кислотой. Примеры восков животного происхождения включают пчелиный воск и ланолин. У растений также есть воск, например покрытие на листьях, которое помогает предотвратить их высыхание.
Концепция в действии
Чтобы получить дополнительную информацию о липидах, изучите «Биомолекулы: Липиды» с помощью этой интерактивной анимации.
Белки являются одной из самых распространенных органических молекул в живых системах и обладают самым разнообразным набором функций среди всех макромолекул. Белки могут быть структурными, регуляторными, сократительными или защитными; они могут служить для транспортировки, хранения или перепонки; или они могут быть токсинами или ферментами. Каждая клетка живой системы может содержать тысячи различных белков, каждый из которых выполняет уникальную функцию. Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры аминокислот, расположенных в линейной последовательности.
Функции белков очень разнообразны, потому что существует 20 различных химически различных аминокислот, которые образуют длинные цепи, и аминокислоты могут быть в любом порядке. Например, белки могут функционировать как ферменты или гормоны. Ферменты , которые вырабатываются живыми клетками, являются катализаторами биохимических реакций (например, пищеварения) и обычно являются белками. Каждый фермент специфичен для субстрата (реагента, который связывается с ферментом), на который он действует. Ферменты могут разрушать молекулярные связи, переупорядочивать связи или образовывать новые связи.Примером фермента является амилаза слюны, которая расщепляет амилозу, компонент крахмала.
Гормоны представляют собой химические сигнальные молекулы, обычно белки или стероиды, секретируемые эндокринной железой или группой эндокринных клеток, которые контролируют или регулируют определенные физиологические процессы, включая рост, развитие, метаболизм и размножение. Например, инсулин — это белковый гормон, который поддерживает уровень глюкозы в крови.
Белки имеют разную форму и молекулярную массу; некоторые белки имеют глобулярную форму, тогда как другие имеют волокнистую природу.Например, гемоглобин — это глобулярный белок, а коллаген, обнаруженный в нашей коже, — это волокнистый белок. Форма белка имеет решающее значение для его функции. Изменения температуры, pH и воздействие химикатов могут привести к необратимым изменениям формы белка, что приведет к потере функции или денатурации (более подробно это будет обсуждаться позже). Все белки состоят из 20 одних и тех же аминокислот по-разному.
Аминокислоты — это мономеры, из которых состоят белки.Каждая аминокислота имеет одинаковую фундаментальную структуру, которая состоит из центрального атома углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группы (–COOH) и атома водорода. Каждая аминокислота также имеет другой вариабельный атом или группу атомов, связанных с центральным атомом углерода, известную как группа R. Группа R — единственное различие в структуре между 20 аминокислотами; в остальном аминокислоты идентичны.
Рис. 2.21. Аминокислоты состоят из центрального углерода, связанного с аминогруппой (–Nh3), карбоксильной группой (–COOH) и атомом водорода.Четвертая связь центрального углерода варьируется среди различных аминокислот, как видно из этих примеров аланина, валина, лизина и аспарагиновой кислоты.Химическая природа группы R определяет химическую природу аминокислоты в ее белке (то есть, является ли она кислотной, основной, полярной или неполярной).
Последовательность и количество аминокислот в конечном итоге определяют форму, размер и функцию белка. Каждая аминокислота присоединена к другой аминокислоте ковалентной связью, известной как пептидная связь, которая образуется в результате реакции дегидратации.Карбоксильная группа одной аминокислоты и аминогруппа второй аминокислоты объединяются, высвобождая молекулу воды. Полученная связь представляет собой пептидную связь.
Продукты, образованные такой связью, называются полипептидами . Хотя термины полипептид и белок иногда используются как взаимозаменяемые, полипептид технически представляет собой полимер аминокислот, тогда как термин белок используется для полипептида или полипептидов, которые объединились вместе, имеют различную форму и имеют уникальную функцию.
Эволюция в действии
Эволюционное значение цитохрома c Цитохром c является важным компонентом молекулярного механизма, который собирает энергию из глюкозы. Поскольку роль этого белка в производстве клеточной энергии имеет решающее значение, за миллионы лет он очень мало изменился. Секвенирование белков показало, что существует значительное сходство последовательностей между молекулами цитохрома с разных видов; эволюционные отношения можно оценить путем измерения сходства или различий между белковыми последовательностями различных видов.
Например, ученые определили, что цитохром с человека содержит 104 аминокислоты. Для каждой молекулы цитохрома с, которая к настоящему времени была секвенирована у разных организмов, 37 из этих аминокислот находятся в одном и том же положении в каждом цитохроме с. Это указывает на то, что все эти организмы произошли от общего предка. При сравнении последовательностей белков человека и шимпанзе различий в последовательностях не обнаружено. При сравнении последовательностей человека и макаки-резуса было обнаружено единственное различие в одной аминокислоте.Напротив, сравнение человека с дрожжами показывает разницу в 44 аминокислотах, предполагая, что люди и шимпанзе имеют более недавнего общего предка, чем люди и макака-резус или люди и дрожжи.
Структура белка
Как обсуждалось ранее, форма белка имеет решающее значение для его функции. Чтобы понять, как белок приобретает свою окончательную форму или конформацию, нам необходимо понять четыре уровня структуры белка: первичный, вторичный, третичный и четвертичный .
Уникальная последовательность и количество аминокислот в полипептидной цепи — это ее первичная структура. Уникальная последовательность каждого белка в конечном итоге определяется геном, кодирующим этот белок. Любое изменение в последовательности гена может привести к добавлению другой аминокислоты к полипептидной цепи, вызывая изменение структуры и функции белка. При серповидно-клеточной анемии β-цепь гемоглобина имеет единственную аминокислотную замену, вызывающую изменение как структуры, так и функции белка.Что наиболее примечательно, так это то, что молекула гемоглобина состоит из двух альфа-цепей и двух бета-цепей, каждая из которых состоит примерно из 150 аминокислот. Таким образом, молекула содержит около 600 аминокислот. Структурное различие между нормальной молекулой гемоглобина и молекулой серповидноклеточных клеток, которое резко снижает продолжительность жизни у пораженных людей, составляет одну аминокислоту из 600.
Из-за этого изменения одной аминокислоты в цепи обычно двояковогнутые или дискообразные эритроциты принимают форму полумесяца или «серпа», что закупоривает артерии.Это может привести к множеству серьезных проблем со здоровьем, таких как одышка, головокружение, головные боли и боли в животе у людей, страдающих этим заболеванием.
Образцы сворачивания, возникающие в результате взаимодействий между частями аминокислот, не относящихся к R-группам, приводят к вторичной структуре белка. Наиболее распространены альфа (α) -спиральные и бета (β) -пластинчатые листовые структуры. Обе структуры удерживаются в форме водородными связями. В альфа-спирали связи образуются между каждой четвертой аминокислотой и вызывают поворот аминокислотной цепи.
В β-складчатом листе «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи. Группы R прикреплены к атомам углерода и проходят выше и ниже складок складки. Гофрированные сегменты выровнены параллельно друг другу, а водородные связи образуются между одинаковыми парами атомов на каждой из выровненных аминокислот. Структуры α-спирали и β-складчатых листов обнаруживаются во многих глобулярных и волокнистых белках.
Уникальная трехмерная структура полипептида известна как его третичная структура.Эта структура вызвана химическим взаимодействием между различными аминокислотами и участками полипептида. Прежде всего, взаимодействия между группами R создают сложную трехмерную третичную структуру белка. Могут быть ионные связи, образованные между группами R на разных аминокислотах, или водородные связи, помимо тех, которые участвуют во вторичной структуре. Когда происходит сворачивание белка, гидрофобные группы R неполярных аминокислот лежат внутри белка, тогда как гидрофильные группы R лежат снаружи.Первые типы взаимодействий также известны как гидрофобные взаимодействия.
В природе некоторые белки образованы из нескольких полипептидов, также известных как субъединицы, и взаимодействие этих субъединиц образует четвертичную структуру. Слабые взаимодействия между субъединицами помогают стабилизировать общую структуру. Например, гемоглобин представляет собой комбинацию четырех полипептидных субъединиц.
Рис. 2.22 На этих иллюстрациях можно увидеть четыре уровня белковой структуры.Каждый белок имеет свою уникальную последовательность и форму, удерживаемую химическими взаимодействиями.Если белок подвержен изменениям температуры, pH или воздействию химикатов, структура белка может измениться, потеряв свою форму в результате так называемой денатурации , как обсуждалось ранее. Денатурация часто обратима, поскольку первичная структура сохраняется, если денатурирующий агент удаляется, позволяя белку возобновить свою функцию. Иногда денатурация необратима, что приводит к потере функции. Один из примеров денатурации белка можно увидеть, когда яйцо жарят или варят.Белок альбумина в жидком яичном белке денатурируется при помещении на горячую сковороду, превращаясь из прозрачного вещества в непрозрачное белое вещество. Не все белки денатурируются при высоких температурах; например, бактерии, которые выживают в горячих источниках, имеют белки, которые адаптированы для работы при этих температурах.
Концепция в действии
Чтобы получить дополнительную информацию о белках, исследуйте «Биомолекулы: Белки» с помощью этой интерактивной анимации.
Нуклеиновые кислоты являются ключевыми макромолекулами в непрерывности жизни.Они несут генетический план клетки и несут инструкции для функционирования клетки.
Двумя основными типами нуклеиновых кислот являются дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК) . ДНК — это генетический материал, содержащийся во всех живых организмах, от одноклеточных бактерий до многоклеточных млекопитающих.
Другой тип нуклеиновой кислоты, РНК, в основном участвует в синтезе белка. Молекулы ДНК никогда не покидают ядро, а вместо этого используют посредника РНК для связи с остальной частью клетки.Другие типы РНК также участвуют в синтезе белка и его регуляции.
ДНК и РНК состоят из мономеров, известных как нуклеотидов . Нуклеотиды объединяются друг с другом с образованием полинуклеотида, ДНК или РНК. Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозного (пятиуглеродного) сахара и фосфатной группы. Каждое азотистое основание в нуклеотиде присоединено к молекуле сахара, которая присоединена к фосфатной группе.
Рис. 2.23. Нуклеотид состоит из трех компонентов: азотистого основания, пентозного сахара и фосфатной группы. ДНКимеет двойную спиральную структуру. Он состоит из двух цепей или полимеров нуклеотидов. Нити образованы связями между фосфатными и сахарными группами соседних нуклеотидов. Нити связаны друг с другом в своих основаниях водородными связями, и нити наматываются друг на друга по своей длине, отсюда и описание «двойной спирали», что означает двойную спираль.
Рис. 2.24. Химическая структура ДНК с цветной меткой, обозначающей четыре основания, а также фосфатный и дезоксирибозный компоненты основной цепи.Чередующиеся сахарные и фосфатные группы лежат на внешней стороне каждой цепи, образуя основу ДНК. Азотистые основания сложены внутри, как ступени лестницы, и эти основания соединяются в пару; пары связаны друг с другом водородными связями. Основания спариваются таким образом, чтобы расстояние между скелетами двух цепей было одинаковым по всей длине молекулы. Правило состоит в том, что нуклеотид A соединяется с нуклеотидом T, а G — с C, см. Раздел 9.1 для более подробной информации.
Живые существа основаны на углероде, потому что углерод играет такую важную роль в химии живых существ. Четыре позиции ковалентной связи атома углерода могут дать начало широкому разнообразию соединений с множеством функций, что объясняет важность углерода для живых существ. Углеводы — это группа макромолекул, которые являются жизненно важным источником энергии для клетки, обеспечивают структурную поддержку многих организмов и могут быть обнаружены на поверхности клетки в качестве рецепторов или для распознавания клеток.Углеводы классифицируются как моносахариды, дисахариды и полисахариды, в зависимости от количества мономеров в молекуле.
Липиды — это класс макромолекул, неполярных и гидрофобных по природе. Основные типы включают жиры и масла, воски, фосфолипиды и стероиды. Жиры и масла представляют собой запасенную форму энергии и могут включать триглицериды. Жиры и масла обычно состоят из жирных кислот и глицерина.
Белки — это класс макромолекул, которые могут выполнять широкий спектр функций для клетки.Они помогают метаболизму, обеспечивая структурную поддержку и действуя как ферменты, переносчики или гормоны. Строительными блоками белков являются аминокислоты. Белки организованы на четырех уровнях: первичный, вторичный, третичный и четвертичный. Форма и функция белка неразрывно связаны; любое изменение формы, вызванное изменениями температуры, pH или химического воздействия, может привести к денатурации белка и потере функции.
Нуклеиновые кислоты — это молекулы, состоящие из повторяющихся единиц нуклеотидов, которые управляют клеточной деятельностью, такой как деление клеток и синтез белка.Каждый нуклеотид состоит из пентозного сахара, азотистого основания и фосфатной группы. Есть два типа нуклеиновых кислот: ДНК и РНК.
аминокислота : мономер протеина
углевод: биологическая макромолекула, в которой отношение углерода к водороду к кислороду составляет 1: 2: 1; углеводы служат источниками энергии и структурной поддержкой в клетках
целлюлоза: полисахарид, который составляет клеточные стенки растений и обеспечивает структурную поддержку клетки
хитин: вид углеводов, образующих внешний скелет членистоногих, таких как насекомые и ракообразные, и клеточные стенки грибов
денатурация: потеря формы белка в результате изменений температуры, pH или воздействия химических веществ
дезоксирибонуклеиновая кислота (ДНК): двухцепочечный полимер нуклеотидов, несущий наследственную информацию клетки
дисахарид: два мономера сахара, которые связаны между собой пептидной связью
фермент : катализатор биохимической реакции, который обычно представляет собой сложный или конъюгированный белок
жир: липидная молекула, состоящая из трех жирных кислот и глицерина (триглицерида), которая обычно существует в твердой форме при комнатной температуре
гликоген: запасной углевод у животных
гормон: химическая сигнальная молекула, обычно белок или стероид, секретируемая эндокринной железой или группой эндокринных клеток; действия по контролю или регулированию определенных физиологических процессов
липиды: класс макромолекул, неполярных и нерастворимых в воде
макромолекула: большая молекула, часто образованная полимеризацией более мелких мономеров
моносахарид: отдельная единица или мономер углеводов
нуклеиновая кислота: биологическая макромолекула, несущая генетическую информацию клетки и инструкции для функционирования клетки
нуклеотид: мономер нуклеиновой кислоты; содержит пентозный сахар, фосфатную группу и азотистое основание
масло: ненасыщенный жир, являющийся жидкостью при комнатной температуре
фосфолипид: основной компонент мембран клеток; состоит из двух жирных кислот и фосфатной группы, присоединенной к основной цепи глицерина
полипептид: длинная цепь аминокислот, связанных пептидными связями
полисахарид: длинная цепь моносахаридов; могут быть разветвленными и неразветвленными
белок: биологическая макромолекула, состоящая из одной или нескольких цепочек аминокислот
рибонуклеиновая кислота (РНК): одноцепочечный полимер нуклеотидов, участвующий в синтезе белка
насыщенная жирная кислота: длинноцепочечный углеводород с одинарными ковалентными связями в углеродной цепи; количество атомов водорода, прикрепленных к углеродному скелету, максимально
крахмал: запасной углевод в растениях
стероид: тип липида, состоящий из четырех конденсированных углеводородных колец
транс-жиры: форма ненасыщенного жира с атомами водорода, соседствующими с двойной связью напротив друг друга, а не на одной стороне двойной связи
триглицерид: молекула жира; состоит из трех жирных кислот, связанных с молекулой глицерина
ненасыщенная жирная кислота: длинноцепочечный углеводород, имеющий одну или несколько двойных связей в углеводородной цепи
Атрибуция в СМИ
сот | Определение, типы, функции, диаграмма, деление, теория и факты
Подумайте, как одноклеточный организм содержит необходимые структуры для питания, роста и воспроизводства.
Клетки — это основные единицы жизни.
Encyclopædia Britannica, Inc. Смотрите все видео к этой статьеКлетка , в биологии, основная мембраносвязанная единица, которая содержит основные молекулы жизни и из которых состоит все живое. Одна клетка сама по себе часто является целостным организмом, например бактерией или дрожжами. По мере созревания другие клетки приобретают особые функции. Эти клетки взаимодействуют с другими специализированными клетками и становятся строительными блоками больших многоклеточных организмов, таких как люди и другие животные.Хотя клетки намного больше атомов, они все же очень маленькие. Самые маленькие из известных клеток — это группа крошечных бактерий, называемых микоплазмами; некоторые из этих одноклеточных организмов представляют собой сферы диаметром всего 0,2 мкм (1 мкм = около 0,000039 дюйма) с общей массой 10 -14 грамм, что равно 8 000 000 000 атомов водорода. Клетки человека обычно имеют массу в 400 000 раз больше, чем масса отдельной бактерии микоплазмы, но даже человеческие клетки имеют только около 20 мкм в поперечнике.Для того, чтобы закрыть булавочную головку, потребуется лист из примерно 10 000 человеческих клеток, а каждый человеческий организм состоит из более чем 30 000 000 000 000 клеток.
животная клеткаОсновные структуры животной клетки Цитоплазма окружает специализированные структуры клетки, или органеллы. Рибосомы, места синтеза белка, находятся в цитоплазме в свободном состоянии или прикреплены к эндоплазматическому ретикулуму, через который материалы транспортируются по клетке. Энергия, необходимая клетке, выделяется митохондриями.Комплекс Гольджи, стопки сплющенных мешочков, обрабатывает и упаковывает материалы, которые должны быть выпущены из клетки в секреторные пузырьки. Пищеварительные ферменты содержатся в лизосомах. Пероксисомы содержат ферменты, выводящие токсины из опасных веществ. Центросома содержит центриоли, которые играют роль в делении клеток. Микроворсинки — это пальцевидные отростки, обнаруженные на определенных клетках. Реснички, похожие на волосы структуры, которые выходят на поверхность многих клеток, могут создавать движение окружающей жидкости. Ядерная оболочка, двойная мембрана, окружающая ядро, содержит поры, которые контролируют движение веществ в нуклеоплазму и из нее.Хроматин, комбинация ДНК и белков, образующих хромосомы, составляет большую часть нуклеоплазмы. Плотное ядрышко — место производства рибосом.
© Merriam-Webster Inc.Популярные вопросы
Что такое ячейка?
Клетка — это масса цитоплазмы, которая снаружи связана клеточной мембраной. Обычно микроскопические по размеру клетки представляют собой мельчайшие структурные единицы живого вещества и составляют все живое. Большинство клеток имеют одно или несколько ядер и других органелл, которые выполняют множество задач.Некоторые отдельные клетки представляют собой полноценные организмы, такие как бактерии или дрожжи. Другие представляют собой специализированные строительные блоки многоклеточных организмов, таких как растения и животные.
Что такое клеточная теория?
Теория клетки утверждает, что клетка является фундаментальной структурной и функциональной единицей живого вещества. В 1839 году немецкий физиолог Теодор Шванн и немецкий ботаник Маттиас Шлейден заявили, что клетки являются «элементарными частицами организмов» как у растений, так и у животных, и признали, что одни организмы одноклеточные, а другие — многоклеточные.Эта теория ознаменовала собой большой концептуальный прогресс в биологии и привела к возобновлению внимания к жизненным процессам, происходящим в клетках.
Что делают клеточные мембраны?
Клеточная мембрана окружает каждую живую клетку и отделяет клетку от окружающей среды. Он служит барьером, препятствующим проникновению содержимого клетки и проникновению нежелательных веществ. Он также функционирует как ворота, как для активного, так и для пассивного перемещения основных питательных веществ в клетку и вывод продуктов жизнедеятельности из нее.Определенные белки клеточной мембраны участвуют в межклеточной коммуникации и помогают клетке реагировать на изменения в окружающей среде.
В этой статье клетка рассматривается как отдельная единица и как составляющая часть более крупного организма. Как отдельная единица, клетка способна метаболизировать свои собственные питательные вещества, синтезировать многие типы молекул, обеспечивать свою собственную энергию и воспроизводить себя, чтобы производить последующие поколения. Его можно рассматривать как закрытый сосуд, внутри которого одновременно происходят бесчисленные химические реакции.Эти реакции находятся под очень точным контролем, поэтому они способствуют жизни и размножению клетки. В многоклеточном организме клетки становятся специализированными для выполнения различных функций в процессе дифференцировки. Для этого каждая ячейка поддерживает постоянную связь со своими соседями. Поскольку он получает питательные вещества из окружающей среды и выбрасывает отходы в окружающую среду, он прилипает к другим клеткам и взаимодействует с ними. Совместные сборки подобных клеток образуют ткани, а сотрудничество между тканями, в свою очередь, формирует органы, которые выполняют функции, необходимые для поддержания жизни организма.
Особое внимание в этой статье уделяется клеткам животных, с некоторым обсуждением процессов синтеза энергии и внеклеточных компонентов, свойственных растениям. (Для подробного обсуждения биохимии растительных клеток, см. Фотосинтез . Для полной обработки генетических событий в ядре клетки, см. Наследственность .)
Брюс М. АльбертсПрирода и функция клеток
A клетка окружена плазматической мембраной, которая образует селективный барьер, который позволяет питательным веществам проникать, а продукты жизнедеятельности — выходить.Внутренняя часть клетки состоит из множества специализированных отсеков или органелл, каждый из которых окружен отдельной мембраной. Одна из основных органелл, ядро, содержит генетическую информацию, необходимую для роста и размножения клеток. Каждая клетка содержит только одно ядро, тогда как другие типы органелл присутствуют в множестве копий в клеточном содержимом или цитоплазме. Органеллы включают митохондрии, которые отвечают за передачу энергии, необходимую для выживания клеток; лизосомы, которые переваривают нежелательные материалы внутри клетки; а также эндоплазматический ретикулум и аппарат Гольджи, которые играют важную роль во внутренней организации клетки, синтезируя выбранные молекулы, а затем обрабатывая, сортируя и направляя их в нужные места.Кроме того, клетки растений содержат хлоропласты, которые отвечают за фотосинтез, благодаря чему энергия солнечного света используется для преобразования молекул углекислого газа (CO 2 ) и воды (H 2 O) в углеводы. Между всеми этими органеллами есть пространство в цитоплазме, называемое цитозолем. Цитозоль содержит организованный каркас из волокнистых молекул, составляющих цитоскелет, который придает клетке ее форму, позволяет органеллам перемещаться внутри клетки и обеспечивает механизм, с помощью которого сама клетка может двигаться.Цитозоль также содержит более 10 000 различных видов молекул, которые участвуют в клеточном биосинтезе, процессе создания больших биологических молекул из маленьких.
клетокКлетки животных и растений содержат мембраносвязанные органеллы, включая отдельное ядро. Напротив, бактериальные клетки не содержат органелл.
Encyclopædia Britannica, Inc. Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасСпециализированные органеллы характерны для клеток организмов, известных как эукариоты.Напротив, клетки организмов, известных как прокариоты, не содержат органелл и обычно меньше эукариотических клеток. Однако все клетки имеют сильное сходство в биохимических функциях.
эукариотическая клеткаИзображение эукариотической клетки в разрезе.
Encyclopædia Britannica, Inc.Молекулы клеток
Понять, как клеточные мембраны регулируют потребление пищи и отходы и как клеточные стенки обеспечивают защиту
Клетки поглощают молекулы через свои плазматические мембраны.
Encyclopædia Britannica, Inc. Посмотреть все видео к этой статьеКлетки содержат особый набор молекул, заключенных в мембрану. Эти молекулы дают клеткам возможность расти и воспроизводиться. Общий процесс клеточного воспроизводства происходит в два этапа: рост клеток и деление клеток. Во время роста клетки клетки поглощают определенные молекулы из своего окружения, избирательно перенося их через клеточную мембрану. Попав внутрь клетки, эти молекулы подвергаются действию узкоспециализированных, больших, тщательно свернутых молекул, называемых ферментами.Ферменты действуют как катализаторы, связываясь с проглоченными молекулами и регулируя скорость их химического изменения. Эти химические изменения делают молекулы более полезными для клетки. В отличие от проглоченных молекул, катализаторы сами химически не изменяются во время реакции, что позволяет одному катализатору регулировать конкретную химическую реакцию во многих молекулах.
Биологические катализаторы создают цепочки реакций. Другими словами, молекула, химически преобразованная одним катализатором, служит исходным материалом или субстратом для второго катализатора и так далее.Таким образом, катализаторы используют небольшие молекулы, принесенные в клетку из внешней среды, для создания все более сложных продуктов реакции. Эти продукты используются для роста клеток и воспроизведения генетического материала. После копирования генетического материала и наличия достаточного количества молекул для поддержки деления клетки клетка делится, образуя две дочерние клетки. Через множество таких циклов клеточного роста и деления каждая родительская клетка может дать начало миллионам дочерних клеток, в процессе преобразования больших количеств неодушевленного вещества в биологически активные молекулы.
клеточная мембрана | Определение, функции и структура
Клеточная мембрана , также называемая плазматической мембраной , тонкая мембрана, которая окружает каждую живую клетку, отделяя клетку от окружающей ее среды. Этой клеточной мембраной (также известной как плазматическая мембрана) окружены составляющие клетки, часто большие, водорастворимые, сильно заряженные молекулы, такие как белки, нуклеиновые кислоты, углеводы и вещества, участвующие в клеточном метаболизме. Вне клетки, в окружающей водной среде, находятся ионы, кислоты и щелочи, которые токсичны для клетки, а также питательные вещества, которые клетка должна поглощать, чтобы жить и расти.Таким образом, клеточная мембрана выполняет две функции: во-первых, быть барьером, удерживающим составляющие клетки внутри и нежелательными веществами, и, во-вторых, быть воротами, позволяющими переносить в клетку необходимые питательные вещества и перемещаться из клетки с отходами. продукты.
Молекулярный вид клеточной мембраныВнутренние белки проникают в липидный бислой и прочно связываются с ним, который состоит в основном из фосфолипидов и холестерина и который обычно составляет от 4 до 10 нанометров (нм; 1 нм = 10 −9 метр ) по толщине.Внешние белки слабо связаны с гидрофильными (полярными) поверхностями, которые обращены к водной среде как внутри, так и снаружи клетки. Некоторые внутренние белки представляют собой боковые цепи сахара на внешней поверхности клетки.
Encyclopædia Britannica, Inc.Подробнее по этой теме
Клетка: клеточная мембрана
Тонкая мембрана, обычно толщиной от 4 до 10 нанометров (нм; 1 нм = 10-9 метров), окружает каждую живую клетку, ограничивая ее границы…
Клеточные мембраны состоят в основном из липидов и белков на основе жирных кислот. Мембранные липиды в основном бывают двух типов: фосфолипиды и стерины (обычно холестерин). Оба типа разделяют определяющую характеристику липидов — они легко растворяются в органических растворителях, но, кроме того, у них обоих есть область, которая притягивается к воде и растворяется в ней. Это «амфифильное» свойство (обладающее двойным притяжением; то есть наличие как жирорастворимой, так и водорастворимой области) является основным для роли липидов как строительных блоков клеточных мембран.Мембранные белки также бывают двух основных типов. Один тип, называемый внешними белками, слабо прикреплен ионными связями или кальциевыми мостиками к электрически заряженной фосфорильной поверхности бислоя. Они также могут присоединяться ко второму типу белков, называемым внутренними белками. Внутренние белки, как следует из их названия, прочно встроены в фосфолипидный бислой. Как правило, мембраны, активно участвующие в метаболизме, содержат более высокую долю белка.
Химическая структура клеточной мембраны делает ее необычайно гибкой, идеальной границей для быстро растущих и делящихся клеток.Тем не менее, мембрана также является грозным барьером, позволяющим проходить одним растворенным веществам или растворенным веществам, блокируя другие. Липидорастворимые молекулы и некоторые небольшие молекулы могут проникать через мембрану, но липидный бислой эффективно отталкивает множество крупных водорастворимых молекул и электрически заряженных ионов, которые клетка должна импортировать или экспортировать, чтобы жить. Транспорт этих жизненно важных веществ осуществляется определенными классами внутренних белков, которые образуют множество транспортных систем: некоторые из них являются открытыми каналами, которые позволяют ионам диффундировать непосредственно в клетку; другие — «посредники», которые помогают растворенным веществам диффундировать за липидный экран; третьи — это «насосы», которые заставляют растворенные вещества проходить через мембрану, когда они недостаточно сконцентрированы для самопроизвольной диффузии.Частицы, слишком большие для диффузии или перекачивания, часто проглатываются или выбрасываются целиком при открытии и закрытии мембраны.
Вызывая трансмембранные движения больших молекул, сама клеточная мембрана совершает согласованные движения, во время которых часть жидкой среды вне клетки интернализуется (эндоцитоз) или часть внутренней среды клетки выводится наружу (экзоцитоз). Эти движения включают слияние поверхностей мембран с последующим воссозданием неповрежденных мембран.
Эндоцитоз, опосредованный рецепторамиРецепторы играют ключевую роль во многих клеточных процессах. Например, рецептор-опосредованный эндоцитоз позволяет клеткам поглощать молекулы, такие как белки, которые необходимы для нормального функционирования клеток.
Encyclopædia Britannica, Inc. Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасCytology Quiz: Cell Membrane (Plasma Membrane)
(1). Средняя толщина плазматической мембраны эукариотической клетки составляет:
A.От 5 до 10 нм
B. от 5 до 10 Å
C. от 5 до 10 мкм
D. от 5 до 10 мкм
(2). Что из перечисленного НЕ является функцией плазматической мембраны?
A. Межклеточные взаимодействия
B. Реагирование на внешние раздражители
C. Передача энергии
D. Помощь в сегрегации хромосом
(3). Какое из следующих утверждений относительно поверхностного натяжения плазматической мембраны верно?
А.Поверхностное натяжение плазматической мембраны больше, чем у чистых липидных структур
B. Поверхностное натяжение плазматической мембраны меньше, чем у чистых липидных структур
C. Поверхностное натяжение плазматической мембраны и чистых липидных структур одинаково
D. Плазменная мембрана не имеет поверхностного натяжения
(4). Какое из следующих утверждений лучше всего описывает химический состав плазматической мембраны?
A. Плазменная мембрана состоит из двух слоев: одного слоя фосфолипидов и одного слоя белков.
B. Плазменная мембрана состоит из равного количества фосфолипидов, белков и углеводов.
C. Плазменная мембрана представляет собой бислой белков с ассоциированными липидами и углеводами.
D. Плазменная мембрана представляет собой бислой фосфолипидов с ассоциированными белками и углеводами.
(5). Рассмотрим следующие утверждения:
A. Полярная часть холестерина обращена наружу по отношению к мембране
B. Размещение молекул холестерина в мембране влияет на гибкость углеводородной цепи липидов
C.Холестерин обеспечивает жесткость мембраны
D. Холестерин отсутствует в плазматической мембране растений
E. Холестерин отсутствует в плазматической мембране бактерий
Какое из приведенных выше утверждений является правильным?
A. A, B, C, D, E
B. A, B, C, E
C. A, C, D, E
D. A, C, D, E
Вам также может понравиться : PPTs Cell and Molecular Biology
(6). Биохимический анализ образца плазматической мембраны показал около 20-25% содержания кардиолипина (тип мембранного липида).Скорее всего, это образец из:
A. Клеточная мембрана эритроцитов человека
B. Миелиновая оболочка нервных клеток
C. Внутренняя мембрана митохондрий
D. Наружная мембрана митохондрий
(7). Гликолипиды в плазматической мембране обычно расположены по адресу:
A. Внешний листок плазматической мембраны
B. Внутренний листок плазматической мембраны
C. Равномерно распределены как во внутренних, так и во внешних листах плазматической мембраны
D. Невозможно предсказать, это варьируется по типам ячеек
(8).Какое из следующих событий в биологической мембране не было бы энергетически выгодным и, следовательно, не происходило бы спонтанно?
A. вращение мембранных белков
B. вращение фосфолипидов
C. латеральное движение фосфолипидов
D. триггер фосфолипидов к противоположной створке
(9). Малярийный паразит использует ________ на плазматической мембране эритроцитов в качестве рецептора для входа в клетку
A. Белок группы 3
B.Гликофорины
C. Белок спектрин
D. Анкириновые белки
(10). Содержание углеводов в плазматической мембране эукариот составляет:
A. 2-10% по весу
B. 20-25% по весу
C. 30-50% по весу
D. 60-70% по весу
Вам также может понравиться: Конспект лекций по клеточной и молекулярной биологии
(11). Углеводы в плазматической мембране:
A.Всегда лицом внутрь к неполярной части мембраны
B. Всегда лицом наружу, к внеклеточному пространству
C. Всегда лицом к просвету клеток
D. Направлен во все стороны в мембране случайным образом
(12). Мышечная дистрофия, разрушительное заболевание, которое калечат и убивает детей, вызывается:
A. Мутация в дистрофине
B. Мутация в белке полосы 3
C. Мутация в гликофорине A
D. Мутация в анкирине
(13) .Ферменты, такие как десатураза, фосфолипаза и ацетилтрансфераза, очень важны для поддержания целостности плазматических мембран. Эти ферменты участвуют в:
A. Поддержание двухслойной природы мембраны
B. Поддержание полупроницаемости мембраны
C. Поддержание текучести мембраны
D. Сохранение положения трансмембранных белков в мембране
(14). Человек, имеющий фермент, который добавляет N-ацетилгалактозамин к гликолипидам, которые определяют группу крови.Группа крови человека будет
A. A
B. B
C. AB
D. O
(15). Человек, имеющий фермент, который добавляет галактозу к гликолипидам, которые определяют группу крови. Группа крови человека будет
A. A
B. B
C. AB
D. O
(16). Эритроциты в крови отталкиваются друг от друга из-за:
A. Вогнутой формы RBC
B.У них отсутствует ядро и другие мембранные структуры
C. Углеводные фрагменты гликофорина A в мембране эритроцитов содержат остатки сиаловой кислоты
D. Аминокислоты в периферической части гликофорина A заряжены отрицательно
(17). Основная роль углеводов в клеточной мембране —
A. Адгезия
B. Распознавание
C. Передвижение
D. Прием
(18). Лучший метод изучения свойств интегральных мембранных белков в плазматической мембране —
A.Криосрезы и электронная микроскопия
B. Анализ разрушения при замораживании и электронная микроскопия
C. Атомно-силовая микроскопия
D. Все эти методы
(19). Якорные белки GPI:
A. Периферические белки плазматической мембраны
B. Интегральные белки плазматической мембраны
C. Белки, которые случайным образом связываются с липидами плазматической мембраны
D. Белки, которые связываются с ионно-управляемыми каналами в плазматической мембране
(20).Текучесть плазматической мембраны увеличивается с
A. Увеличение насыщенных жирных кислот в мембране
B. Увеличение ненасыщенных жирных кислот в мембране
C. Увеличение содержания фосфолипидов в мембране
D. Увеличение содержания гликолипидов в мембране мембрана
Больше MCQ для цитологии
Ответ и пояснения…
1. Ответ. (А). От 5 до 10 нм
2.Ответ (D). Помощь в сегрегации хромосом
Подробнее: Мембранные липиды: свойства, структура и классификация + PPT
Функции плазматической мембраны: (1). Селективный захват и экспорт ионов и молекул; (2). Компартментализация клеток; (3). Сортировка белков; (4). Закрепление цитоскелета; (5). Производство промежуточных энергетических продуктов, таких как АТФ и НАДФН; (6). Передача сигналов клетки; (7). Клеточное и ядерное деление; (8). Адгезия клеток между собой и с внеклеточным матриксом
3.Ответ (В). Поверхностное натяжение плазматической мембраны меньше, чем у чистых липидных структур
Это наблюдение привело к открытию белков в мембране. Снижение поверхностного натяжения мембраны по сравнению с чистыми липидными структурами связано с присутствием белков в плазматической мембране.
4. Ответ. (D). Плазменная мембрана представляет собой бислои фосфолипидов с ассоциированными белками и углеводами
5. Отв. (А). A, B, C, D
6.Ответ (D). Наружная мембрана митохондрий
Единственное другое место, где можно найти кардиолипин, — это плазматическая мембрана бактерий. Присутствие кардиолипина во внешней мембране митохондрий является одним из самых убедительных доказательств эндосимбионтной теории происхождения митохондрий у эукариот.
7. Отв. (А). Наружный листок плазматической мембраны
Они образуют гликокаликс клетки
8. Отв. (D). Флип-флоп фосфолипидов к противоположной створке
9.Ответ (В). Гликофорины
10. Отв. (А). 2 — 10% по весу
11. Отв. (В). Всегда лицом наружу, во внеклеточное пространство
12. Отв. (А). Мутация в дистрофине
13. Отв. (С). Поддержание текучести мембраны
14. Ответ. (А). A
15. Отв. (В). Б
16.Ответ (С). Углеводные фрагменты гликофорина А в мембране эритроцитов содержат остатки сиаловой кислоты
17. Отв. (В). Признание
18. Отв. (В). Анализ трещин при замораживании и электронная микроскопия
19. Отв. (А). Периферические белки плазматической мембраны
20. Отв. (В). Увеличение ненасыщенных жирных кислот в мембране
Ключ ответа подготовлен с учетом наших знаний.
Не стесняйтесь сообщать Admin , если вы обнаружите какие-либо ошибки в ключе ответа.
