Проект «Три состояния воды» | Обучонок
В детской исследовательской работе по биологии на тему «Три состояния воды» автор выясняет, что такое вода, а также проводит исследование и изучение свойств воды для того, что понимать условия изменения агрегатного состояния воды, и как этот процесс влияет на природу и живых организмов.
Подробнее о работе
В ученической исследовательской работе по биологии на тему «Три состояния воды» собрана и проанализирована научная литература по изучаемому вопросу, проведены практические эксперименты по определению цвета и запаха воды, основных свойств воды. В процессе работы над проектом учащаяся выявила пользу каждого агрегатного состояния воды для живых организмов.
Данный индивидуальный проект по биологии на тему «Три состояния воды» содержит описание твёрдого агрегатного состояния воды, а также жидкого и газообразного. В завершении исследования автором проекта были изучены и описаны фазовые переходы воды из одного состояния в другое.
Оглавление
Введение
1. История изучения свойств воды.
1.1 Твёрдое агрегатное состояние воды
1.2 Жидкое агрегатное состояние воды
1.3 Газообразное агрегатное состояние воды
1.4 Фазовые переходы
Заключение
Список использованной литературы
Введение
Любому человеку с детства занокомо выражение «Что такое Н2О». Каждый с уверенностью ответит что это конечно же вода! Данная жидкость зачастую встречается и в устном народном творчестве, а чаще всего в загадках, пословицах и поговорках.
Например: сапоги мои того, пропускают Н2О, вода камень точит, длинные сосульки — долгий лён, как с гуся вода, на обиженных воду возят и многие другие.
Мы каждый день пользуемся водой. Вода служит универсальным источником для питья и мытья, для поливки сельскохозяйственных культур, для отопления жилых помещений, и этот список не имеет конца. Но кто — нибудь хоть раз задавался вопросом: « А что такое вода? Почему снег — это тоже вода? Как укротить воду ?».
В данной исследовательской работе постараемся дать ответы на поставленные вопросы, и выяснить, почему вода имеет три состояния по сравнению с другими жидкостями.
Цель работы: исследование и изучение свойств воды для того, что понимать условия изменения агрегатного состояния воды, как этот процесс влияет на природу и живых организмов.
Объект исследования: три агрегатных состояния воды.
Предмет исследования: вода.
Задачи:
- Определить цвет и запах воды.
- Определить основные свойства воды.
- Выявить пользу каждого агрегатного состояния воды для живых организмов.
История изучения свойств воды
Истоки древней философии гласят о том, что всё в природе образовано четырьмя элементами (стихиями): земля, воздух, огонь и вода. Данная идея просуществовала до начала Средних веков.
В 1783 году основатель современной химии Антуан Лоран Лавуазье смог опытным путём доказать, что вода — это не химический элемент, в соединение водорода и кислорода.
В 1819 году шведский химик Йёнс Якоб Берцелиус и французский химик Пьер Луи Дюлонг и чуть позже в 1842 году французский химик Жан Батист Дюма совместно с бельгийским химиком Жаном Серве Стасом смогли установить весовой состав воды, пропуская водород через оксид меди.
Исходя из проведённых лабораторных исследований, учёные смогли определить соотношение водорода к кислороду для воды. В 1820 году французский химик Жозеф Луи Гей — Люссак смог измерить объёмы газообразного водорода и кислорода, которые при взаимодействии давали воду. Выведенное соотношение показало выражение 2 к 1, которое отвечает современной формуле воды —
На сегодняшний день можно было бы сказать о том, что человечество уже знает всё о воде, но как вода появилась на планете Земля до сих пор остаётся нерешённым. Часть учёных говорит о том, что вода на Земле образовалась за счёт синтеза водорода и кислорода. Советский математик Отто Юльевич Шмидт считает, что вода на нашу планету была привнесена из космического пространства при образовании планеты.
Советский математик Отто Юльевич Шмидт считает, что вода на нашу планету была привнесена из космического пространства при образовании планеты.
Вместе с космической пылью и минеральными частицами на Землю падали куски и глыбы космического льда, которые при разогревании планеты превращались в водяной пар и воду.
Основные сведения в воде
№ 1. Химическая формула воды — Н2О
№ 2. Вода — это жидкость без цвета, вкуса и запаха.
№ 4. Человеческое тело более чем на 65 % состоит из воды.
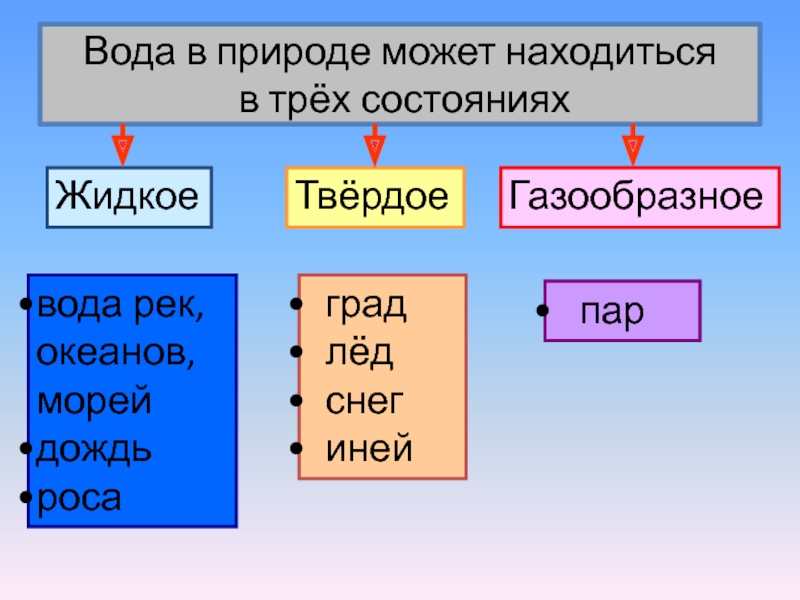
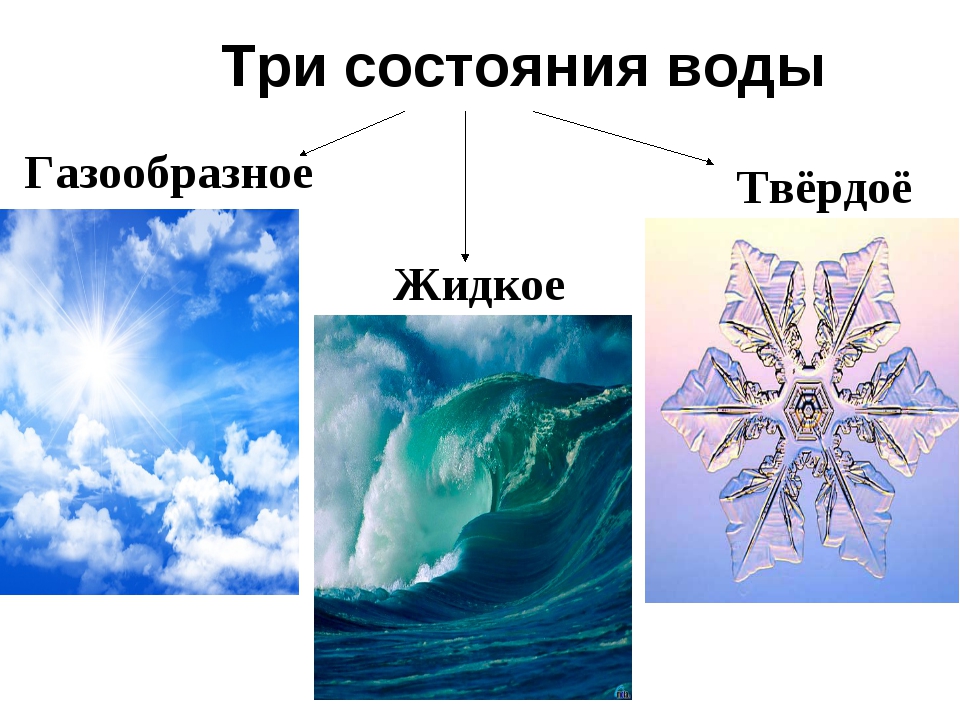
№ 5. Вода в природе представлена в трёх агрегатных состояниях — твёрдом, жидком и газообразном.
РИС.1 Отображение агрегатных состояний воды
75 % процентов поверхности планеты Земля покрыто водой. На научном языке водную оболочку нашей планеты называют Гидросфера. Основная часть данной оболочки составлена из солёных вод морей и океанов и чуть меньше занимает пресная вода рек, озёр, ледников, грунтовых вод.
Как известно, вода на земле существует в трёх агрегатных состояниях — твёрдом, жидком и газообразном. Абсолютно в любом живом организме вода необходима для осуществления различных химических реакций, без которых невозможна жизнь. Вода является самым ценным и самым необходимым веществом для жизнедеятельности живых организмов.
Постоянный обмен влагой между гидросферой, атмосферой и земной поверхностью, состоящий из процессов испарения, передвижения водяного пара в атмосфере, его конденсации в атмосфере, выпадения осадков и стока, получил название круговорота воды в природе. Атмосферные осадки частично испаряются, частично образуют временные и постоянные водоемы, частично — просачиваются в землю и образуют подземные воды.
Скорость обновления воды
| Среда | Среднее время обновления |
| Океаны | 3200 лет |
| Ледники | От 5 до 10 лет |
| Снежный покров | От 2 до 6 месяцев |
| Почвенная корка | От 1 до 2 месяцев |
| Грунтовые воды: паводок | От 100 до 200 лет |
| Грунтовые воды: углубленные | 10000 лет |
| Озёра | От 15 до 17 лет |
| Реки | От 17 до 19 дней |
| Атмосфера | 10 дней |
Скорость переноса различных видов воды изменяется в широких пределах, так и периоды расходов, и периоды обновления воды также разные.
 Они изменяются от нескольких часов до нескольких десятков тысячелетий.
Они изменяются от нескольких часов до нескольких десятков тысячелетий.Атмосферная влага, которая образуется при испарении воды из океанов, морей и суши и существует в виде облаков, обновляется в среднем через восемь дней.
Воды, входящих в состав живых организмов, восстанавливаются в течение нескольких часов. Это наиболее активная форма водообмена.
Период обновления запасов воды в горных ледниках составляет около 1 600 лет, в ледниках полярных стран значительно больше — около 9 700 лет.
Полное обновление вод Мирового океана происходит примерно в 2 700 лет.
РИС.2 Круговорот воды в природе
Типы воды:
1. Мягкая и жёсткая вода — по содержанию катионов кальция и магния.
2. По изотопам молекулы:
а) лёгкая вода (по составу соответствует обычной).
б) тяжёлая вода (дейтериевая).
в) сверхтяжёлая вода (тритиевая).
3. Дождевая вода (одна из форм атмосферных осадков, влага, которая испаряется с поверхности почвы и различных водоемов.)
Дождевая вода (одна из форм атмосферных осадков, влага, которая испаряется с поверхности почвы и различных водоемов.)
4. Пресная вода (Пресной называют воду, в которой содержится не более 0,1 % соли. Она может находиться в виде жидкости, пары или льда. От общего количества водных ресурсов составляет 2,5—3 %.).
5. Морская вода (Солёность Мирового океана составляет в среднем 3,47 % (34,7 ‰), с колебаниями от 3,4 до 3,6 % (34-36 ‰). Это значит, что в каждом литре морской воды растворено 35 граммов солей (в основном хлорида натрия).
6. Минеральная вода (воды, добытые из водоносных горизонтов или водоносных комплексов, защищённых от антропогенного воздействия, сохраняющих естественный химический состав и относящиеся к пищевым продуктам, а при повышенной минерализации или при повышенном содержании определённых биологически активных компонентов).
7. Солоноватая вода (вода с концентрацией солей до 10 г/л.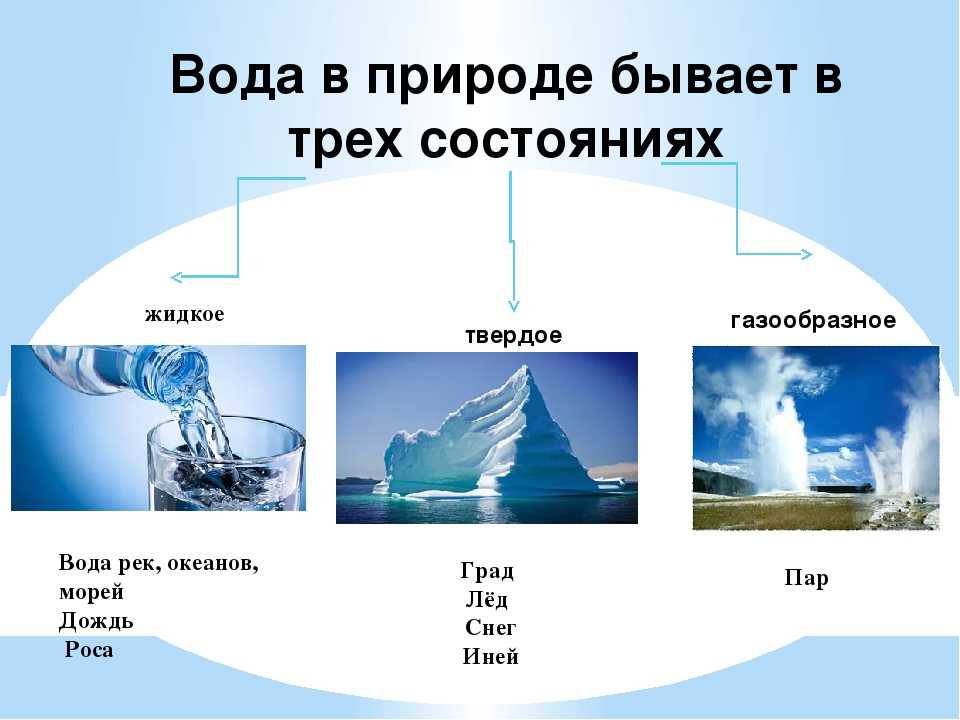 ).
).
8. Питьевая, водопроводная вода (вода, которая предназначена для ежедневного неограниченного и безопасного потребления человеком и другими живыми существами).
9. Дистиллированная вода
(очищенная вода, практически не содержащая примесей и посторонних включений).10. Сточные воды (К сточным водам относятся любые воды, а также те, что образовались вследствие атмосферных осадков (дождевые, талые), которые отводятся с территорий городов, поселков и промышленных предприятий в водоемы самотеком или через канализационную систему, имеющие свойства, ухудшенные в результате человеческой жизнедеятельности).
11. Ливневая вода, поверхностные воды (дождевые, талые, поливомоечные воды, поступающие в системы водоотведения с территорий поселений, объектов хозяйственной и иной деятельности).
12. Поливода (гипотетическая полимеризованная форма воды, которая может образоваться за счёт поверхностных явлений и обладать уникальными физическими свойствами.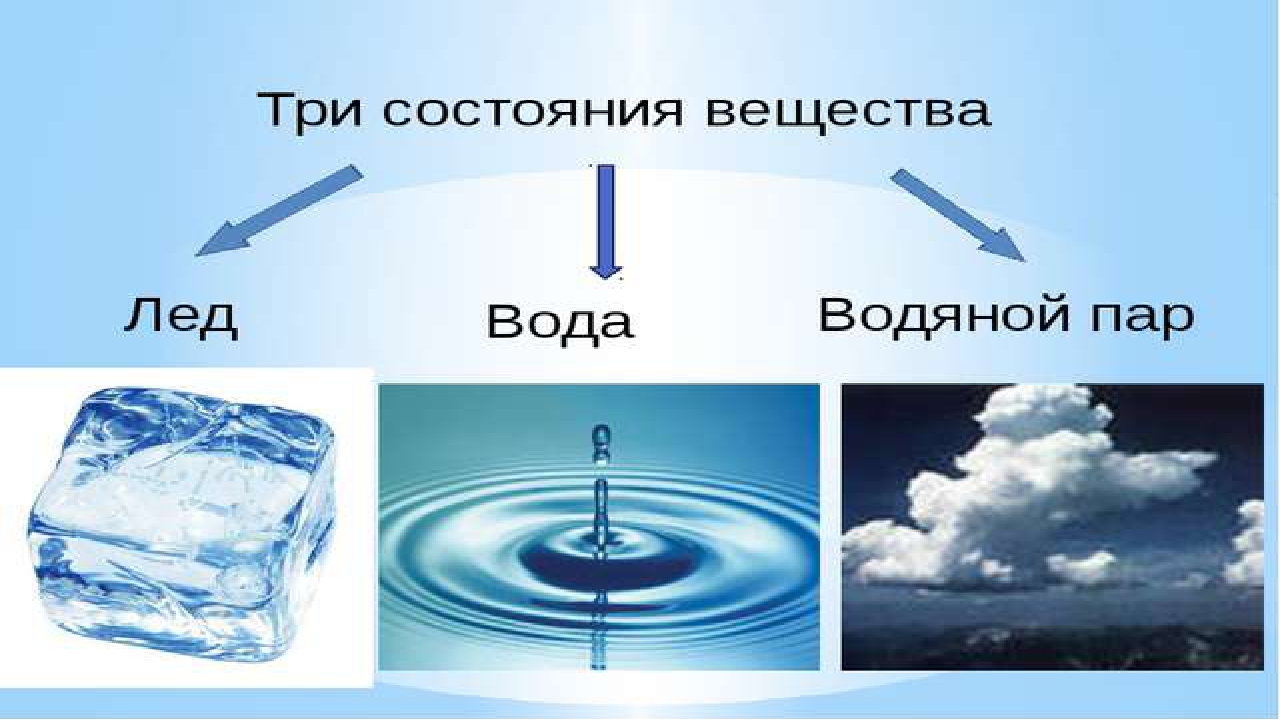 Активное изучение феномена «поливоды» происходило в 1960-х — начале 1970-х годов).
Активное изучение феномена «поливоды» происходило в 1960-х — начале 1970-х годов).
13. Талая вода (чистая высококачественная вода, которая вовсе не имеет или имеет в себе минимальное количество тяжелой или дейтериевой воды, не содержит хлориды, соли, вредные вещества и соединения).
Свойства воды
1. Диполь (Диполь молекулы воды характеризуется дипольным моментом, т. е. вектором, направленным от отрицательного к положительному заряду. Он равен произведению зарядов на расстояние между ними).
2. Высокое поверхностное натяжение (Поверхностное натяжение обуславливает капиллярные явления, собирает воду в капли, создаёт поверхностную плёнку и позволяет некоторым насекомым перемещаться по ней. Высокая полярность молекул обуславливает способность воды растворять вещества с ионной или ковалентной полярной связью).
3. Растворитель (Каждая молекула растворяемого вещества окружается молекулами воды, причём положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода, а отрицательно заряженные — атомы водорода.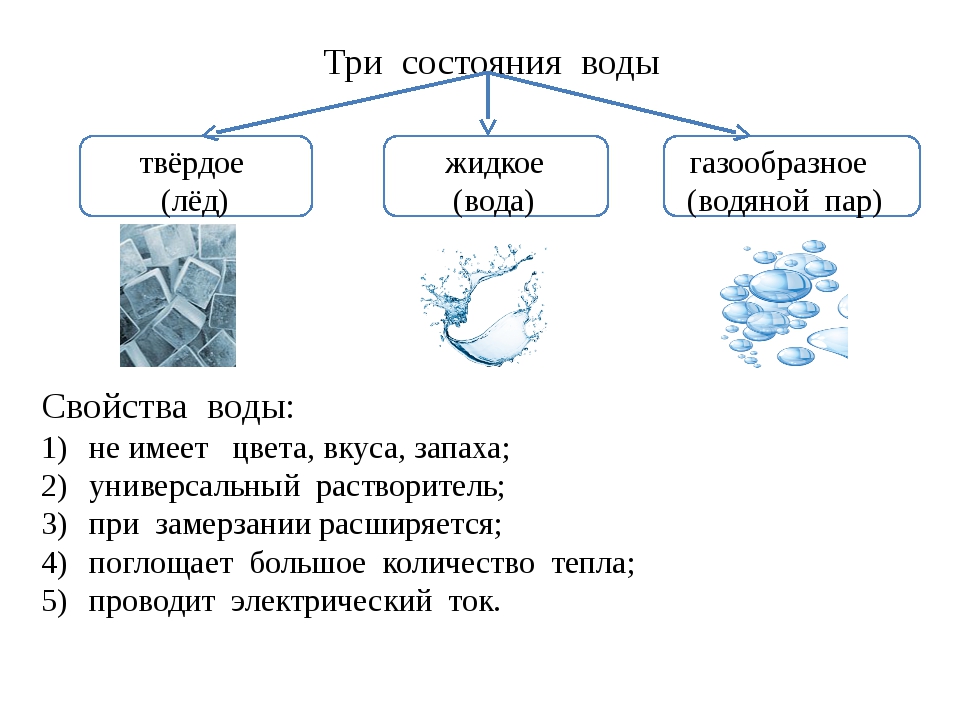 Поскольку молекула воды мала по размерам, много молекул воды могут окружить каждую молекулу растворяемого вещества).
Поскольку молекула воды мала по размерам, много молекул воды могут окружить каждую молекулу растворяемого вещества).
4. Высокая вязкость (Динамическая вязкость воды выше, чем у сопоставимых, не связанных водородом жидкостей. Более того, зависимость вязкости от давления аномальна: вязкость уменьшается с давлением и достигает минимума около 60 МПа (это давление эквивалентно толще воды в 6 км).
5. Большая теплоёмкость (Это значит, что существенное увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение ее температуры).
6. Электропроводность (Электрическая проводимость природной воды зависит в основном от степени минерализации и температуры).
7. Радиоактивность (Вода может нести радиоактивные вещества в растворимых и нерастворимых частицах. Частицы могут включать в себя полезные ископаемые в воде, или посторонние предметы, оказавшиеся в воде случайно).
Твёрдое агрегатное состояние воды
Твёрдое агрегатное состояние воды — это либо лёд либо снег.
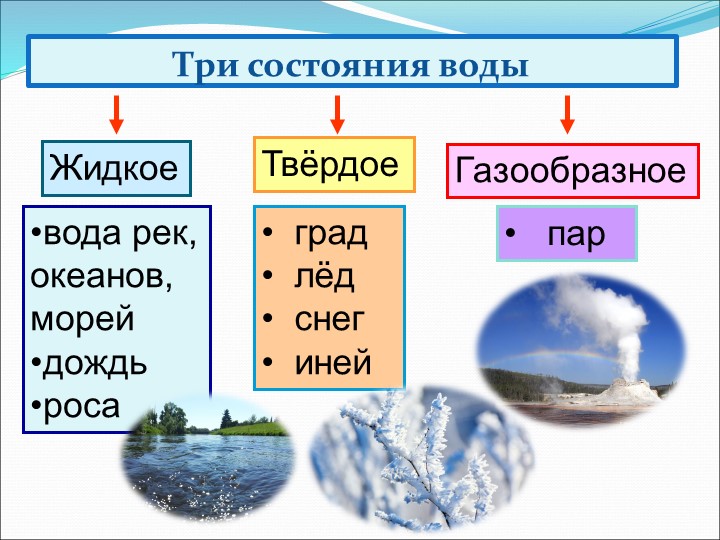 Но есть и некоторые ассоциации, касаемые тому, к какому агрегатному состоянию относится иней — а иней- это твёрдое агрегатное состояние, так как это мелкая ледяная крошка либо замёрзшие капли росы.
Но есть и некоторые ассоциации, касаемые тому, к какому агрегатному состоянию относится иней — а иней- это твёрдое агрегатное состояние, так как это мелкая ледяная крошка либо замёрзшие капли росы.При замерзании воды, её молекулы начинают отодвигаться дальше друг от друга, при этом делая лёд менее плотным, чем жидкость, т.е. получается, что вода в твёрдом агрегатном состоянии занимает больший объём, нежели в жидком.
Исходя из закона известного физика Даниила Бернулли «большинство испытываемых веществ при снижении температурного режима начинают сжиматься, а вода — начинает расширяться, в чём заключается её уникальная особенность».
Процесс замерзания воды — это происходящий процесс при значении температурного параметра в по шкале Цельсия (273, 15 К — по шкале Кельвина), т.е. вода кристаллизуется и переходит из жидкого состояния в твёрдое. Есть один фактор, влияющий на температуру замерзания воды — это содержание и наличие солей в составе кристаллической решётки.
Есть интересный вопрос, который зачастую встречается в олимпиадных заданиях по физике: «Назовите металл, который находясь в жидком агрегатном состоянии (т.е. находясь в расплавленном состоянии) может заморозить воду ?».
Единственным ответом на данный вопрос является следующий факт: такой металл как ртуть начинает плавиться при температурном значении. Исходя из этого, следует, что ртуть при температуре от — 38 до 0 градусов по шкале Цельсия способна заморозить воду, при это забирая у неё накопленное тепло.
Самое распространенное состояние воды на нашей планеты в отличие от остальных — это всех пресноводных запасов воды, которые в большей степени находятся в замороженном виде, так как около 11 % — это площадь, занимаемая ледниками на нашей планете.
Жидкое агрегатное состояние воды может перейти в твёрдое при температуре порядка по шкале Цельсия, то морская вода (имея среднюю плотность около 1030, так называемой средней солёности может замерзать при температуре около по шкале Цельсия.
В таком виде вода, в данном случае лёд, сохраняет свою форму и объём. Под воздействием температуры вода начинает менять состояние и превращаться в лёд, т.е. замерзать. Различают два вида твердого состояния воды — это аморфное и кристаллическое. При аморфном состоянии атомы вещества хаотичны, а при кристаллическом — наоборот упорядочены.
Жидкое агрегатное состояние воды
Изредвля веков каждый знает, что в привычном обиходе для каждого живого организма вода представлена в жидком агрегатном состоянии, которая встречается чаще всего в реках, озёрах, морях и океанах. Факт единственный — это то, что атмосферные облака состоят из мельчайших кристаллов воды и льда, что является самым частым явлением — это дождь.
Дело в том, что вода в жидком агрегатном состоянии может с лёгкостью проходить в почвенный покрой, при этом образуя подземные водные горизонты, именно благодаря которым выводится основная масса питьевой воды для существования жизни на нашей планете.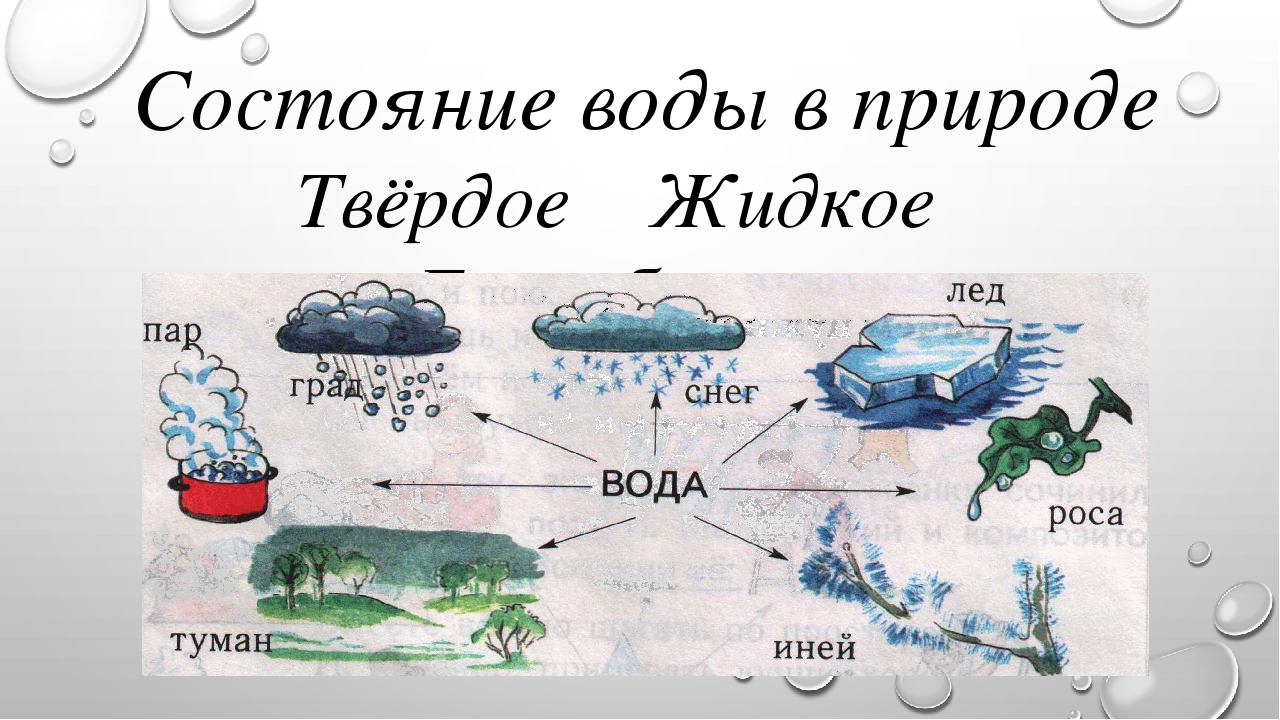
Вода в жидком агрегатном состоянии может отличаться единственным своим свойством — это высокая прилипчивость к различной твёрдой материи или поверхности. Сама по себе вода не может быть «влажной», но по своим свойствам очень легко может сделать «влажными» большое количество твёрдых материалов.
Вода из жидкого агрегатного состояния с лёгкостью может перейти в твёрдое и даже газообразное состояние, так как всё зависит от одного параметра — это температура. Но не стоит забывать о том, что не мало важную роль играет также самый важный параметр жизни всего и всех — это «Давление».
Что такое «Испарение ?» — это по сути переход от жидкого агрегатного состояния в газообразное. А тогда, такой вопрос — «Как вода может превратиться в пар?». Исходя из простых наблюдений, при кипячении воды именно она начинает превращаться в водяной пар, т.е. это уже жидкое состояние воды — иными словами скопление её микроскопических капелек.
Что такое «Пар — это по сути вода в газообразном состоянии, когда по сути вода либо кипит либо испаряется». Настоящий пар, он по сути невидим человеческому глазу.
И тут всплывает такое понятие, как «Точка росы». Это температура воздуха, которая меняется в зависимости от давления и влажности, ниже которой водный пар начинает конденсироваться в водяные капли и образуется роса. Т.е. агрегатное состояние воды из газообразного состояния меняется на жидкое. Закипает жидкая пресная вода при 100°C (градусах Цельсия) или 212°F (градусах Фаренгейта), в условиях нормального атмосферного давления. Чем ниже давление (например, в горах), тем выше температура кипения.
Газообразное агрегатное состояние воды
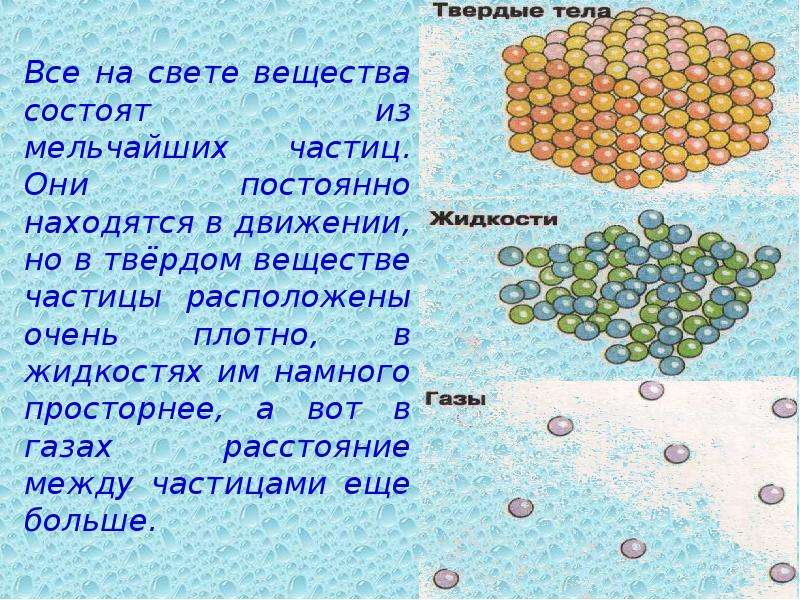
Особенностью воды является то, что ее молекулы способны при колебании температуры изменять характер связи друг с другом. Основные свойства ее при этом не меняются. Если нагревать воду, ее молекулы начинают двигаться быстрее.
Т.е. молекулы, которые соприкасаются с воздухом, разрывают свои связи и смешиваются с его молекулами.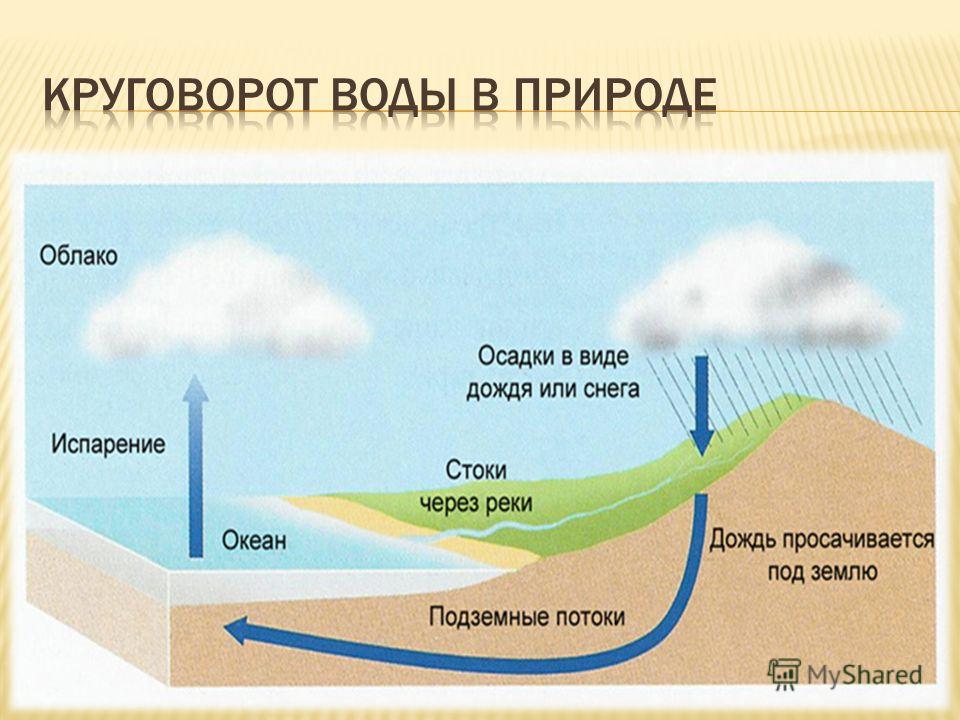 Вода в газообразном состоянии сохраняет все свои качества, но приобретает также свойства газа. Ее частицы находятся на большом расстоянии друг от друга и интенсивно двигаются. Чаще всего такое состояние называют водяным паром.
Вода в газообразном состоянии сохраняет все свои качества, но приобретает также свойства газа. Ее частицы находятся на большом расстоянии друг от друга и интенсивно двигаются. Чаще всего такое состояние называют водяным паром.
Это бесцветный прозрачный газ, который при определенных условиях опять превратится в воду. Он повсеместно распространен на Земле, но чаще всего его не видно. Примеры воды в газообразном состоянии — это облака, туман или водяной пар, образующийся при кипении жидкости. Кроме того, она везде находится в составе воздуха. Ученые заметили, что при его увлажнении дышать становится легче.
Чаще всего вода переходит в газообразное состояние при изменении температуры. Обычный пар, который всем знаком, образуется при кипении. Именно это беловатое горячее облако мы и называем водяным паром. Когда жидкость при нагревании достигает точки кипения, а при обычном давлении это происходит при 100°, молекулы ее начинают интенсивно испаряться. Попадая на более холодные предметы, они конденсируются в виде капелек воды.
Если нагревается большое количество жидкости, то в воздухе образуется насыщенный пар. Это состояние, когда газ и вода сосуществуют, потому что скорость испарения и конденсации одинакова. В том случае, когда в воздухе присутствует много водяного пара, говорят о его повышенной влажности. При понижении температуры такой воздух интенсивно конденсирует влагу в виде капелек росы или тумана. Но для образования тумана мало особых условий температуры и влажности.
Нужно, чтобы в воздухе находилось определенное количество пылинок, вокруг которых и конденсируется влага. Поэтому в городах туманы из-за пыли образуются чаще.
Процесс образования пара называется парообразованием. Его наблюдает каждая женщина при приготовлении пищи. Но существует и обратный процесс, когда газ превращается обратно в воду, оседая на предметах в виде мельчайших капелек. Это называется конденсацией. Каким же образом чаще всего происходит парообразование?
В естественных условиях этот процесс называется испарением. Вода испаряется постоянно под воздействием солнечного тепла или ветра. Искусственно образование пара можно вызвать с помощью кипения воды.
Вода испаряется постоянно под воздействием солнечного тепла или ветра. Искусственно образование пара можно вызвать с помощью кипения воды.
Это процесс, когда получается газообразное состояние воды. Он может быть естественным или ускоренным с помощью различных приспособлений. Испаряется вода постоянно.
Это ее свойство люди издавна использовали для просушки белья, посуды, дров или зерна. Любой мокрый предмет постепенно высыхает благодаря испарению влаги с его поверхности. Молекулы воды в своем движении одна за другой отрываются и смешиваются с молекулами воздуха.
Фазовые переходы
Под действием температуры и определенных внешних воздействий вода меняет свое состояние, происходит фазовый переход воды из одного состояния в другое. К фазовым переходам воды относятся такие процессы, как:
1. Лёд-вода, иначе процесс плавления, при котором происходит переход вещества из твердого состояния в жидкое.
2. Вода-лёд, это процесс замерзания (кристаллизации) — жидкое вещество переходит в твердое. Рассмотрим процесс кристаллизации, он возможен, когда понижается температура. Когда молекулы теряют свое теплоту, то становятся менее подвижны, так как им не хватает энергии. Например, мы контейнер с водой поставили в морозильную камеру холодильника, и вода превратится в лед.
Рассмотрим процесс кристаллизации, он возможен, когда понижается температура. Когда молекулы теряют свое теплоту, то становятся менее подвижны, так как им не хватает энергии. Например, мы контейнер с водой поставили в морозильную камеру холодильника, и вода превратится в лед.
3. Вода-пар (газо/парообразование), пар-вода (конденсация). По мере того, как происходит увеличения температуры воды, ускоряется испарение, и как вода достигнет температуры 100*С, она начинает закипать, в таком состоянии она больше не может принимать энергию не изменив свое состояние, в итоге происходит испарение. Кипение — это интенсивный процесс перехода воды в пар, а конденсация это процесс обратный. При конденсации же, процесс происходит наоборот, выделяется небольшое количество тепла в окружающую среду, и ее температура немного повышается.
4. Лёд-пар (минуя состояние воды), такой процесс получил название сублимация примером сублимации может послужить эксперимент с мокрой рубашкой, вывешенной на мороз — лед исчезнет с рубахи, превратившись в пар.
5. Пар — лед, в итоге мы имеем десублимацию. При этом процессе выделяется энергия. Примером может послужить морозный узор на стеклах.
6. Газ-плазма. Для этого необходимо ионизировать газ. Степень ионизации зависит от количества атомов и от температуры.
Заключение
Вода — это и строительный материал, который используется для создания всего живого, и среда, в которой протекают все жизненные процессы, и растворитель, выносящий из организма вредные для него вещества, и уникальный транспорт, снабжающий биологические структуры всем необходимым для нормального протекания в них сложнейших физико-химических процессов.
И это всеобъемлющее влияние воды на любую живую структуру может быть не только положительным, но и отрицательным. В зависимости от своего состояния вода может быть как созидателем цветущей жизни, так и ее разрушителем, могильщиком — всё зависит от ее химического и изотопного состава, структурных, биоэнергетических свойств. Не случайно академик И.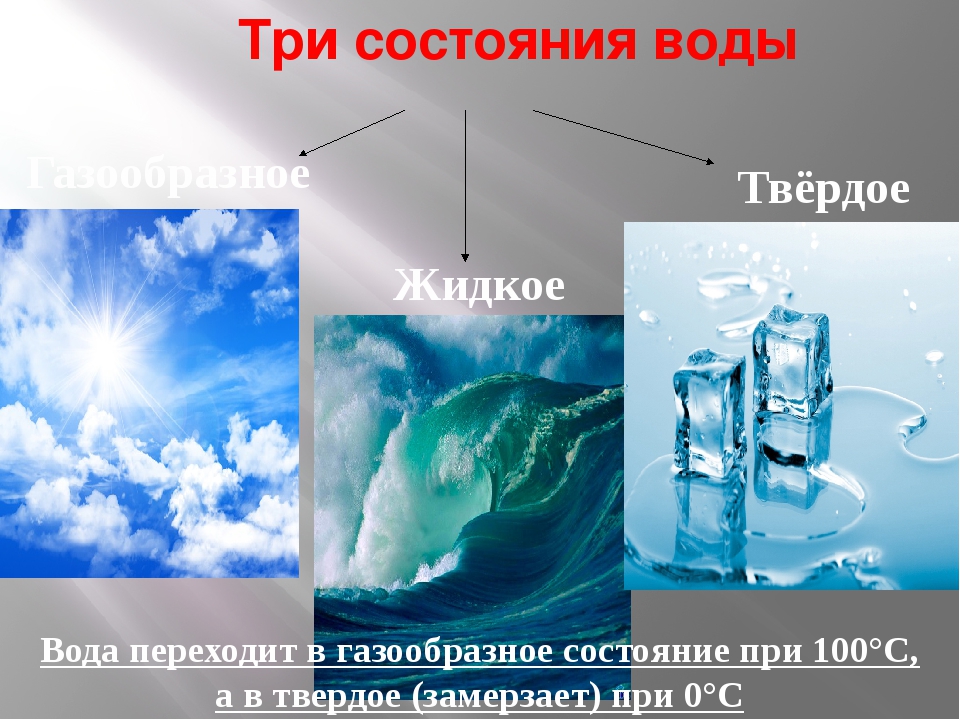 В. Петрянов сказал: «Вода — это подлинное чудо природы!». Учёные абсолютно правы: нет на Земле вещества, более важного для нас, чем обыкновенная вода, и в тоже время не существует другого такого вещества, в свойствах которого было бы столько противоречий и аномалий, сколько в её свойствах.
В. Петрянов сказал: «Вода — это подлинное чудо природы!». Учёные абсолютно правы: нет на Земле вещества, более важного для нас, чем обыкновенная вода, и в тоже время не существует другого такого вещества, в свойствах которого было бы столько противоречий и аномалий, сколько в её свойствах.
«Что такое вода ?» — вопрос далеко не простой. Все, о чем было рассказано о ней в данной работе не является исчерпывающим ответом на этот вопрос, а во многих случаях дать ясный ответ на него пока и совсем нельзя. Например, пока остается открытым вопрос о структуре воды, причинах многочисленных аномалий воды и, вероятно, еще о многих свойствах и разновидностях воды, о которых мы даже не подозреваем. Однозначно можно сказать лишь то, что вода — самое уникальное вещество на земле.
Напомним слова нашего гениального соотечественника акад. В. И. Вернадского о том, о «надо ждать особый исключительный характер физико-химических свойств воды среди всех других соединений, который отражается и на ее положении в мироздании и на структуре мироздания».
Список использованной литературы
- Андреев Ю. А. Три кита здоровья. — СПб., Диамант. 1996.
- Грейсер Е.Л., Иванова Н.Г. Пресные подземные воды: состояние и перспективы водоснабжения населенных пунктов и промышленных объектов. // Разведка и охрана недр. 2005 Вып. 5. С. 36-42.
- Залманов А. С. Тайная мудрость человеческого организма. — М., Наука. 1991.
- Зенин С.В. Структурное состояние воды как показатель ее качества. //«Стандартсервис» Информ. сборник 2004. № 5.
- Масару Эмото Послание воды. М, ООО Издательство «София». 2006.
- Мосин О. В. Химическая природа воды и её память. //«Стандартсервис» Информ.сборник 2008. № 3.
- Неумывакин И. П. Вода – жизнь и здоровье: мифы и реальность. Издательство: Диля. 2015.
- Яхнин Э. Я., Томилин А. М., Шелемотов А. С. Оценка качества и химический состав подземной воды дочетвертичных отложений Ленинградской области // Разведка и охрана недр. 2005. Вып.
 5, С. 42-48.
5, С. 42-48. - National Research Council // Drinking Water and Health. Washington, 1977. Vol. 7.
- Fletcher N. H., The chemical physics of ice, Camb., 1970.
Если страница Вам понравилась, поделитесь в социальных сетях:
Превращения и круговорот воды. Урок 12. 3 класс
иНикифорова Н.В.
Работа по учебнику.
1.Откройте учебник на стр.55.
2.Прочитайте текст «Три
состояния воды ».
Никифорова Н.В.
Три состояния воды.
жидкое
твёрдое
Вода в реках,
озёрах, морях,
лужах, дожди,
роса
Снег , лёд ,
иней, град
Никифорова Н.В.
газообразное
Пар , облака,
туман
Агрегатное состояние воды.
жидкое
твёрдое
Вода в жидком
состоянии
Лёд
Никифорова Н.В.
газообразное
Пар
В природе вода постоянно испаряется с
поверхности морей, рек, озёр, почвы. Поэтому
в воздухе всегда содержится невидимый
водяной пар.
Никифорова Н.
 В.
В.Работа по учебнику.
1.Откройте учебник на
стр.56-57.
2.Прочитайте текст
«Круговорот воды»
Никифорова Н.В.
Солнечные лучи нагревают поверхность нашей
планеты.
Никифорова Н.В.
С поверхности водоёмов и почвы вода в виде
пара поднимается вверх.
Никифорова Н.В.
Пар охлаждается там и образует множество
водяных капелек или крошечных льдинок. Из
Никифорова Н.В.
них образуются облака.
Облака очень лёгкие, и ветер переносит их
порой на очень большие расстояния.
Никифорова Н.В.
Из облаков вода возвращается на землю в виде
дождя ,снега или града .
Никифорова Н.В.
Вот она снова оказалась на земле, под землёй,
но уже в другом месте.
Никифорова Н.В.
Вода снова возвращается к нам, превращается в пар,
поднимается вверх и так повторяется всё снова.
Никифорова Н.В.
Это вечное движение называется
круговорот воды в природе.
Никифорова Н.В.
Никифорова Н.В.
Рамка
Учебник
Круговорот
Река Лёд Пар
Состояния воды
Туман
Поверхность
Солнце Облака Пар Дождь
Круговая стрелка
Отрисовки муравья и черепахи авторские
Поурочные разработки по курсу
«Окружающий мир» Н.
 Ю.Васильева
Ю.Васильевадля 3 класса
Никифорова Н.В.
ГДЗ 3 класс. Окружающий мир. Плешаков. Рабочая тетрадь. Часть 1. Страницы 33, 34
Ответы к страницам 33 и 34
содержание
Другие решебники 3 класс:Превращения и круговорот воды
1. Наш неутомимый Попугай снова составил кроссворд. Все слова в нём — вода. Как она любит загадочные превращения! Угадаешь ли ты все её «маски»?
ПАР
ЛЁД
ДОЖДЬ
ОБЛАКО
КАПЛЯ
СНЕЖИНКА
ТУМАН
ТУЧА
2. Самостоятельно или с помощью учебника заполни таблицу.
Три состояния воды
| Примеры | Состояние воды |
| Вода в реке, роса | жидкое |
| Лёд, снег | твердое |
| Водяной пар | газообразное |
3. Изобразите с помощью схематического рисунка испарение воды. (Частицы воды обозначайте кружочками.)
Изобразите с помощью схематического рисунка испарение воды. (Частицы воды обозначайте кружочками.)
Посмотрите, что нарисовали другие ребята. Сравните рисунки. Все ли они верные? Какой самый удачный? Расскажите по схематическому рисунку о том, как происходит испарение воды.
4. Нарисуй схему круговорота воды в природе. Сначала выполни рисунок простым карандашом. Проверь себя по учебнику. После проверки можно раскрасить схему. Расскажи по ней о круговороте воды в природе.
Круговорот воды в природе
5. Мудрая Черепаха приглашает тебя на мини-экзамен. Верны ли эти утверждения? Обведи «Да» или «Нет».
| 1. Вода встречается в природе в трёх состояниях: жидком, твёрдом и газообразном. | Да Нет |
| 2. Вода превращается в лёд при температуре +10°С. | Да Нет |
3. Лёд и снег — вода в твёрдом состоянии. Лёд и снег — вода в твёрдом состоянии. | Да Нет |
| 4. При превращении в лёд вода сжимается. | Да Нет |
| 5. Водяной пар — вода в газообразном состоянии. | Да Нет |
- ← предыдущее
- следующее →
Руководство по обучению детей состояниям материи
Многие из нас испытали это экзистенциальное «вау, наука!» момент взрослой жизни.
Возможно, это произошло во время наблюдения за таянием кубика льда на солнце. Внезапно до нас доходит, что лед на самом деле состоит из кристаллических молекул воды, что они поглощают свет звезды, находящейся на расстоянии 93 миллионов миль, и это заставляет их взволнованно покачиваться, пока они не соскользнут с кубика льда. Колосс научных знаний, стоящий даже за этим простым процессом, может быть ошеломляющим, если только он поймает нас в правильном настроении.
Но вот более сложный вопрос — как передать это чудо детям так, чтобы они вдохновились и увлеклись?
Наука увлекательна, интересна и чрезвычайно полезна для будущего детей. Самое главное, понимание его принципов позволяет им взаимодействовать с окружающим миром, критически размышляя обо всем, что они видят — буквально обо всем, что они видят . Почему лужи воды замерзают по утрам? Почему кипящая вода образует пар? Почему по утрам над руслами рек парит туман?
Давайте рассмотрим лучшие способы научить детей состояниям материи, одной из самых применимых и вездесущих научных концепций в их жизни.
Начните со строительных блоков материи
Одна из величайших особенностей этого предмета заключается в том, что природа демонстрирует его нам везде, куда бы мы ни посмотрели. Состояния материи начинаются с атомов и молекул.
атом является основным строительным блоком природы. Это частица в 1 миллион раз меньше пылинки, а значит, ее невозможно увидеть. Вы можете понять маленький размер атома, спросив детей, сколько атомов, по их мнению, содержится в одной крупице соли.Ответ: 1 200 000 000 000 000 000 — это 1,2 квинтиллиона.
Вы можете понять маленький размер атома, спросив детей, сколько атомов, по их мнению, содержится в одной крупице соли.Ответ: 1 200 000 000 000 000 000 — это 1,2 квинтиллиона.
Молекула , с другой стороны, возникает, когда два или более атома соединяются вместе. Этот небольшой кластер атомов образует совершенно новое вещество. Например, в то время как золото состоит из отдельных атомов, упакованных вместе, вода состоит из молекул. В частности, вода состоит из двух атомов водорода, связанных с одним атомом кислорода.
Атомы и молекулы часто связаны друг с другом, то есть между ними существуют силы притяжения, которые заставляют их слипаться.Вот почему вода образует шарики, а не растекается.
Есть масса забавных фактов об атомах. Если вы ищете способы вызвать у детей чувство удивления атомами и молекулами, расскажите эти факты в своих разговорах:
- Атомы состоят из 2 частей: ядра, состоящего из протонов и нейтронов, и электронов, вращающихся вокруг него.
 Хотя на самом деле это немного сложнее, вы можете проиллюстрировать это, сравнив его с планетами, вращающимися вокруг Солнца.
Хотя на самом деле это немного сложнее, вы можете проиллюстрировать это, сравнив его с планетами, вращающимися вокруг Солнца. - Большая часть атома — это пустое пространство.Если бы один атом был размером с футбольный стадион, ядро было бы прямо в центре поля и было бы размером с горошину. Это означает, что твердая толщина всего вокруг вас — иллюзия — это в основном пустое пространство.
- Если бы атом был больше — скажем, если бы он был размером с точку в конце предложения, — то человек, лежащий на спине, растянулся бы от Далласа, штат Техас, до Лос-Анджелеса, штат Калифорния.
- «Атом» происходит от древнегреческого термина «неразрезаемый».Греки полагали, что можно взять кусок материи и продолжать резать его пополам до тех пор, пока станет невозможно сделать его еще меньше. Этот самый маленький кусочек был тем, что они назвали «атомом».
- В вашем теле около 7 миллиардов миллиардов миллиардов атомов. Во время еды, питья и дыхания вы заменяете 98% этих атомов каждый год.

- Если ребенку трудно понять, что такое миллиард, покажите ему наглядное изображение 7 миллиардов человек. Это приблизительная численность населения Земли, которая дает представление о том, насколько велики эти цифры.
Технически существует 5 состояний материи, но большинству людей нужно знать только 3. Вот они:
1. Твердые вещества
Материал в твердом состоянии сохраняет свою форму и форму. значит не течет. Твердые тела могут быть разных цветов, могут иметь различную твердость и иметь различные формы. Тот факт, что объект является твердым, не означает, что его нельзя сплющить или отформовать — это означает, что если оставить его нетронутым, материал не будет течь.
Примеры твердых объектов:
- Полы
- Карандаши
- Деревья
- Автомобили
- Кожа
- Книги
- Лед
- Стулья
- Компьютеры
Существует много твердых материалов, которые можно прессовать и формовать, например, глину, пластилин Play-Doh, подушки, ткань и одежду. Хотя эта последняя группа меняет форму, когда мы надавливаем и сжимаем ее, это не означает, что она не твердая. Если вы оставите его на столе в умеренно прохладной комнате, он будет иметь ту же форму, когда вы вернетесь к нему позже, как и когда вы его оставили.
Хотя эта последняя группа меняет форму, когда мы надавливаем и сжимаем ее, это не означает, что она не твердая. Если вы оставите его на столе в умеренно прохладной комнате, он будет иметь ту же форму, когда вы вернетесь к нему позже, как и когда вы его оставили.
Давайте подумаем, как это относится к атомам и молекулам. В твердом теле атомы и молекулы тесно связаны друг с другом, что делает их жесткими и жесткими. Это фактически означает, что они застыли на месте и не обтекают друг друга. Эта жесткость возникает из-за того, что связи между атомами или молекулами прочны и удерживают их вместе.
2. Жидкости
Жидкость принимает форму сосуда. Это означает, что если вы нальете его в миску, он заполнит миску снизу вверх и остановится.Представьте себе разницу между тем, чтобы положить большой кусок льда в миску и налить в нее такое же количество воды. Лед твердый и будет держать форму, а вода заполнит чашу.
Жидкости могут иметь различную густоту, известную как «вязкость». Например, тесто для блинов гуще — оно более вязкое — чем вода и течет медленнее. Примеры жидкостей:
Например, тесто для блинов гуще — оно более вязкое — чем вода и течет медленнее. Примеры жидкостей:
- Вода
- Сок
- Масло
- Кровь
- Кофе
- Бензин
Ртуть является примером металла, который также является жидкостью.
Чтобы лучше понять вязкость, представьте, что вы просыпаетесь холодным утром. Вы точно не сбросите одеяло и не выпрыгнете из кровати. Скорее, вы тянете крышки выше и медленно двигаетесь. Многие жидкости реагируют на холод одинаково — чем они холоднее, тем медленнее они движутся. Это относится к таким веществам, как сироп, масло и жидкое мыло для ванн. Обратите внимание, что вода не реагирует таким же образом, но, как мы увидим, вода — это странное вещество.
Атомы и молекулы в жидкостях расположены дальше друг от друга, чем в твердых телах, что дает им свободу передвижения и уменьшает связь между отдельными атомами.В жидком состоянии атомы и молекулы находятся достаточно далеко друг от друга, чтобы обтекать друг друга, но не так далеко, чтобы оказаться в конечном состоянии материи — газе.
3. Газы
Газ — это вещество, которое ведет себя как воздух вокруг нас. Газы также принимают форму своего сосуда, но они намного легче жидкостей. Это означает, что они расширятся, чтобы заполнить любой контейнер, в который они помещены. Если вы нальете воду в стеклянный аквариум, вода заполнит контейнер снизу вверх.Если бы вы сделали то же самое с газом, он расширился бы, чтобы заполнить все части стеклянного аквариума, а не только дно.
Перемещаться через газы нетрудно, и если они вырвутся из контейнера, то быстро распространяются по окружающему воздуху. Вы не можете измерить количество газа с помощью весов или мерного стакана. Чтобы понять это, вы должны использовать математику. Примеры газов включают:
- Воздух
- Пар из кипящей воды
- Дым из дымовых труб
- Выхлоп автомобилей
Внутри газа атомы и молекулы находятся далеко друг от друга и движутся независимо друг от друга. Они не обтекают друг друга, как в жидкости, а свободно отталкиваются друг от друга во всех направлениях.
Они не обтекают друг друга, как в жидкости, а свободно отталкиваются друг от друга во всех направлениях.
Теперь, когда мы рассмотрели 3 состояния материи, пришло время обсудить явление, которое мы можем наблюдать в повседневной жизни. Это смена состояний или тенденция материи переходить из твердого состояния в жидкое и газообразное.
Мы видим это все время — масло тает на горячих тостах, лед тает, превращаясь в воду, вода закипает, образуя пар, капельки воды конденсируются на холодных поверхностях или испаряется пот.По нашему повседневному опыту, наиболее распространенной причиной изменения состояния форматера является температура. Вещество в твердой форме холоднее, чем такое же вещество в жидкой форме, которое холоднее, чем его газообразная форма.
Давайте посмотрим на некоторые изменения, происходящие между состояниями материи.
1. Изменения между твердым и жидким состояниями
Чтобы понять переход между твердым и жидким состояниями, полезно попробовать для себя очень вкусный пример: масло, тающее на кусочке горячего тоста. Масло довольно твердое, когда достают из холодильника. Однако, когда вы кладете его кусочек на тост, только что вынутый из тостера, он начинает размягчаться и превращаться в жидкость, что облегчает его намазывание.
Масло довольно твердое, когда достают из холодильника. Однако, когда вы кладете его кусочек на тост, только что вынутый из тостера, он начинает размягчаться и превращаться в жидкость, что облегчает его намазывание.
Давайте теперь увеличим изображение атомов и молекул, из которых состоит масло. Когда они выходят из холодильника, они сбиваются в кучу и становятся холодными и жесткими. Затем гигантский нож скользит внутрь и сметает целую часть их, только чтобы шлепнуть их на горячий кусок хлеба.Тепло от этого хлеба распространяется на масло. Он рассеивается среди молекул, нагревая их и заставляя отдаляться от своих соседей.
В конце концов, они находятся достаточно далеко друг от друга, чтобы начать обтекать друг друга. Если уменьшить масштаб, это жидкая стадия масла. Поскольку холодное масло поглощало больше энергии в виде тепла, его молекулы начинали раскачиваться и могли двигаться свободнее.
Прежде чем мы двинемся дальше, давайте рассмотрим обратный процесс в эксперименте с переходом жидкости в твердое состояние. Представьте себе миску с растопленным маслом, поставленную в холодильник. Мы знаем, что молекулы масла свободно обтекают друг друга в жидкой форме, потому что у них достаточно тепла для этого. Но по мере того, как морозильник отбирает тепло масла, молекулы внутри него начинают слипаться и замедляться. В конце концов, они застынут и образуют твердое тело.
Представьте себе миску с растопленным маслом, поставленную в холодильник. Мы знаем, что молекулы масла свободно обтекают друг друга в жидкой форме, потому что у них достаточно тепла для этого. Но по мере того, как морозильник отбирает тепло масла, молекулы внутри него начинают слипаться и замедляться. В конце концов, они застынут и образуют твердое тело.
2. Изменения между жидким и газообразным состояниями
Рассказывать детям о состоянии материи легче, когда у вас есть на что посмотреть.Попробуйте использовать эксперимент с переходом жидкости в газ, чтобы проиллюстрировать это изменение.
Вскипятить на плите кастрюлю с водой. Вы включаете циферблат и начинаете нагревать его. Это тепло переходит в воду через дно кастрюли, и в ответ молекулы воды начинают двигаться. Добавляется все больше и больше тепла. Они двигаются все больше и больше в ответ. Но как долго это может продолжаться? Будут ли они двигаться все быстрее и быстрее?
В определенный момент молекулы воды поглощают достаточно тепловой энергии , чтобы они превращались в газ. Это означает, что они двигаются так быстро, что поднимаются на поверхность воды и исчезают в окружающем воздухе. С нашей точки зрения снаружи это пар, поднимающийся из горшка с водой. Этот процесс в конечном итоге приводит к испарению.
Это означает, что они двигаются так быстро, что поднимаются на поверхность воды и исчезают в окружающем воздухе. С нашей точки зрения снаружи это пар, поднимающийся из горшка с водой. Этот процесс в конечном итоге приводит к испарению.
Обратной стороной испарения является конденсация. В воздухе вокруг вас всегда есть вода. Он испарился из рек, озер и океанов, из почвы и составляет большую часть нашей атмосферы. Эти молекулы воды находятся в газообразной форме, и хотя они не имеют температуры кипения, они достаточно легкие и достаточно далеко друг от друга, чтобы у них не было причин снова превращаться в жидкость.
Однако представьте, что у вас есть стакан холодного лимонада со льдом. Влажный воздух вокруг стекла, содержащий воду, соприкасается с холодным стеклом. Холод заставляет газообразную воду в воздухе «конденсироваться», то есть она собирается на стекле, потому что из него высосано тепло, пока ее не станет достаточно для образования жидкой воды. Эта жидкая вода собирается и образует капли, которые мы все называем конденсатом.
Стоит отметить, что вода, самая важная жидкость в нашей жизни, также, вероятно, является самым странным веществом, которое мы знаем.Ученые регулярно ломают голову над его причудливой тенденцией нарушать все правила. Вот несколько странных фактов о воде, которые вы, возможно, захотите упомянуть, объясняя детям состояние материи:
- Расширяется в холоде . Основное универсальное правило состоит в том, что вещества сжимаются или сжимаются при охлаждении. Вот почему мы ведем все эти разговоры об атомах и молекулах, «сжимающихся» вместе, когда они теряют свое тепло. Но вода расширяется при замерзании.Например, лед, замороженный в стакане, при таянии производит, по-видимому, меньшее количество воды в стакане.
- На его нагрев уходит много энергии . Вода может поглотить много тепла, прежде чем превратиться в газ — как боксер, который может выдержать много ударов, прежде чем проиграет бой.

- Может растворить практически все . Будучи такой питательной частью жизни, вода определенно имеет тенденцию разрывать вещи на части. Он может растворять сахар, соль и многие другие твердые вещества — больше, чем любая другая жидкость, известная человеку.
Поддержка научного образования вашего ребенка может открыть для него новые двери и помочь ему понять мир. Science Explorers предлагает веселые летние лагеря и кружки после школы, которые позволяют детям исследовать окружающий мир и взаимодействовать с ним. Это приводит к большей мотивации, пониманию, успеваемости в школе и общему интересу к окружающей среде.
Работа всей нашей жизни — сделать науку интересной для детей.По словам нашего владельца и основателя Юпитера Джен: «Если это не весело, мы этим не занимаемся». Эта программа идеально подходит для детей в возрасте от 4 до 11 лет, позволяя им заняться наукой и снять с нее клеймо как сложный предмет. Мы ориентируемся на практический формат с классными экспериментами, такими как вскрытия, химия, создание классных материалов, изучение органов, запуск ракет и многое другое. Свяжитесь с нами сегодня, чтобы узнать больше о наших программах.
Мы ориентируемся на практический формат с классными экспериментами, такими как вскрытия, химия, создание классных материалов, изучение органов, запуск ракет и многое другое. Свяжитесь с нами сегодня, чтобы узнать больше о наших программах.
15 креативных способов преподавания состояний материи
Понимание различных состояний материи является одним из ключевых понятий, необходимых детям для изучения химии и физики.Эти состояния активности материи помогают им изучить физические изменения, которые происходят, когда материя превращается из твердого состояния в жидкое и в газообразное. Им понравятся практические аспекты, когда они увидят науку в действии!
1. Начните с якорной диаграммы
Анкерная диаграмма, подобная этой, дает учащимся информацию, на которую они могут ссылаться, когда они изучают концепции и полные состояния деятельности материи.
Подробнее: Терра Палмер/Pinterest
2. Читайте книги о состояниях материи
Прочитайте одну или две книги, чтобы познакомить младших школьников с понятиями твердых тел, жидкостей и газов. Вот несколько наших фаворитов, которые стоит попробовать.
Вот несколько наших фаворитов, которые стоит попробовать.
3. Сортировать и сопоставлять состояния материи
Возьмите бесплатные карточки для печати по ссылке или вырежьте картинки из журналов. Затем попросите детей рассортировать их по состояниям вещества.
Подробнее: Дар Любопытства/Сортировка и сопоставление состояний материи
4. Откройте для себя состояния вещества с водой
Все, что вам нужно, это вода для одного из самых простых видов деятельности. Начните с кубиков льда, растопите их до состояния воды, затем доведите до кипения, чтобы наблюдать за образованием пара.
Узнать больше: Дар Любопытства/состояний материи с использованием воды
5. Раскрась и узнай о состояниях материи
Детям, которые любят раскрашивать, понравятся эти бесплатные рабочие листы для печати. По мере раскрашивания картинок расскажите о различиях между состояниями материи.
Подробнее: This Reading Mama
6. Используйте хлопья для представления атомов
Используйте хлопья Cheerios (или M&Ms, или изюм… вы поняли), чтобы составить схему действия атомов в различных состояниях материи.Перекусите «атомами», когда закончите!
Подробнее: Сокровища миссис Томпсон
7. Поплавки для питья корневого пива
Говоря о восхитительной науке, рутбир — одно из наших любимых занятий в состоянии материи! Мы гарантируем, что это будет хит.
Дополнительные сведения: Ресурсы учебной лаборатории
8. Взбивание мороженого в пакете
Если вы действительно настроены амбициозно, сделайте свое собственное мороженое для поплавков! Это также интересный способ исследовать переход от жидкого к твердому.
Подробнее: У костра
9. Сбор воды из тумана
Имитируйте туман, распыляя воду из бутылки. Используйте кусок нейлонового чулка, чтобы поймать туман и превратить его обратно в воду.
Используйте кусок нейлонового чулка, чтобы поймать туман и превратить его обратно в воду.
Подробнее: Научные друзья/Ловец тумана
10. Исследуйте жидкости и твердые тела мелками
В этом эксперименте исследуется переход от твердого состояния к жидкому и обратно с использованием тепла. И, наконец, у детей есть «новые» мелки для раскрашивания!
Узнать больше: Life Over Cs
11.Сделайте чашку горячего шоколада
Готовы к еще одному съедобному эксперименту? Горячий шоколад — отличный способ исследовать состояния материи. (Не забудьте твердые вещества: зефир!)
Узнать больше: Крутое потомство
12. Попробуйте рисовать ватной палочкой
С помощью ватных палочек, смоченных краской, изобразите движение атомов в твердых телах, жидкостях и газах.
Подробнее: Вдохнови меня как можно скорее
13.
 Приготовить партию сливочного масла
Приготовить партию сливочного маслаЭтот эксперимент исследует не только твердые тела и жидкости, но и процесс, известный как эмульсия.Вы получаете двойную науку и вкусное угощение!
Подробнее: Пластилин для Платона
14. Наполнение воздушных шаров твердыми веществами, жидкостями и газами
Наполните воздушные шары водой (жидкой и замороженной) и воздухом, затем расскажите о свойствах каждого из них. Это хороший способ доказать наличие газа, даже если вы не всегда можете его увидеть.
Подробнее: Детский клуб Fit
15. Исследуйте свойства Ублека
Как раз в тот момент, когда дети думают, что они понимают состояния материи, появляется неньютоновская жидкость, такая как ооблек, чтобы запутать дело! Это одна научная демонстрация, которая не перестает удивлять.
Подробнее: Научные друзья/Ублек
Нравится это состояние деятельности? Попробуйте эти 28 съедобных научных экспериментов, которые вы действительно захотите съесть.
Плюс, 50 простых научных экспериментов, которые дети могут проводить дома.
состояний материи | Давайте поговорим о науке
Химия помогает нам понять свойства и состав окружающего нас мира. Здесь вы узнаете о состояниях материи, а также многое об одном состоянии в частности (три догадки — ни твердое, ни жидкое…).
Состояние материи
В зависимости от температуры , давления и свойств вещества вещество может принимать различные физические формы. Мы называем эти физические формы состояниями материи . Существует три хорошо известных состояния вещества: Твердые тела , Жидкости и Газы . Существуют и другие состояния вещества. К ним относятся Плазма (состояние вещества, похожее на газ, но содержащее свободно движущиеся электроны и ионы — атомы, потерявшие электроны) и Конденсат Бозе-Эйнштейна (БЭК) (волны вещества, которые могут возникать с некоторыми типами атомов при сверхнизких температурах).
Силы между частицами и давление на частицы удерживают частицы вместе. Если мы разогреем вещество (добавим энергию), частицы начнут двигаться быстрее и будут стремиться разойтись. Это движение частиц оказывает большое влияние на состояние вещества.
Твердые вещества
В твердых телах силы, удерживающие частицы вместе, относительно сильны, и частицы остаются очень близко друг к другу. Частицы могут вибрировать, но они мало перемещаются.Вот почему твердые тела твердые и твердые. Оставленные сами по себе, твердые тела будут сохранять свою форму.
Жидкости
В жидкостях силы между частицами слабее, чем в твердых телах. Частицы все еще довольно близко друг к другу, но могут свободно перемещаться. Жидкости могут течь внутри контейнера и не имеют какой-либо определенной фиксированной формы.
Газы
С газами трудно установить связь, потому что они часто невидимы, но их можно найти повсюду. Их можно почувствовать, когда, например, дует ветер.Иногда вы можете почувствовать их запах, когда, например, чувствуете запах готовящейся еды или когда скунс расстроен. Некоторые газы важны для нашего здоровья (например, кислород), в то время как другие могут быть смертельными (например, сероводород и хлор). Перед операцией вам могут ввести анестезирующий газ, содержащий химические вещества, чтобы облегчить боль и лишить вас сознания во время процедуры. Газы также ответственны за силу взрывов. Давайте поближе познакомимся с газами.
Их можно почувствовать, когда, например, дует ветер.Иногда вы можете почувствовать их запах, когда, например, чувствуете запах готовящейся еды или когда скунс расстроен. Некоторые газы важны для нашего здоровья (например, кислород), в то время как другие могут быть смертельными (например, сероводород и хлор). Перед операцией вам могут ввести анестезирующий газ, содержащий химические вещества, чтобы облегчить боль и лишить вас сознания во время процедуры. Газы также ответственны за силу взрывов. Давайте поближе познакомимся с газами.
Типы газов
Существует элементарных газов (состоящих из одного элемента ) и газов, состоящих из соединений (состоящих из более чем одного элемента).Символы элементарных газов можно найти в любой Периодической таблице элементов . Они представлены в таблице ниже.
| Двухатомный газ | Химическая формула | Одноатомный газ | Химическая формула |
Водород | Н 2 | Гелий | Он |
Кислород | О 2 | Неон | Не |
Азот | Н 2 | Аргон | Ар |
Фтор | Ж 2 | Криптон | Кр |
Хлор | Класс 2 | Ксенон | Хе |
Двухатомный газ — это газ, в котором основной единицей является молекула, состоящая из двух атомов, соединенных вместе. Одноатомный газ — это газ, в котором основной единицей является один атом. Однако большинство газов являются соединениями, состоящими из двух или более различных химических элементов. Наиболее распространенным является водяной пар, H 2 O. Вот названия, формулы и использование некоторых составных газов:
Одноатомный газ — это газ, в котором основной единицей является один атом. Однако большинство газов являются соединениями, состоящими из двух или более различных химических элементов. Наиболее распространенным является водяной пар, H 2 O. Вот названия, формулы и использование некоторых составных газов:
| Общее название | Химическая формула | Там, где обычно |
Углекислый газ | СО 2 | Атмосфера, автомобильные выхлопы, поп, наши легкие |
Пропан | С 3 Н 8 | Барбекю, походные печи, топливо для некоторых транспортных средств |
Метан | СН 4 | Компонент парниковых газов и природного газа |
Аммиак | НХ 3 | Используется для производства удобрений, чистящих средств |
Твердое тело, жидкость и газ для детей с практическим экспериментом по определению плотности
Помочь детям понять концепцию твердого жидкого газа для детей непросто: учащиеся лучше всего учатся, видя и трогая, а с газом ничего не поделаешь. Этот проект состояний материи для детей позволяет ЛЕГКО представить 3 состояния материи для детей с помощью воздушных шаров! Этот детский сад с твердым жидким газом , подготовительный класс, первый класс, 2-й класс, 3-й класс, 4-й класс и выше идеально подходит для летнего обучения, уроков естествознания и многого другого. МЫ также включили способ превратить это в эксперимент с плотностью для детей ! Кроме того, не пропустите рабочий лист состояний материи в формате pdf для дальнейшего изучения концепции! Вы также можете распечатать эксперимент с твердым жидким газом , чтобы расширить свои знания.
Этот проект состояний материи для детей позволяет ЛЕГКО представить 3 состояния материи для детей с помощью воздушных шаров! Этот детский сад с твердым жидким газом , подготовительный класс, первый класс, 2-й класс, 3-й класс, 4-й класс и выше идеально подходит для летнего обучения, уроков естествознания и многого другого. МЫ также включили способ превратить это в эксперимент с плотностью для детей ! Кроме того, не пропустите рабочий лист состояний материи в формате pdf для дальнейшего изучения концепции! Вы также можете распечатать эксперимент с твердым жидким газом , чтобы расширить свои знания.
Состояние вещества для детей
Когда дети начнут узнавать и исследовать окружающий мир, они узнают, что все можно классифицировать и сгруппировать в 3 состояния материи для детей . Концепция твердого жидкого газа для детей может быть объяснена с разной степенью глубины дошкольникам, детсадовцам, учащимся 1, 2, 3 и 4 классов. Этот пример твердого жидкого газа для детей и рабочий лист для экспериментов позволяют детям начать понимать три состояния материи для детей .
Этот пример твердого жидкого газа для детей и рабочий лист для экспериментов позволяют детям начать понимать три состояния материи для детей .
Существуют три распространенных состояния вещества:
- Твердые тела – Твердые тела имеют определенную форму; атомы и молекулы, из которых он состоит, связаны друг с другом. Они могут вибрировать на месте, но не двигаться.
- Жидкости. Жидкости занимают определенное пространство, но могут менять форму, протекая. Атомы и молекулы слабо связаны, но остаются близко друг к другу.
- Газы. Газ не имеет определенного объема или формы. Атомы и молекулы свободно перемещаются и расходятся друг от друга.
Твердый жидкий газ Рабочий лист
Начните с прокрутки сообщения вниз, в разделе условий использования, и щелкните текстовую ссылку, которая гласит >> _____ << Файл PDF откроется в новом окне, чтобы вы могли сохранить халяву и распечатать твердое тело . рабочий лист сжиженного газа .
рабочий лист сжиженного газа .
В отличие от нашего изображения, пожалуйста, убедитесь, что вы наполняете свои воздушные шары ОДНОГО размера!
Твердый сжиженный газ для детей
В этом простом примере мы попытались помочь учащимся ВИЗУАЛИЗИРОВАТЬ разницу между тремя состояниями материи.Теперь это непросто, поскольку газ не имеет объема и формы и, следовательно, является более абстрактным. Но мы воспользовались помощью воздушных шаров, чтобы оживить эту иллюстрацию для детей!
Для этого простого эксперимента вам понадобится следующее:
- 3 баллона
- маркер
- вода
- доступ к морозильной камере
Твердые вещества, жидкости и газы для детей
Начните с того, что наполните свой шарик тремя состояниями материи:
- Баллон, наполненный углекислым газом.CO2 — это газ, который вы выделяете при выдохе. Вы выдохнете этот газ в воздушный шар, который задержит газа в одном пространстве для визуализации.
 Пометьте шар маркером как ГАЗ.
Пометьте шар маркером как ГАЗ. - Воздушный шар, наполненный водой. h30 — это химическая формула жидкой воды. Поместите воздушный шар над краном и наполните его до того же среднего размера, что и предыдущий воздушный шар, и завяжите его. Пометьте шар с помощью вашего шари ЖИДКОСТЬЮ.
- Воздушный шар, наполненный замороженной водой.Когда вода замерзает, она становится ТВЕРДОЙ; он не движется, как вода. Наполните этот воздушный шар водой, чтобы он был такого же размера, как и другой воздушный шар с водой. Завяжите его, напишите ТВЕРДЫЙ и заморозьте шарик, пока вода не затвердеет — мы оставили его на ночь.
Твердый сжиженный газ детский сад
Теперь ваши ученики могут визуально видеть, трогать и понимать 3 состояния материи для детей !
3 состояния вещества для детей
Сделайте еще один шаг, чтобы ввести понятие плотности.По сути, плотность — это то, насколько атомы и молекулы упакованы в одном и том же относительном пространстве. Если объект тяжелый и компактный, он имеет высокую плотность. Если объект легкий и занимает много места, он имеет низкую плотность. Наши воздушные шары примерно столько же уносят из космоса, давайте сравним их плотность.
Если объект тяжелый и компактный, он имеет высокую плотность. Если объект легкий и занимает много места, он имеет низкую плотность. Наши воздушные шары примерно столько же уносят из космоса, давайте сравним их плотность.
Плотность для детей
Поднимите каждый из воздушных шаров. какой из них кажется тяжелее? Обычно воздух не подхватываешь, а в этом проекте можно. Дети легко утвердят, что газ легкий и имеет очень малую плотность.Помните, что в газе атомы плавают в воздухе и не связаны друг с другом.
Эксперимент с плотностью для детей
Теперь возьмите два шара, наполненных водой. Один из них был заморожен, чтобы стать твердым, а другой остался жидким. Спросите детей, имеют ли они одинаковую плотность? Позвольте им подумать об этом, дайте вам свой ответ и попросите их объяснить свои рассуждения.
Эксперимент с твердым жидким газом
Оба баллона были заполнены примерно одинаковым ОБЪЕМОМ воды.Так они были одинаковой плотности. Количество молекул воды в баллоне было одинаковым. Однако, когда вода замерзает и переходит из жидкого состояния в твердое, она расширяется. Вы заметили, что ваш воздушный шар со льдом больше, чем ваш воздушный шар с водой. Вода расширяется при замерзании. Таким образом, хотя в воздушном шаре те же самые молекулы, они занимают больше места; поэтому количество молекул на дюйм МЕНЬШЕ, чем в воздушном шаре.
Количество молекул воды в баллоне было одинаковым. Однако, когда вода замерзает и переходит из жидкого состояния в твердое, она расширяется. Вы заметили, что ваш воздушный шар со льдом больше, чем ваш воздушный шар с водой. Вода расширяется при замерзании. Таким образом, хотя в воздушном шаре те же самые молекулы, они занимают больше места; поэтому количество молекул на дюйм МЕНЬШЕ, чем в воздушном шаре.
Шарик с твердой водой имеет меньшую плотность, чем шар с жидкой водой, который начинался с того же размера.
Три агрегатных состояния для детей
Это упражнение «Твердое жидкое газообразное» — это такой простой, но эффективный способ помочь детям понять различные состояния материи и то, как они могут переходить из одного состояния в другое.
Твердые жидкие Газовые примеры для детей
Узнайте больше о состояниях материи с помощью этих забавных проектов:
Наука для детей
Ищете еще много веселых научных экспериментов для детей? Вы ДОЛЖНЫ попробовать некоторые из этих возмутительно забавных научных экспериментов для детей! У нас так много веселых, творческих и простых научных экспериментов для детей младшего возраста:
Эксперимент с пищевой содой и уксусом
Есть так много забавных способов поиграть и научить детей химическим реакциям, используя реакцию пищевой соды и уксуса.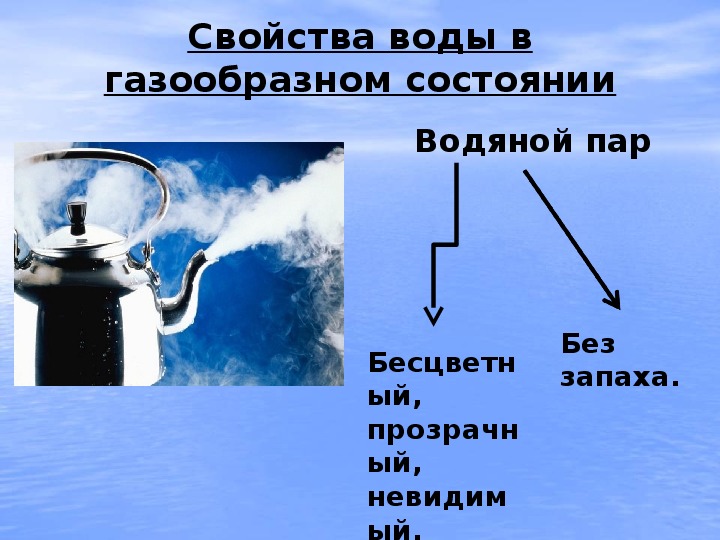 Вот некоторые из наших любимых действий с пищевой содой и уксусом.
Вот некоторые из наших любимых действий с пищевой содой и уксусом.
Состояние вещества Рабочий лист
Используя ресурсы моего сайта, вы соглашаетесь со следующим:
- Это для личного или персонального класса только для использования (чтобы поделиться, отправьте другим пользователям ссылку на этот пост, чтобы получить их собственную копию, спасибо!)
- Это ЗАПРЕЩЕНО продавать, размещать, воспроизводить или хранить на любом другом сайте (включая блог, Facebook, Dropbox и т. д.)
- Все предоставленные материалы защищены авторским правом.См. Условия использования.
- Графика Приобретена и используется с разрешения
- Я предлагаю бесплатные печатные материалы, чтобы благословить своих читателей И обеспечить свою семью. Ваши частые посещения моего блога и поддержка покупок через партнерские ссылки и рекламу, так сказать, поддерживают меня. Спасибо!
>> Активность твердых жидких газов
<<<Состояние материи: факты (Научный путь: Общественное телевидение Айдахо)
См.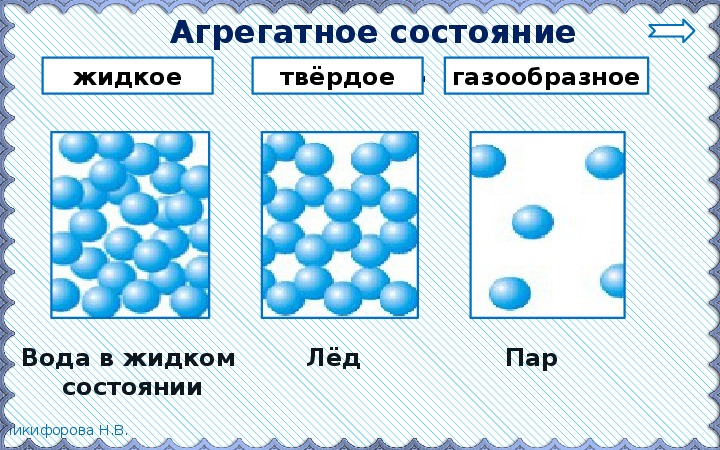 10 лучших вопросов
10 лучших вопросов
Материя окружает нас повсюду.Материя — это воздух, которым вы дышите. Материя — это компьютер, с которого вы сейчас читаете. Материя — это то, к чему вы прикасаетесь и что видите. И больше. Материя определяется как все, что имеет массу и занимает пространство. Материя находится в 3 основных состояниях; твердые, жидкие и газообразные.
Так из чего состоит материя? Вся материя состоит из атомов. Атомы – мельчайшие частицы материи. Они настолько малы, что их нельзя увидеть ни глазами, ни даже в обычный микроскоп. Стандартный лист бумаги имеет толщину около миллиона атомов.Наука разработала технологию идентификации атомов, называемую сканирующим туннельным микроскопом (СТМ), который использует электричество для картирования атомов. Об атомах мы поговорим позже, но сначала давайте узнаем о трех состояниях материи.
Твердые вещества
Вещество, состоящее из плотно упакованных атомов, называется твердым телом. Вы не можете пройти через сплошную стену. Материя упакована настолько плотно, что не позволяет двигаться сквозь нее. Твердые тела сохраняют свою форму при комнатной температуре.Карандаш, который вы оставили в парте в школе, останется такой же формы, когда вы вернетесь завтра.
Материя упакована настолько плотно, что не позволяет двигаться сквозь нее. Твердые тела сохраняют свою форму при комнатной температуре.Карандаш, который вы оставили в парте в школе, останется такой же формы, когда вы вернетесь завтра.
Даже в твердых телах между атомами есть небольшое пространство. В зависимости от того, насколько плотно упакованы атомы, определяется плотность вещества. Это означает, что блок дерева в один дюйм не такой плотный, как блок золота в один дюйм. Между атомами дерева больше пространства, чем между атомами золота.
Жидкости
Жидкости не сохраняют свою форму при комнатной температуре.Между атомами жидкости есть пространство, и они все время немного двигаются. Это позволяет вам опускать палец в воду и вытаскивать его обратно, позволяя воде снова заполнить то место, где когда-то был ваш палец. Но когда вы идете по воде в бассейне, вы должны отталкивать воду в сторону ‐ это означает, что вы чувствуете тяжесть воды. Жидкости текут или переливаются и могут принимать форму сосуда.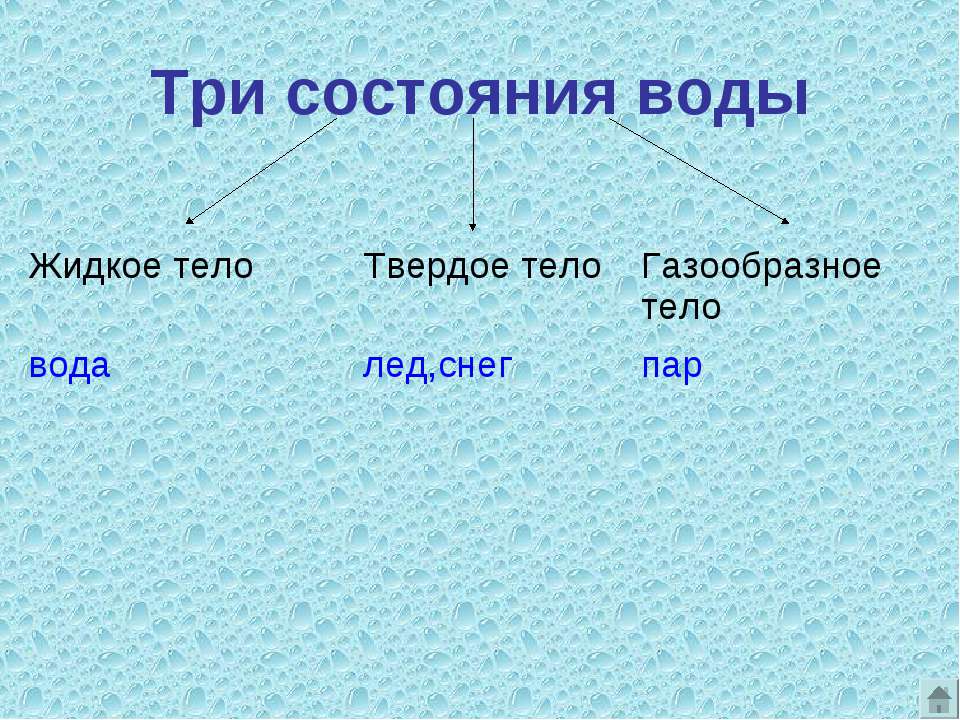 Если жидкость налить в более широкую или узкую емкость, жидкость примет эту новую форму.На жидкости действует гравитация. Если вы нальете только полстакана молока, в верхней половине контейнера не будет молока. Жидкости нельзя передавать другому человеку без контейнера. Представьте, что вы идете в ресторан и просите лимонад. Что, если официант просто даст лимонад вам в руки ‐ без стакана или чашки? Не могли бы вы поставить лимонад на стол, чтобы выпить через несколько минут? Даже вода в реке или озере имеет емкость ‐ берега, дно, берег ‐ они образуют контейнер.
Если жидкость налить в более широкую или узкую емкость, жидкость примет эту новую форму.На жидкости действует гравитация. Если вы нальете только полстакана молока, в верхней половине контейнера не будет молока. Жидкости нельзя передавать другому человеку без контейнера. Представьте, что вы идете в ресторан и просите лимонад. Что, если официант просто даст лимонад вам в руки ‐ без стакана или чашки? Не могли бы вы поставить лимонад на стол, чтобы выпить через несколько минут? Даже вода в реке или озере имеет емкость ‐ берега, дно, берег ‐ они образуют контейнер.
Газы
Газы не только не сохраняют свою форму при комнатной температуре, они даже не остаются на месте. Газы всегда в движении. Между атомами в газе так много пространства, что вы можете легко перемещаться в нем. Когда вы идете из одного конца комнаты в другой, вы проходите через кучу газов, из которых состоит наш воздух. Вы даже не знаете, что они там. Газы примут форму своего контейнера и могут быть сжаты в меньшее пространство.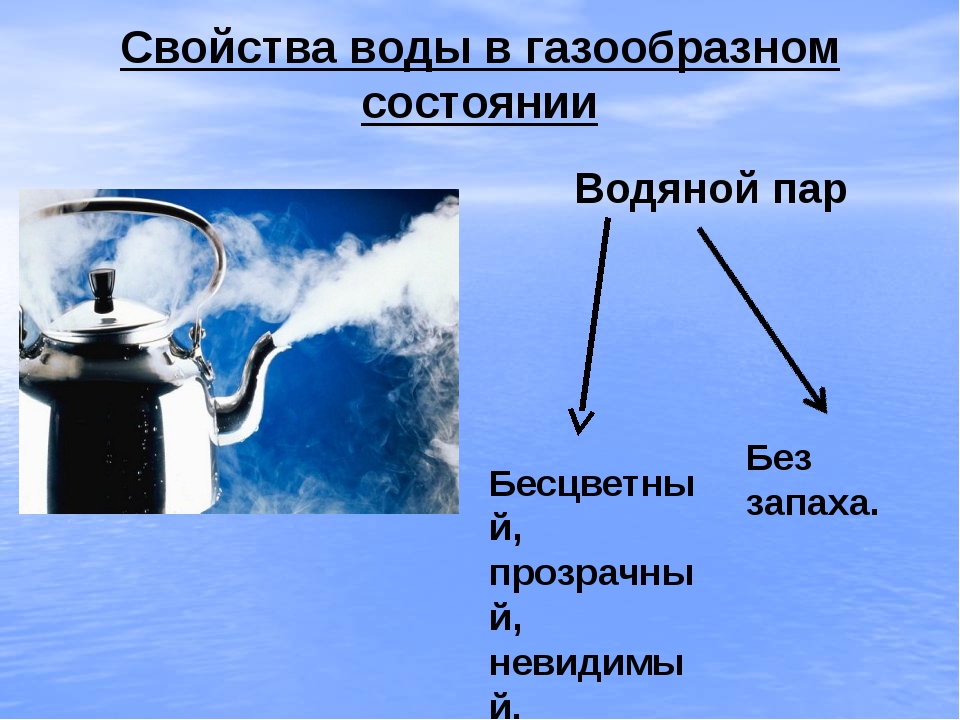 Например, когда мы сжимаем воздух в воздушный шар ‐ он заполняет форму воздушного шара.Газы также заполнят пространство. Вы не видите только половину шара, наполненного воздухом ‐ на воздух не так влияет гравитация, как на жидкость или твердое тело.
Например, когда мы сжимаем воздух в воздушный шар ‐ он заполняет форму воздушного шара.Газы также заполнят пространство. Вы не видите только половину шара, наполненного воздухом ‐ на воздух не так влияет гравитация, как на жидкость или твердое тело.
Для лучшего понимания взгляните на эти анимации поведения твердых тел, жидкостей и газов.
Изменение состояния
Материя может переходить из одного состояния в другое, но может оставаться одной и той же субстанцией. Изменение состояния, также называемое фазовым переходом, представляет собой физическое изменение одного состояния вещества в другое, например, из твердого состояния в жидкое или из жидкого в газообразное.
Как материя переходит из одной фазы в другую? Если движение атомов изменяется под воздействием давления или температуры, то и состояние может измениться. Понижая температуру воды, она может замерзнуть в твердое состояние. Нагревая воду, она может стать паром, который является газом. Твердое, жидкое или газообразное ‐ вода остается водой.
Твердое, жидкое или газообразное ‐ вода остается водой.
Давление может переводить материю из одного состояния в другое. Глубоко в земле твердые вещества превращаются в жидкости, потому что тяжелый вес слоев и слоев земли давит на твердые тела, заставляя их превращаться в жидкую магму.Это всего лишь один пример того, как давление может изменить материю.
Другая материя тоже меняется, но часто существует только в двух состояниях или требует помощи людей и технологий для прохождения всех трех фаз. Вода — единственное вещество на земле, которое в природе может быть найдено во всех трех формах: твердом, жидком и газообразном.
Подробнее об атомах
Атом состоит из ядра нейтронов и протонов ‐ даже более мелкие частицы, чем атом. Их называют субатомными частицами.Электроны вращаются вокруг этого ядра. Атомы, как правило, имеют такое же количество электронов, как и количество протонов в ядре. Это число очень значимо. Каждый вид атома имеет разное количество протонов. Например: кислород имеет 8 протонов. Это означает, что у него также есть 8 электронов. 8 известен как его атомный номер. Но у золота 79 протонов и 79 электронов. Если вы хотите узнать, сколько протонов и электронов содержится в том или ином атоме, периодическая таблица элементов — то, что вам нужно.
Например: кислород имеет 8 протонов. Это означает, что у него также есть 8 электронов. 8 известен как его атомный номер. Но у золота 79 протонов и 79 электронов. Если вы хотите узнать, сколько протонов и электронов содержится в том или ином атоме, периодическая таблица элементов — то, что вам нужно.
Элементы
Таблица говорит нам только об атомах примерно 100 элементов, обнаруженных на Земле. Элемент не может быть разбит на более мелкие компоненты. Золото ни из чего не состоит ‐ кроме элемента золота. Самый маленький возможный кусок золота — это просто золото. Если бы он был немного меньше, это были бы субатомные частицы ‐ протоны, нейтроны и электроны.
Некоторые из этих элементов представляют собой твердые тела, такие как золото или серебро. Другие представляют собой газы, такие как кислород и водород, а третьи могут быть жидкими, как ртуть.Конечно, это зависит от комнатной температуры. Если элемент нагревается или охлаждается, или если к элементу приложено достаточное давление, которое может изменить его состояние материи.
Соединения
Бьюсь об заклад, вы не найдете соли в Периодической таблице элементов. Это потому, что соль на самом деле состоит из двух элементов; натрий и хлор. Вы можете найти оба из них на столе. Атомы натрия и хлорида соли связаны друг с другом так же, как магниты могут быть связаны друг с другом.Мы называем это соединением. Вода – это соединение, состоящее из кислорода и водорода. Сахар ‐ белый материал, который вы добавляете в печенье ‐ состоит из углерода, водорода и кислорода. Многие вещества вокруг нас являются соединениями. От уксуса до бытового отбеливателя, жидкости для снятия лака, пищевой соды и аспирина ‐ мы используем соединения по всему дому.
Свойства
Вся материя обладает качествами, которые описывают ее с научной точки зрения. Мы называем эти свойства.Они могут объяснить физические или химические свойства вещества. Некоторые из способов, которыми мы описываем материю, — это ее цвет, ее блеск и ее состояние при комнатной температуре или ее запах. Масса, температура, при которой она меняет состояния, электропроводность и гибкость, также являются свойствами материи. Они различны для каждого типа материи и могут помочь ученым идентифицировать материю.
Масса, температура, при которой она меняет состояния, электропроводность и гибкость, также являются свойствами материи. Они различны для каждого типа материи и могут помочь ученым идентифицировать материю.
Плазма
Мы часто говорим о трех состояниях материи; твердые, жидкие и газообразные.Большая часть материи, которую мы используем, находится в одной из этих трех форм. Но есть еще один, который мы видим и используем, и без которого нам было бы трудно жить ‐ плазма. Его часто называют четвертым состоянием вещества. Плазма электрически заряжена, не держит форму, обладает огромным количеством энергии, и ею очень трудно манипулировать без лаборатории. Плазму можно найти здесь, на Земле, в пламени, молниях и полярных сияниях. Солнце, звезды и некоторые другие космические явления и объекты также состоят из плазменного вещества.
Больше состояний материи?
Знаете ли вы, что существует больше фаз материи? Мы не так знакомы с ними и не видим их каждый день. Некоторые существуют только в теории, другие могут быть воспроизведены в лабораториях, некоторые настолько новы, что ученые еще выясняют детали, а другие могут существовать, но еще не обнаружены в природе. К ним относятся: кварк-глюонная плазма, конденсаты Бозе-Эйнштейна, фермионные конденсаты, странная материя, жидкие кристаллы, квантовая спиновая жидкость (КСР), сверхтекучие жидкости, сверхтвердые тела и парамагнитные и ферромагнитные фазы магнитных материалов.Новые теории и открытия происходят постоянно, поэтому вам придется продолжать изучать физику, чтобы узнать больше об этих состояниях материи.
Некоторые существуют только в теории, другие могут быть воспроизведены в лабораториях, некоторые настолько новы, что ученые еще выясняют детали, а другие могут существовать, но еще не обнаружены в природе. К ним относятся: кварк-глюонная плазма, конденсаты Бозе-Эйнштейна, фермионные конденсаты, странная материя, жидкие кристаллы, квантовая спиновая жидкость (КСР), сверхтекучие жидкости, сверхтвердые тела и парамагнитные и ферромагнитные фазы магнитных материалов.Новые теории и открытия происходят постоянно, поэтому вам придется продолжать изучать физику, чтобы узнать больше об этих состояниях материи.
Что означает комнатная температура?
Состояние вещества элемента или атома основано на его поведении при комнатной температуре. Но что такое комнатная температура? Комнатная температура относится к температуре воздуха, не подвергаемого специальному нагреву или охлаждению. Обычно от 20 до 25°C (от 68 до 77°F). Хотя фактическая температура может быть выше или ниже этих цифр, это просто означает, что вещество не было помещено в духовку или морозильник, а было оставлено в комнате, чтобы достичь температуры остальной части комнаты. Если кубик льда оставить в комнате на некоторое время, он растает и превратится в жидкую воду. Вода является жидкостью при комнатной температуре. Алмаз, с другой стороны, является твердым телом при комнатной температуре и не изменит своего состояния независимо от того, как долго он там находится.
Если кубик льда оставить в комнате на некоторое время, он растает и превратится в жидкую воду. Вода является жидкостью при комнатной температуре. Алмаз, с другой стороны, является твердым телом при комнатной температуре и не изменит своего состояния независимо от того, как долго он там находится.
Основы круговорота воды
• Школа водных наук ДОМАШНЯЯ СТРАНИЦА • Круговорот воды •
Примечание: Наша информация касается только естественного круговорота воды, который не принимает во внимание деятельность человека.В современном мире люди оказывают большое влияние на многие компоненты круговорота воды.
Загрузите и распечатайте эту схему
Доступ к подробной информации о каждом компоненте водного цикла:
атмосфера · Конденсация · Испарение · Evapotranspiration · Evapotranspirate · пресноводные озера · Оборудование для подземных вод · Хранение подземных вод · Ice и Snow · Infiltration · Oceans · Осадки · Снеготаяние · Родники · Речной сток · Сублимация · Поверхностный сток
(очень) краткий обзор круговорота воды
Откуда вся вода Земли ? Первобытная Земля представляла собой раскаленный шар из магмы, но все магмы содержат воду. Вода, освобожденная магмой, начала охлаждать атмосферу Земли , пока не смогла остаться на поверхности в виде жидкости . Вулканическая деятельность продолжала и продолжает приносить воду в атмосферу, тем самым увеличивая объем поверхностных и подземных вод Земли.
Вода, освобожденная магмой, начала охлаждать атмосферу Земли , пока не смогла остаться на поверхности в виде жидкости . Вулканическая деятельность продолжала и продолжает приносить воду в атмосферу, тем самым увеличивая объем поверхностных и подземных вод Земли.
Круговорот воды не имеет начальной точки. Но мы начнем с океанов , так как именно там находится большая часть воды на Земле. Солнце, управляющее круговоротом воды, нагревает воду в океанах. Часть его испаряется в виде пара в воздух. Лед и снег могут сублимировать непосредственно в водяной пар. Восходящие воздушные потоки уносят пар вверх в атмосферу вместе с водой из эвапотранспирации , которая представляет собой воду, испаряемую растениями и испаряемую из почвы. Пар поднимается в воздух, где более низкие температуры заставляют его конденсироваться в облака .
Воздушные потоки перемещают облака по земному шару, частицы облаков сталкиваются, растут и выпадают с неба в виде осадков .Некоторые осадки выпадают в виде снега и могут накапливаться в виде ледяных шапок и ледников, которые могут хранить замороженную воду в течение тысяч лет. Снежный покров в более теплом климате часто тает и тает с приходом весны, и талая вода стекает по суше в виде таяния снега .
Большая часть осадков выпадает обратно в океаны или на сушу, где под действием силы тяжести осадки стекают по земле в виде поверхностного стока . Часть стока поступает в реки в долинах ландшафта, при этом речной поток перемещает воду к океанам.Сток и просачивание подземных вод накапливаются и сохраняются в виде пресной воды в озерах. Однако не весь сток стекает в реки. Большая его часть впитывается в землю в виде проникновения . Часть воды проникает глубоко в землю и пополняет водоносные горизонты (насыщенные подземные породы), которые хранят огромные количества пресной воды в течение длительных периодов времени.
Некоторая инфильтрация остается близко к поверхности земли и может просачиваться обратно в поверхностные водоемы (и океан) в виде выхода подземных вод , а часть подземных вод находит отверстия на поверхности земли и выходит в виде пресноводных родников .Однако с течением времени вся эта вода продолжает двигаться, некоторые снова попадают в океан, где круговорот воды «заканчивается»… упс, я имею в виду, где он «начинается».
Глобальное распределение воды
Для примерного объяснения того, где на Земле есть вода, посмотрите на таблицу ниже. К настоящему времени вы знаете, что круговорот воды описывает движение воды на Земле, поэтому поймите, что диаграмма и таблица ниже представляют присутствие воды на Земле в определенный момент времени. Если вы вернетесь назад через тысячу или миллион лет, несомненно, эти цифры будут другими!
Обратите внимание, что из общего запаса воды в мире, составляющего около 333 миллионов кубических миль (1 386 миллионов кубических километров) воды, более 96 процентов составляют соленых . И из общего количества пресной воды более 68 процентов заперты во льду и ледниках. Еще 30 процентов пресной воды находится в земле. Таким образом, реки и озера , которые снабжают людей поверхностными водами, составляют всего около 22 300 кубических миль (93 100 кубических километров), что составляет около 0,007 процента от общего объема воды, однако реки являются источником большей части воды, используемой людьми.
И из общего количества пресной воды более 68 процентов заперты во льду и ледниках. Еще 30 процентов пресной воды находится в земле. Таким образом, реки и озера , которые снабжают людей поверхностными водами, составляют всего около 22 300 кубических миль (93 100 кубических километров), что составляет около 0,007 процента от общего объема воды, однако реки являются источником большей части воды, используемой людьми.
Одна оценка глобального распределения воды
(Проценты округлены, поэтому не будут добавляться к 100)
| Источник воды | Объем воды в кубических милях | Объем воды в кубических километрах | Процент пресной воды | Процент от общего количества воды |
|---|---|---|---|---|
| Океаны, моря и заливы | 321 000 000 | 1 338 000 000 | — | 96.54 |
| Ледяные шапки, ледники и вечный снег | 5 773 000 | 24 064 000 | 68,7 | 1,74 |
| Подземные воды | 5 614 000 | 23 400 000 | — | 1,69 |
| Свежий | 2 526 000 | 10 530 000 | 30,1 | 0,76 |
| Солевой раствор | 3 088 000 | 12 870 000 | — | 0. 93 93 |
| Влажность почвы | 3 959 | 16 500 | 0,05 | 0,001 |
| Грунтовый лед и вечная мерзлота | 71 970 | 300 000 | 0,86 | 0,022 |
| Озера | 42 320 | 176 400 | — | 0,013 |
| Свежий | 21 830 | 91 000 | 0.26 | 0,007 |
| Солевой раствор | 20 490 | 85 400 | — | 0,006 |
| Атмосфера | 3 095 | 12 900 | 0,04 | 0,001 |
| Болотная вода | 2 752 | 11 470 | 0,03 | 0,0008 |
| Реки | 509 | 2 120 | 0.006 | 0,0002 |
| Биологическая вода | 269 | 1 120 | 0,003 | 0,0001 |
Источник: глава Игоря Шикломанова «Мировые ресурсы пресной воды» в книге Питера Х. Глейка (редактор), 1993 г., «Вода в условиях кризиса: Путеводитель по мировым ресурсам пресной воды» (издательство Оксфордского университета, Нью-Йорк).
Глейка (редактор), 1993 г., «Вода в условиях кризиса: Путеводитель по мировым ресурсам пресной воды» (издательство Оксфордского университета, Нью-Йорк).
Книги о свойствах материи и изменениях в материи для учащихся начальной школы
Преподавание с помощью иллюстрированных книг о состояниях материи улучшит ваши научные знания и расширит базовые знания учащихся о свойствах материи.Наряду с состояниями вещества учащиеся также могут узнать о необратимых и необратимых изменениях.
Эти учебники соответствуют стандартам NGSS для второго класса по физике. Понимание свойств материи и состояний материи находится во втором классе научных стандартов следующего поколения, а также обратимых и необратимых изменений. В стандартах учащимся предлагается описать свойства вещества, понять свойства твердых тел, жидкостей и газов, а также то, что вещество изменяется в зависимости от температуры.
Эти книги дополняют наши научные станции второго уровня о свойствах материи и состояниях материи, а также наши научные станции об обратимых и необратимых изменениях.
Книги о материи для расширения ваших научных знаний
Материя: физика для детей – Энди Дин
Возраст: 4–8 лет
Класс: K-3
Все, к чему вы можете прикоснуться и взять в руки, состоит из материи! Эта книга исследует определение материи и различные состояния материи, а также вещи в нашем мире, которые не являются материей.Дети знакомятся с физическими науками с помощью подробных иллюстраций и веселого языка, чтобы передать знакомые примеры реальных научных связей.
Из чего состоит мир? Все о твердых телах, жидкостях и газах. – Kathleen Weidner Zoehfeld
Возраст: 4–8 лет
Класс: PreK-3
Эта книга представляет собой увлекательное исследование трех состояний материи с богатым словарным запасом и простыми забавными диаграммами, объясняющими различия между твердыми телами, жидкостями и газ.
Что случилось в комнате мистера Уискера? – Майкл Элсон Росс
Возраст: 6–9 лет
Класс: 1–4
В классе мистера Уискера каждый – ученый, где практические мини-эксперименты приводят к большим идеям. Эта книга даже включает дополнительные проекты для младших школьников.
Эта книга даже включает дополнительные проекты для младших школьников.
Измени! Твердые тела, жидкости, газы и вы – Эдриенн Мейсон
Возраст: 4–7 лет
Уровень: PreK-2
Эта книга представляет собой пособие для обучения детей младшего возраста физическим наукам. Он берет физику твердых тел, жидкостей и газов и превращает ее в простую для понимания научную книгу для самых маленьких.
Супернаука: материя имеет значение! – Том Адамс
Возраст: 7-10 лет
Класс: 2-5
Эта книга исследует элементы науки о материи в увлекательной и простой форме. Он включает в себя иллюстрации в стиле комиксов и исследует атомы, молекулы, реакции, элементы, радиоактивность и другие аспекты химии.
Материя: увидь, потрогай, попробуй, понюхай – Дарлин Р. Стилл
Возраст: 5–10 лет
Класс: K-4
В этой книге объясняются и демонстрируются состояния материи, а также он даже включает эксперимент, который вы можете попробовать дома.
Многие виды материи: Взгляд на твердые тела, жидкости и газы – Дженнифер Бутройд
Возраст: 6–9 лет
Класс: 1–3
Твердые тела, жидкости и газы окружают вас повсюду. В этой книге рассказывается о различных состояниях материи и о том, как их различать!
Свойства материи – Classroom Complete Press
Возраст: 10–13 лет
Класс: 4–8
Что есть материя, а что нет? Этот ресурс разрушает физические и химические свойства материи.Читатели начнут с того, что я идентифицирую атомы, частицы и молекулы. Затем исследуйте состояния материи и определите, является ли что-то прозрачным, непрозрачным или полупрозрачным. Они узнают о физических и химических изменениях, которые могут произойти в наших собственных домах. Кроме того, они также смогут завершить свой собственный эксперимент.
Изменяющаяся материя: понимание физических и химических изменений – Трейси Маурер
Возраст: 9–10 лет
Класс: 4–5
В этой книге исследуется, как физические изменения создают различные формы или состояния материи, и приводятся примеры различных состояний в легко читаемый текст. Он также знакомит учащихся с законом сохранения массы.
Он также знакомит учащихся с законом сохранения массы.
Твердая правда о состояниях материи с Максом Аксиомой, суперученый – Агнешка Бискуп
Возраст: 8–14 лет
Класс: 3–9 , и газы, плавление, кипение и замерзание, испарение и конденсация.
Прикоснись! Материалы, материя и вы – Эдриенн Мейсон
Возраст: 4–7 лет
Класс: PreK-2
Эта книга учит детей младшего возраста физическим наукам и полна удивительных фактов и практических занятий.Он исследует материалы и их цвет, форму, текстуру, размер, массу, магнетизм и многое другое.
Природа материи – Дебора Дж. Хаузел
Возраст: 6–9 лет
Класс: 2–3
Все, что занимает место, является материей. Узнайте о материи с помощью этой книги для чтения, которая легко читается и даже включает в себя забавный и увлекательный научный эксперимент.
Материя принимает все формы – Эми С. Хансен
Возраст: 6-7 лет
Класс: 1-2
В этой книге первые читатели будут исследовать различные типы материи, которые они видят и испытывают в повседневной жизни. Он не только описывает состояния материи, но также показывает, как материя меняет форму в зависимости от контейнера, в котором она находится. Есть также компоненты книги, посвященные необратимым изменениям.
Он не только описывает состояния материи, но также показывает, как материя меняет форму в зависимости от контейнера, в котором она находится. Есть также компоненты книги, посвященные необратимым изменениям.
Физика. Почему Материя имеет значение! – Дэн Грин
Возраст: 10–14 лет
Класс: 4–5
В этой книге представлены персонажи, основанные на физике и строительных кирпичиках вселенной, и каждый из них обладает уникальным характером. Он охватывает все, от гравитации до теории относительности.Он имеет визуальные интерпретации сложных понятий, которые делают изучение физики легким и увлекательным.
Замерзание и таяние – Робин Нельсон
Возраст: 5–8 лет
Класс: K-2
В этой книге рассказывается о том, как вода превращается из жидкого состояния в твердое и обратно, а также приводится множество интересных фактов о воде и льде.
Изменяющаяся материя – Карен Ларсон
Возраст: 6–11 лет
Класс: 3–4
Эта книга позволяет учащимся не только изучать науку, но и развивать навыки грамотности и проводить простые практические научные эксперименты. Книга затрагивает три состояния материи, плазмы, и побуждает студентов задаться вопросом, является ли материя явно твердым, жидким или газообразным.
Книга затрагивает три состояния материи, плазмы, и побуждает студентов задаться вопросом, является ли материя явно твердым, жидким или газообразным.
Плавящаяся материя – Эми С. Хансен
Возраст: 7–8 лет
Класс: 2–3
В этой книге рассказывается о том, что происходит с объектами в различных условиях, например, в горячем и холодном, влажном и сухом.
Все 17 книг о свойствах материи в одном месте
- Материя: физика для детей – Энди ДинКомната Уискера? – Майкл Элсон Росс
- Измени это! Твердые вещества, жидкости, газы и вы – Эдриенн Мейсон
- Супернаука: материя имеет значение! – Том Адамс
- Материя: увидеть, потрогать, попробовать, понюхать – Дарлин Р. Стилл
- Многие виды материи: взгляд на твердые тела, жидкости и газы – Дженнифер Бутройд
- Свойства материи – Класс завершен Press
- Изменяющаяся материя: понимание физических и химических изменений – Трейси Маурер
- Твердая правда о состояниях материи с Максом Аксиомой, Суперученый – Агнешка Бискуп
- Прикоснись к ней! Материалы, материя и вы — Эдриенн Мейсон
- Природа материи — Дебора Дж.
 Housel
Housel - Материя принимает все формы – Эми С. Хансен
- Физика. Почему Материя имеет значение! – Дэн Грин
- Замораживание и плавление – Робин Нельсон
- Изменение материи – Карен Ларсон
- Плавление материи – Эми С. Хансен
Matter
, Научные станции второго уровня избавились от догадок о том, как планировать, что преподавать для науки.Основное внимание в разделе «Свойства станций изучения материи» уделяется NGSS DCI 2-PS1.A. Он включает в себя представления о том, как материя может находиться в разных состояниях в зависимости от температуры, и что материю можно классифицировать по ее свойствам. Кроме того, учащиеся узнают, как объекты можно создавать из небольших наборов деталей.
Более подробную информацию о свойствах станций изучения материи для второклассников можно найти в этом сообщении блога.

