Формула азота в химии
Атомная масса: 14,008.а.е.м.
Электронная и графическая формула азота
Электронная формула: 1s2 2s2 2p3.
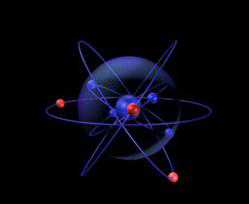
Электронно-графическая формула внешнего электронного слоя атома азота:
Азот является одним из самых распространенных элементов на Земле, а также одним из основных биогенных элементов, входит в состав белков и нуклеиновых кислот.
Азот – простое вещество, состоящее из двух атомов азота.
Формула: N2.
Структурная формула азота
Структурная формула:
Молярная масса: 28,016 г/моль.
При нормальных условиях азот – бесцветный газ, не имеет запаха, цвета и вкуса, плохо растворим в воде. В жидком состоянии – бесцветная, подвижная жидкость. При контакте с воздухом жидкий азот поглощает из него кислород. В твердом состоянии (−209,86°C) существует в виде снегоподобной массы или больших белоснежных кристаллов.
Молекула азота очень прочная, поскольку между атомами азота в молекуле N
Азот при обычных условиях реагирует только с литием:
при нагревании может вступить в реакцию с некоторыми другими металлами и неметаллами, также с образованием нитридов:
Наибольшее практическое значение имеет аммиак (нитрид водорода) NH3, который получается при взаимодействии водорода с азотом:
В электрическом разряде азот реагирует с кислородом, образуя оксид азота(II) NO:
Азот также может образовывать комплексные соединения с переходными металлами.
Примеры решения задач
ru.solverbook.com
Азот и его характеристики
Общая характеристика азота
Большая часть азота находится в свободном состоянии. Свободный азот является главной составной частью воздуха, который содержит 78,2% (об.) азота. Неорганические соединения азота не встречаются в природе в больших количествах, если не считать натриевую селитру NaNO3, образующую мощные пласты на побережье Тихого океана в Чили. Почва содержит незначительные количества азота, преимущественно в виде солей азотной кислоты. Но в виде сложных органических соединений – белков – азот входит в состав всех живых организмов.
Общее содержание азота в земной коре (включая гидросферу и атмосферу) составляет 0,04% (масс.).
В виде простого вещества азот – это бесцветный газ, не имеющий запаха и весьма мало растворимый в воде. Он немного легче воздуха: масса 1 л азота равна 1,25 г.
Атомная и молекулярная масса азота
Относительной атомной массой элемента называют отношение массы атома данного элемента к 1/12 массы атома углерода. Относительная атомная масса безразмерна и обозначается A
Массы молекул, также как массы атомов выражаются в атомных единицах массы. Молекулярной массой вещества называется масса молекулы, выраженная в атомных единицах массы. Относительной молекулярной массой вещества называют отношение массы молекулы данного вещества к 1/12 массы атома углерода, масса которого равна 12 а.е.м. Известно, что молекула азота двухатомна – N2. Относительная молекулярная масса молекулы азота будет равна:
Mr(N2) = 14,0064× 2 ≈ 28.
Изотопы азота
В природе азот существует в виде двух стабильных изотопов 14N (99,635%) и 15N (0,365%). Их массовые числа равны 14 и 15 соответственно. Ядро атома изотопа азота 14N содержит семь протонов и семь нейтронов, а изотопа 15N – такое же количество протонов и шесть нейтронов.
Существует четырнадцать искусственных изотопов азота с массовыми числами от 10-ти до 13-ти и от 16-ти до 25-ти, из которых наиболее стабильным является изотоп 13Nс периодом полураспада равным 10 минут.
Ионы азота
На внешнем энергетическом уровне атома азота имеется пять электронов, которые являются валентными:
1s22s22p3.
Схема строения атома азота представлена ниже:
В результате химического взаимодействия азот может терять свои валентные электроны, т.е. являться их донором, и превращаться в положительно заряженные ионы или принимать электроны другого атома, т.е. являться их акцептором, и превращаться в отрицательно заряженные ионы:
N0 –5e → N2+;
N0-4e → N4+
N0-3e → N3+;
N0-2e → N2+;
N0-1e → N1+;
N0+1e → N1-;
N0+2e → N2-;
N0+3e → N3-.
Молекула и атом азота
Молекула азота состоит из двух атомов – N2. Приведем некоторые свойства, характеризующие атом и молекулу азота:
|
Энергия ионизации атома, эВ |
14,53 |
|
Сродство атома к электрону, эВ |
0,27 |
|
Относительная электроотрицательность |
3,07 |
|
Радиус атома, нм |
0,071 |
|
Стандартная энтальпия диссоциации молекул при 25oС, кДж/моль |
945 |
Примеры решения задач
ru.solverbook.com
это что за вещество? Типы и свойства азота
Азот — это всем известный химический элемент, который обозначается буквой N. Этот элемент, пожалуй, основа неорганической химии, его начинают подробно изучать еще в 8 классе. В данной статье мы рассмотрим данный химический элемент, а также его свойства и типы.
История открытия химического элемента
Азот — это элемент, который впервые был представлен знаменитым французским химиком Антуаном Лавуазье. Но за звание первооткрывателя азота борются многие ученые, среди них и Генри Кавендиш, Карл Шееле, Даниэль Резерфорд.
Генри Кавендиш в результате опыта первым выделил химический элемент, но так и не понял, что он получил простое вещество. О своем опыте он сообщил Джозефу Пристли, который тоже проделывал ряд исследований. Вероятно, Пристли тоже удалось выделить этот элемент, но ученый не смог понять, что именно он получил, поэтому не заслужил звание первооткрывателя. Карл Шееле одновременно с ними проводил те же исследования, но не пришел к нужному выводу.
В том же году Даниэль Резерфорд сумел не только получить азот, но и описать его, опубликовать диссертацию и указать основные химические свойства элемента. Но даже Резерфорд так до конца и не понял, что он получил. Однако именно его считают первооткрывателем, потому что он был ближе всех к разгадке.

Происхождение названия азота
С греческого «азот» переводится как «безжизненный». Именно Лавуазье трудился над правилами номенклатуры и решил так назвать элемент. В 18 веке про этот элемент было известно лишь то, что он не поддерживает ни реакций горения, ни дыхания. Поэтому данное название приняли.
В латинском языке азот называется «нитрогениум», что в перевод означает «рождающий селитру». Из латинского языка и появилось обозначение азота — буква N. Но само название во многих странах не прижилось.
Распространенность элемента
Азот — это, пожалуй, один из самых распространенных элементов на нашей планете, он занимает четвертое место по распространенности. Элемент также найден в солнечной атмосфере, на планетах Уран и Нептун. Из азота состоят атмосферы Титана, Плутона и Тритона. Помимо этого, атмосфера Земли состоит на 78-79 процентов из этого химического элемента.
Азот играет важную биологическую роль, ведь он необходим для существования растений и животных. Даже тело человека содержит от 2 до 3 процентов этого химического элемента. Входит в состав хлорофилла, аминокислот, белков, нуклеиновых кислот.

Жидкий азот
Жидкий азот — это бесцветная прозрачная жидкость, является одним из агрегатных состояний химического вещества. Жидкий азот широко используется в промышленности, строительстве и медицине. Он используется при заморозке органических материалов, охлаждения техники, а в медицине для удаления бородавок (эстетическая медицина).
Жидкий азот не токсичен, а также не взрывоопасен.
Молекулярный азот
Молекулярный азот — это элемент, который содержится в атмосфере нашей планеты и образует большую ее часть. Формула молекулярного азота — N2. Такой азот вступает в реакции с другими химическими элементами или веществами только при очень высокой температуре.
Физические свойства
При нормальных условиях химический элемент азот — это газ, который не имеет запаха, цвета, а также практически не растворим в воде. Азот жидкий по своей консистенции напоминает воду, такой же прозрачный и бесцветный. У азота есть еще одно агрегатное состояние, при температуре ниже -210 градусов он превращается в твердое тело, образует много больших белоснежных кристаллов. Поглощает кислород из воздуха.
Химические свойства
Азот относится к группе неметаллов и перенимает свойства у других химических элементов из этой группы. Как правило, неметаллы не являются хорошими проводниками электричества. Азот образует различные оксиды, например NO (моноокисид). NO или окись азота является мышечным релаксантом (вещество, которое значительно расслабляет мускулатуру и при этом не оказывает никакого вреда и иных влияний на организм человека). Оксиды, где содержится больше атомов азота, например N2O — это веселящий газ, чуть-чуть сладковатый на вкус, который используется в медицине как анестезирующее средство. Однако уже оксид NO2 не имеет никакого отношения к первым двум, ведь это довольно вредный выхлопной газ, который содержится в выхлопах автомобилей и серьезно загрязняет атмосферу.
Азотная кислота, которую образуют атомы водорода, азота и три атома кислорода, является сильной кислотой. Ее широко используют в производстве удобрений, в ювелирном деле, органическом синтезе, военной промышленности (производство взрывчатых веществ, ракетного топлива и синтеза отравляющих веществ), производстве красителей, лекарств и др. Азотная кислота очень вредна для организма человека, на коже оставляет язвы и химические ожоги.
Люди ошибочно полагают, что углекислый газ — это азот. На самом деле, по своим химическим свойствам элемент реагирует лишь с небольшим количеством элементов при нормальных условиях. А углекислый газ — это оксид углерода.

Применение химического элемента
Азот в жидком состоянии применяют в медицине для лечения холодом (криотерапии), а также в кулинарии как хладагент.
Этот элемент также нашел широкое применение в промышленности. Азот — это газ, который взрыво- и пожаробезопасен. Помимо этого, он препятствует гниению и окислению. Сейчас азот используют в шахтах с целью создания взрывобезопасной среды. Газообразный азот применяют в нефтехимии.
В химической промышленности без азота обойтись очень нелегко. Его используют для синтеза различных веществ и соединений, например некоторых удобрений, аммиака, взрывчатых веществ, красителей. Сейчас большое количество азота используют для синтеза аммиака.
В пищевой промышленности это вещество зарегистрировано как пищевая добавка.

Смесь или чистое вещество?
Даже ученые первой половины 18 века, которым удалось выделить химический элемент, думали, что азот — это смесь. Но существует большая разница между этими понятиями.
Чистое вещество имеет целый комплекс постоянных свойств, таких как состав, физические и химические свойства. А смесь — это соединение, в которое входит два или больше химических элемента.
Сейчас мы знаем, что азот — это чистое вещество, так как он является химическим элементом.

При изучении химии очень важно понять, что азот является основой всей химии. Он образует различные соединения, которые всем нам встречаются, это и веселящий газ, и бурый газ, и аммиак, и азотная кислота. Недаром химия в школе начинается именно с изучения такого химического элемента, как азот.
fb.ru
АЗОТ | Энциклопедия Кругосвет
Содержание статьиАЗОТ, N (nitrogenium), химический элемент (ат. номер 7) VA подгруппы периодической системы элементов. Атмосфера Земли содержит 78% (об.) азота. Чтобы показать, как велики эти запасы азота, отметим, что в атмосфере над каждым квадратным километром земной поверхности находится столько азота, что из него можно получить до 50 млн. т нитрата натрия или 10 млн. т аммиака (соединение азота с водородом), и все же это составляет малую долю азота, содержащегося в земной коре. Существование свободного азота свидетельствует о его инертности и трудности взаимодействия с другими элементами при обычной температуре. Связанный азот входит в состав как органической, так и неорганической материи. Растительный и животный мир содержит азот, связанный с углеродом и кислородом в белках. Помимо этого, известны и могут быть получены в больших количествах азотсодержащие неорганические соединения, такие, как нитраты (NO
Историческая справка.
Опыты А.Лавуазье, посвященные исследованию роли атмосферы в поддержании жизни и процессов горения, подтвердили существование относительно инертного вещества в атмосфере. Не установив элементную природу остающегося после сгорания газа, Лавуазье назвал его azote, что на древнегреческом означает «безжизненный». В 1772 Д.Резерфорд из Эдинбурга установил, что этот газ является элементом, и назвал его «вредный воздух». Латинское название азота происходит от греческих слов nitron и gen, что означает «образующий селитру».
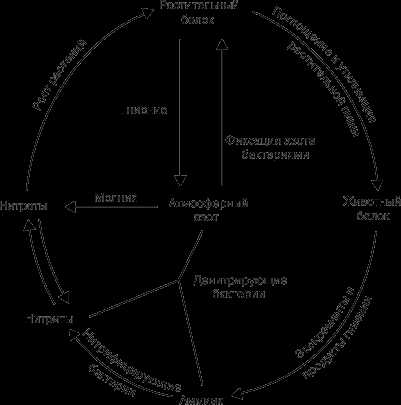
Фиксация азота и азотный цикл.
Термин «фиксация азота» означает процесс связывания атмосферного азота N2. В природе это может происходить двумя путями: либо бобовые растения, например горох, клевер и соя, накапливают на своих корнях клубеньки, в которых бактерии, фиксирующие азот, превращают его в нитраты, либо происходит окисление атмосферного азота кислородом в условиях разряда молнии. С.Аррениус установил, что таким способом фиксируется до 400 млн. т азота ежегодно. В атмосфере оксиды азота соединяются с дождевой водой, образуя азотную и азотистую кислоты. Кроме того, установлено, что с дождем и снегом на каждый гектар земли попадает ок. 6700 г азота; достигая почвы, они превращаются в нитриты и нитраты. Растения используют нитраты для образования растительных белковых веществ. Животные, питаясь этими растениями, усваивают белковые вещества растений и превращают их в животные белки. После смерти животных и растений происходит их разложение, азотные соединения превращаются в аммиак. Аммиак используется двумя путями: бактерии, не образующие нитратов, разрушают его до элементов, выделяя азот и водород, а другие бактерии образуют из него нитриты, которые другими бактериями окисляются до нитратов. Таким образом происходит круговорот азота в природе, или азотный цикл.
Строение ядра и электронных оболочек.
В природе существуют два стабильных изотопа азота: с массовым числом 14 ( содержит 7 протонов и 7 нейтронов) и с массовым числом 15 ( содержит 7 протонов и 8 нейтронов). Их соотношение составляет 99,635:0,365, поэтому атомная масса азота равна 14,008. Нестабильные изотопы азота 12N, 13N, 16N, 17N получены искусственно. Схематически электронное строение атома азота таково: 1s22s22px 12py12pz1. Следовательно, на внешней (второй) электронной оболочке находится 5 электронов, которые могут участвовать в образовании химических связей; орбитали азота могут также принимать электроны, т.е. возможно образование соединений со степенью окисления от (–III) до (V), и они известны. См. также АТОМА СТРОЕНИЕ.
Молекулярный азот.
Из определений плотности газа установлено, что молекула азота двухатомна, т.е. молекулярная формула азота имеет вид NєN (или N2). У двух атомов азота три внешних 2p-электрона каждого атома образуют тройную связь:N:::N:, формируя электронные пары. Измеренное межатомное расстояние N–N равно 1,095 Å. Как и в случае с водородом (см. ВОДОРОД), существуют молекулы азота с различным спином ядра – симметричные и антисимметричные. При обычной температуре соотношение симметричной и антисимметричной форм равно 2:1. В твердом состоянии известны две модификации азота:
Энергия диссоциации моля (28,016 г или 6,023Ч1023 молекул) молекулярного азота на атомы (N2 2N) равна примерно –225 ккал. Поэтому атомарный азот может образовываться при тихом электрическом разряде и химически более активен, чем молекулярный азот.
Получение и применение.
Способ получения элементного азота зависит от требуемой его чистоты. В огромных количествах азот получают для синтеза аммиака, при этом допустимы небольшие примеси благородных газов.
Азот из атмосферы.
Экономически выделение азота из атмосферы обусловлено дешевизной метода сжижения очищенного воздуха (пары воды, CO2, пыль, другие примеси удалены). Последовательные циклы сжатия, охлаждения и расширения такого воздуха приводят к его сжижению. Жидкий воздух подвергают фракционной перегонке при медленном подъеме температуры. Первыми выделяются благородные газы, затем азот, и остается жидкий кислород. Очистка достигается многократностью процессов фракционирования. Таким методом производят многие миллионы тонн азота ежегодно, преимущественно для синтеза аммиака, который является исходным сырьем в технологии производства различных азотсодержащих соединений для промышленности и сельского хозяйства. Кроме того, очищенную азотную атмосферу часто используют, когда недопустимо присутствие кислорода.
Лабораторные способы.
Азот в небольших количествах можно получать в лаборатории разными способами, окисляя аммиак или ион аммония, например:
Очень удобен процесс окисления иона аммония нитрит-ионом:
Известны и другие способы – разложение азидов при нагревании, разложение аммиака оксидом меди(II), взаимодействие нитритов с сульфаминовой кислотой или мочевиной:
При каталитическом разложении аммиака при высокой температуре тоже можно получить азот:
Физические свойства.
Некоторые физические свойства азота приведены в табл. 1.
| Таблица 1. НЕКОТОРЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА АЗОТА | |
| Плотность, г/см3 | 0,808 (жидк.) |
| Температура плавления, °С | –209,96 |
| Температура кипения, °С | –195,8 |
| Критическая температура, °С | –147,1 |
| Критическое давление, атма | 33,5 |
| Критическая плотность, г/см3а | 0,311 |
| Удельная теплоемкость, Дж/(мольЧК) | 14,56 (15° С) |
| Электроотрицательность по Полингу | 3 |
| Ковалентный радиус, | 0,74 |
| Кристаллический радиус, | 1,4 (M3–) |
| Потенциал ионизации, Вб | |
| первый | 14,54 |
| второй | 29,60 |
| а Температура и давление, при которых плотности азота жидкого и газообразного состояния одинаковы. б Количество энергии, необходимое для удаления первого внешнего и следующего за ним электронов, в расчете на 1 моль атомарного азота. | |
Химические свойства.
Как уже было отмечено, преобладающим свойством азота при обычных условиях температуры и давления является его инертность, или малая химическая активность. Электронная структура азота содержит электронную пару на 2s-уровне и три наполовину заполненные 2р-орбитали, поэтому один атом азота может связывать не более четырех других атомов, т.е. его координационное число равно четырем. Небольшой размер атома также ограничивает количество атомов или групп атомов, которые могут быть связаны с ним. Поэтому многие соединения других членов подгруппы VA либо вовсе не имеют аналогов среди соединений азота, либо аналогичные соединения азота оказываются нестабильными. Так, PCl5 – стабильное соединение, а NCl5 не существует. Атом азота способен связываться с другим атомом азота, образуя несколько достаточно стабильных соединений, такие, как гидразин N2H4 и азиды металлов MN3. Такой тип связи необычен для химических элементов (за исключением углерода и кремния). При повышенных температурах азот реагирует со многими металлами, образуя частично ионные нитриды MxNy. В этих соединениях азот заряжен отрицательно. В табл. 2 приведены степени окисления и примеры соответствующих соединений.
| Таблица 2. СТЕПЕНИ ОКИСЛЕНИЯ АЗОТА И СООТВЕТСТВУЮЩИЕ СОЕДИНЕНИЯ | |
| Степень окисления | Примеры соединений |
| –III | Аммиак NH3, ион аммония NH4+, нитриды M3N2 |
| –II | Гидразин N2H4 |
| –I | Гидроксиламин NH2OH |
| I | Гипонитрит натрия Na2N2O2, оксид азота(I) N2O |
| II | Оксид азота(II) NO |
| III | Оксид азота(III) N2O3, нитрит натрия NaNO2 |
| IV | Оксид азота(IV) NO2, димер N2O4 |
| V | Оксид азота(V) N2O5, азотная кислота HNO3 и ее соли (нитраты) |
Нитриды.
Соединения азота с более электроположительными элементами, металлами и неметаллами – нитриды – похожи на карбиды и гидриды. Их можно разделить в зависимости от характера связи M–N на ионные, ковалентные и с промежуточным типом связи. Как правило, это кристаллические вещества.
Ионные нитриды.
Связь в этих соединениях предполагает переход электронов от металла к азоту с образованием иона N3–. К таким нитридам относятся Li3N, Mg3N2, Zn3N2 и Cu3N2. Кроме лития, другие щелочные металлы IA подгруппы нитридов не образуют. Ионные нитриды имеют высокие температуры плавления, реагируют с водой, образуя NH3 и гидроксиды металлов.
Ковалентные нитриды.
Когда электроны азота участвуют в образовании связи совместно с электронами другого элемента без перехода их от азота к другому атому, образуются нитриды с ковалентной связью. Нитриды водорода (например, аммиак и гидразин) полностью ковалентны, как и галогениды азота (NF3 и NCl3). К ковалентным нитридам относятся, например, Si3N4, P3N5 и BN – высокостабильные белые вещества, причем BN имеет две аллотропные модификации: гексагональную и алмазоподобную. Последняя образуется при высоких давлениях и температурах и имеет твердость, близкую к твердости алмаза.
Нитриды с промежуточным типом связи.
Переходные элементы в реакции с NH3 при высокой температуре образуют необычный класс соединений, в которых атомы азота распределены между регулярно расположенными атомами металла. В этих соединениях нет четкого смещения электронов. Примеры таких нитридов – Fe4N, W2N, Mo2N, Mn3N2. Эти соединения, как правило, совершенно инертны и обладают хорошей электрической проводимостью.
Водородные соединения азота.
Азот и водород взаимодействуют, образуя соединения, отдаленно напоминающие углеводороды (см. также ОРГАНИЧЕСКАЯ ХИМИЯ). Стабильность азотоводородов уменьшается с увеличением числа атомов азота в цепи в отличие от углеводородов, которые устойчивы и в длинных цепях. Наиболее важные нитриды водорода – аммиак NH3 и гидразин N2H4. К ним относится также азотистоводородная кислота HNNN (HN3).
Аммиак Nh4.
Аммиак – один из наиболее важных промышленных продуктов современной экономики. В конце 20 в. США производили ок. 13 млн. т аммиака ежегодно (в пересчете на безводный аммиак).
Строение молекулы.
Молекула NH3 имеет почти пирамидальное строение. Угол связи H–N–H составляет 107°, что близко к величине тетраэдрического угла 109°. Неподеленная электронная пара эквивалентна присоединенной группе, в результате координационное число азота равно 4 и азот располагается в центре тетраэдра.
Cвойства аммиака.
Некоторые физические свойств аммиака в сравнении с водой приведены в табл. 3.
| Таблица 3. НЕКОТОРЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА АММИАКА И ВОДЫ | ||
| Свойство | Аммиак | Вода |
| Плотность, г/см3 | 0,65 (–10° С) | 1,00 (4,0° С) |
| Температура плавления, °С | –77,7 | 0 |
| Температура кипения, °С | –33,35 | 100 |
| Критическая температура, °С | 132 | 374 |
| Критическое давление, атм | 112 | 218 |
| Энтальпия испарения, Дж/г | 1368 (–33° С) | 2264 (100° С) |
| Энтальпия плавления, Дж/г | 351 (–77° С) | 334 (0° С) |
| Удельная электропроводность | 5Ч10–11 (–33° С) | 4Ч10–8 (18° С) |
Температуры кипения и плавления у аммиака намного ниже, чем у воды, несмотря на близость молекулярных масс и сходство строения молекул. Это объясняется относительно большей прочностью межмолекулярных связей у воды, чем у аммиака (такая межмолекулярная связь называется водородной).
Аммиак как растворитель.
Высокая диэлектрическая проницаемость и дипольный момент жидкого аммиака позволяют использовать его как растворитель для полярных или ионных неорганических веществ. Аммиак-растворитель занимает промежуточное положение между водой и органическими растворителями типа этилового спирта. Щелочные и щелочноземельные металлы растворяются в аммиаке, образуя темносиние растворы. Можно полагать, что в растворе происходит сольватация и ионизация валентных электронов по схеме
Синий цвет связывают с сольватацией и движением электронов или с подвижностью «дырок» в жидкости. При высокой концентрации натрия в жидком аммиаке раствор принимает бронзовую окраску и отличается высокой электропроводностью. Несвязанный щелочной металл можно выделить из такого раствора испарением аммиака или добавлением хлорида натрия. Растворы металлов в аммиаке являются хорошими восстановителями. В жидком аммиаке происходит автоионизация
аналогично процессу, протекающему в воде:
Некоторые химические свойства обеих систем сопоставлены в табл. 4.
Жидкий аммиак как растворитель имеет преимущество в некоторых случаях, когда невозможно проводить реакции в воде из-за быстрого взаимодействия компонентов с водой (например, окисление и восстановление). Например, в жидком аммиаке кальций реагирует с KCl с образованием CaCl2 и K, поскольку CaCl2 нерастворим в жидком аммиаке, а К растворим, и реакция протекает полностью. В воде такая реакция невозможна из-за быстрого взаимодействия Ca с водой.
Получение аммиака.
Газообразный NH3 выделяется из солей аммония при действии сильного основания, например, NaOH:
Метод применим в лабораторных условиях. Небольшие производства аммиака основаны также на гидролизе нитридов, например Mg3N2, водой. Цианамид кальция CaCN2 при взаимодействии с водой также образует аммиак. Основным промышленным методом получения аммиака является каталитический синтез его из атмосферного азота и водорода при высоких температуре и давлении:
Водород для этого синтеза получают термическим крекингом углеводородов, действием паров воды на уголь или железо, разложением спиртов парами воды или электролизом воды. На синтез аммиака получено множество патентов, отличающихся условиями проведения процесса (температура, давление, катализатор). Существует способ промышленного получения при термической перегонке угля. С технологической разработкой синтеза аммиака связаны имена Ф.Габера и К.Боша.
Химические свойства аммиака.
Кроме реакций, упомянутых в табл. 4, аммиак реагирует с водой, образуя соединение NH3ЧH2O, которое часто ошибочно считают гидроксидом аммония NH4OH; в действительности существование NH4OH в растворе не доказано. Водный раствор аммиака («нашатырный спирт») состоит преимущественно из NH3, H2O и и малых концентраций ионов NH4+ и OH–, образующихся при диссоциации
Основной характер аммиака объясняется наличием неподеленной электронной пары азота:NH3. Поэтому NH3 – это основание Льюиса, которое имеет высшую нуклеофильную активность, проявляемую в форме ассоциации с протоном, или ядром атома водорода:
Любые ион или молекула, способные принимать электронную пару (электрофильное соединение), будут взаимодействовать с NH3 с образованием координационного соединения. Например:
Символ Mn+ представляет ион переходного металла (B-подгруппы периодической таблицы, например, Cu2+, Mn2+ и др.). Любая протонная (т.е. Н-содержащая) кислота реагирует с аммиаком в водном растворе с образованием солей аммония, таких, как нитрат аммония NH4NO3, хлорид аммония NH4Cl, сульфат аммония (NH4)2SO4, фосфат аммония (NH4)3PO4. Эти соли широко применяются в сельском хозяйстве как удобрения для введения азота в почву. Нитрат аммония кроме того применяют как недорогое взрывчатое вещество; впервые оно было применено с нефтяным топливом (дизельным маслом). Водный раствор аммиака применяют непосредственно для введения в почву или с орошающей водой. Мочевина NH2CONH2, получаемая синтезом из аммиака и углекислого газа, также является удобрением. Газообразный аммиак реагирует с металлами типа Na и K с образованием амидов:
Аммиак реагирует с гидридами и нитридами также с образованием амидов:
Амиды щелочных металлов (например, NaNH2) реагируют с N2O при нагревании, образуя азиды:
Газообразный NH3 восстанавливает оксиды тяжелых металлов до металлов при высокой температуре, по-видимому, благодаря водороду, образующемуся в результате разложения аммиака на N2 и H2:
Атомы водорода в молекуле NH3 могут замещаться на галоген. Иод реагирует с концентрированным раствором NH3, образуя смесь веществ, содержащую NI3. Это вещество очень неустойчиво и взрывается при малейшем механическом воздействии. При реакции NH3 c Cl2 образуются хлорамины NCl3, NHCl2 и NH2Cl. При воздействии на аммиак гипохлорита натрия NaOCl (образуется из NaOH и Cl2) конечным продуктом является гидразин:
Гидразин.
Приведенные выше реакции представляют собой способ получения моногидрата гидразина состава N2H4ЧH2O. Безводный гидразин образуется при специальной перегонке моногидрата с BaO или другими водоотнимающими веществами. По свойствам гидразин слегка напоминает пероксид водорода H2O2. Чистый безводный гидразин – бесцветная гигроскопичная жидкость, кипящая при 113,5° C; хорошо растворяется в воде, образуя слабое основание
В кислой среде (H+) гидразин образует растворимые соли гидразония типа [NH2NH2H]+X–. Легкость, с которой гидразин и некоторые его производные (например, метилгидразин) реагируют с кислородом, позволяет использовать его в качестве компонента жидкого ракетного топлива. Гидразин и все его производные сильно ядовиты.
Оксиды азота.
В соединениях с кислородом азот проявляет все степени окисления, образуя оксиды: N2O, NO, N2O3, NO2 (N2O4), N2O5. Имеется скудная информация об образовании пероксидов азота (NO3, NO4).
Оксид азота(I)
N2O (монооксид диазота) получается при термической диссоциации нитрата аммония:
Молекула имеет линейное строение
N2O довольно инертен при комнатной температуре, но при высоких температурах может поддерживать горение легко окисляющихся материалов. N2O, известный как «веселящий газ», используют для умеренной анестезии в медицине.
Оксид азота(II)
NO – бесцветный газ, является одним из продуктов каталитической термической диссоциации аммиака в присутствии кислорода:
NO образуется также при термическом разложении азотной кислоты или при реакции меди с разбавленной азотной кислотой:
NO можно получать синтезом из простых веществ (N2 и O2) при очень высоких температурах, например в электрическом разряде. В структуре молекулы NO имеется один неспаренный электрон. Соединения с такой структурой взаимодействуют с электрическим и магнитным полями. В жидком или твердом состоянии оксид имеет голубую окраску, поскольку неспаренный электрон вызывает частичную ассоциацию в жидком состоянии и слабую димеризацию в твердом состоянии: 2NO N2O2.
Оксид азота(III)
N2O3 (триоксид азота) – ангидрид азотистой кислоты: N2O3 + H2O 2HNO2. Чистый N2O3 может быть получен в виде голубой жидкости при низких температурах (–20° С) из эквимолекулярной смеси NO и NO2. N2O3 устойчив только в твердом состоянии при низких температурах (т.пл. –102,3° С), в жидком и газообразном состояния он снова разлагается на NO и NO2.
Оксид азота(IV)
NO2 (диоксид азота) также имеет в молекуле неспаренный электрон (см. выше оксид азота(II)). В строении молекулы предполагается трехэлектронная связь, и молекула проявляет свойства свободного радикала (одна линия соответствует двум спаренным электронам):
NO2 получается каталитическим окислением аммиака в избытке кислорода или окислением NO на воздухе:
а также по реакциям:
При комнатной температуре NO2 – газ темнокоричневого цвета, обладает магнитными свойствами благодаря наличию неспаренного электрона. При температурах ниже 0° C молекула NO2 димеризуется в тетраоксид диазота, причем при –9,3° C димеризация протекает полностью: 2NO2 N2O4. В жидком состоянии недимеризовано только 1% NO2, а при 100° C остается в виде димера 10% N2O4.
NO2 (или N2O4) реагирует в теплой воде с образованием азотной кислоты: 3NO2 + H2O = 2HNO3 + NO. Технология NO2 поэтому очень существенна как промежуточная стадия получения промышленно важного продукта – азотной кислоты.
Оксид азота(V)
N2O5 (устар. ангидрид азотной кислоты) – белое кристаллическое вещество, получается обезвоживанием азотной кислоты в присутствии оксида фосфора P4O10:
N2O5 легко растворяется во влаге воздуха, вновь образуя HNO3. Свойства N2O5 определяются равновесием
N2O5 – хороший окислитель, легко реагирует, иногда бурно, с металлами и органическими соединениями и в чистом состоянии при нагреве взрывается. Вероятную структуру N2O5 можно представить как
Оксокислоты азота.
Для азота известны три оксокислоты: гипоазотистая H2N2O2, азотистая HNO2 и азотная HNO3.
Гипоазотистая кислота
H2N2O2 – очень нестабильное соединение, образуется в неводной среде из соли тяжелого металла – гипонитрита при действии другой кислоты: M2N2O2 + 2HX 2MX + H2N2O2. При выпаривании раствора образуется белое взрывчатое вещество с предполагаемой структурой H–O–N=N–O–H.
Азотистая кислота
HNO2 не существует в чистом виде, однако водные растворы ее невысокой концентрации образуются при добавлении серной кислоты к нитриту бария:
Азотистая кислота образуется также при растворении эквимолярной смеси NO и NO2 (или N2O3) в воде. Азотистая кислота немного сильнее уксусной кислоты. Степень окисления азота в ней +3 (ее структура H–O–N=O), т.е. она может являться и окислителем, и восстановителем. Под действием восстановителей она восстанавливается обычно до NO, а при взаимодействии с окислителями окисляется до азотной кислоты.
Скорость растворения некоторых веществ, например металлов или иодид-иона, в азотной кислоте зависит от концентрации азотистой кислоты, присутствующей в виде примеси. Соли азотистой кислоты – нитриты – хорошо растворяются в воде, кроме нитрита серебра. NaNO2 применяется в производстве красителей.
Азотная кислота
HNO3 – один из наиболее важных неорганических продуктов основной химической промышленности. Она используется в технологиях множества других неорганических и органических веществ, например, взрывчатых веществ, удобрений, полимеров и волокон, красителей, фармацевтических препаратов и др. См. также ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ.
www.krugosvet.ru
характеристика, химические свойства, физические свойства, соединения, место в природе.
АЗОТ, N (лат. Nitrogenium * а. nitrogen; н. Stickstoff; ф. azote, nitrogene; и. nitrogeno), — химический элемент V группы периодической системы Менделеева, атомный номер 7, атомная масса 14,0067. Открыт в 1772 английским исследователем Д. Резерфордом.
Свойства азота
При обычных условиях азот — газ без цвета и запаха. Природный азот состоит из двух стабильных изотопов: 14N (99,635%) и 15N (0,365%). Молекула азота двухатомная; атомы связаны ковалентной тройной связью NN. Диаметр молекулы азота, определённый разными способами, 3,15-3,53 А. Молекула азота очень устойчива — энергия диссоциации 942,9 кДж/моль.
Молекулярный азот
Константы молекулярного азота: f плавления — 209,86°С, f кипения — 195,8°С; плотность газообразного азота 1,25 кг/ м3, жидкого — 808 кг/м3.
Характеристика азота
В твёрдом состоянии азот существует в двух модификациях: кубической а-форме с плотностью 1026,5 кг/м3 и гексагональной b-форме с плотностью 879,2 кг/м3. Теплота плавления 25,5 кДж/кг, теплота испарения 200 кДж/кг. Поверхностное натяжение жидкого азота в контакте с воздухом 8,5•10-3 Н/м; диэлектрическая проницаемость 1,000538. Растворимость азота в воде (см3 на 100 мл Н2О): 2,33 (0°С), 1,42 (25°С) и 1,32 (60°С). Внешняя электронная оболочка атома азота состоит из 5 электронов. Степени окисления азота меняются от 5 (в N2О5) до -3 (в NH3).
Соединение азота
Азот при нормальных условиях может реагировать с соединениями переходных металлов (Ti, V, Mo и др.), образуя комплексы либо восстанавливаясь с образованием аммиака и гидразина. С такими активными металлами, как литий, кальций, магний, азот взаимодействует при нагревании до сравнительно невысоких температур. С большинством других элементов азот реагирует при высокой температуре и в присутствии катализаторов. Хорошо изучены соединения азота с кислородом: N2О, NO, N2О5. С водородом азот соединяется только при высокой температуре и в присутствии катализаторов; при этом образуется аммиак NH3. С галогенами азот непосредственно не взаимодействует; поэтому все галогениды азота получают только косвенным путём, например фтористый азот NF3 — при взаимодействии фтора с аммиаком. С серой также не происходит непосредственного соединения азота. При взаимодействии раскалённого кокса с азотом образуется циан (CN)2. При действии на обычный азот электрических разрядов, а также при электрических разрядах в воздухе может образоваться активный азот, представляющий собой смесь молекул и атомов азота, обладающих повышенным запасом энергии. Активный азот весьма энергично взаимодействует с кислородом, водородом, парами серы, фосфором и некоторыми металлами.
Азот — один из самых распространённых элементов на Земле, причём основная его масса (около 4•1015 т) сосредоточена в свободном состоянии в атмосфере. Ежегодно при вулканической деятельности в атмосферу выделяется 2•106 т азота. Незначительная часть азота концентрируется в литосфере (среднее содержание в литосфере 1,9•10-3%). Природные соединения азота — хлористый аммоний и различные нитраты (селитры). Нитриды азота могут образовываться только при высоких температурах и давлениях, что, по-видимому, имело место на самых ранних стадиях развития Земли. Крупные скопления селитры встречаются только в условиях сухого пустынного климата (Чили, Индия, Египет, Испания и др.). Небольшие количества связанного азота находятся в каменном угле (1-2,5%) и нефти (0,02-1,5%), а также в водах рек, морей и океанов. Азот накапливается в почвах (0,1 %) и живых организмах (0,3%). Азот входит в состав белковых молекул и многих естественных органических соединений.
Круговорот азота в природе
В природе осуществляется круговорот азота, который включает цикл молекулярного атмосферного азота в биосфере, цикл в атмосфере химически связанного азота, круговорот захоронённого с органическим веществом поверхностного азота в литосфере с возвратом его обратно в атмосферу. Азот для промышленности ранее добывался целиком из месторождений природных селитр, число которых в мире весьма ограничено. Особенно крупные залежи азота в виде азотнокислого натрия находятся в Чили; добыча селитры в отдельные годы составляла более 3 млн. т.
Применение азота
Азот получают главным образом разделением предварительно сжиженного воздуха, который затем подвергается разгонке. Основная часть получаемого азота используется для производства аммиака, который затем перерабатывается на азотную кислоту, удобрения, взрывчатые вещества. Свободный азот применяют во многих отраслях промышленности как инертную среду при разнообразных химических и металлургических процессах. Жидкий азот находит применение в различных холодильных установках. Ведутся работы по использованию жидкого азота для замораживания неустойчивых пород (главным образом глинистых) при проходке шахтных стволов, в качестве безопасного энергоносителя для шахтных машин, а также для борьбы с рудничными пожарами, где применение азота позволяет резко снизить содержание кислорода в очаге пожара. При разработке нефтяных месторождений закачиванием азота в нефтяные пласты эффективно вытесняют нефть после заводнения. Азот используется также для поддержания давления в скважинах при бурении.
www.mining-enc.ru
Азот, свойства азота | Формулы и расчеты онлайн

Азот — бесцветный газ, который составляет 78% атмосферы нашей планеты.
Фермеры во всем мире используют в качестве удобрения аммиак, содержащий азот.
\[NH_3\]
Аммиак имеет резкий неприятный запах, и является одним из опасных химических веществ, но растворенный в небольшом количестве воды после орошения этим раствором почвы, он становится пищей для разных сель хоз-культур. Огромное количество азота ежегодно используется для орошения почв. К сожалению, большая его часть убегает с подземными водами в океан, где азот вызывает бурное цветение водорослей, потому, что в морской воде, так же как и в почве, азот часто является фактором, влияющим на рост растений. Положительной стороной, этого является возможность накормить миллиарды людей, которые в противном случае могли бы умереть с голоду. Жизнь полна компромиссов.
Азот, Свойства и параметры азота
Азот, Вступление | |
| Символ | N |
| Латинское название | Nitrogen |
| Тип вещества | простой химический элемент |
| Первооткрыватель | Д. Резерфорд |
| Год открытия | 1772 |
Основные параметры азота по таблице Менделеева | |
| Атомный номер Z | 7 |
| Атомная масса | 14.0067 |
| Группа | 15 |
| Период | 2 |
| Принадлежность к группе | неметаллы |
Механические свойства азота | |
| Плотность газообразных веществ (при 0°C и 760мм.рт.ст) | 1.250 (Килограмм / Метр3) |
| Скорость звука | 333.6 (Метр / Секунда) |
Термодинамические свойства азота | |
| Агрегатное состояние при нормальных условиях | газ |
| Точка плавления по Кельвину | 63.05 (Кельвин) |
| Точка плавления по Цельсию | -210.1 (°C) |
| Точка кипения по Кельвину | 77.36 (Кельвин) |
| Точка кипения по Цельсию | -195.79 (°C) |
| Показатель адиабаты | 1.40 |
| Газовая постоянная | 297 (Джоуль / (Килограмм · Кельвин)) |
| Коэффициент объемного расширения газов в интервале температур (0..100°C) при давлении 101.3 кПа | 3.372 · 10 − 3 (1 / Кельвин) |
Магнитные свойства азота | |
| Тип магнитной проницаемости | диамагнетик |
Свойства атома азота | |
| Конфигурация электронного облака | 1s22s22p3 |
| Радиус атома | 56 · 10 − 12 (Метр) |
| Число протонов p | 7 |
| Число нейтронов n | 7 |
| Число электронов e | 7 |
| Массовое число A | 14 |
| Атомная структура азота | 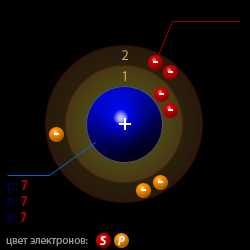 |
Химические свойства азота | |
| Валентность | 3 |
Распространенность азота | |
| Вселенная состоит из азота на | 0.1% |
| Солнце состоит из азота на | 0.1% |
| Мировой океан состоит из азота на | 0.00005% |
| Человеческое тело состоит из азота на | 2.6% |
Вселенная | |
| Вселенная состоит из азота на | 0.1% |
В помощь студенту
Азот, свойства азота |
стр. 782 |
|---|
www.fxyz.ru
Молярная масса азота (N), формула и примеры
Молярная масса азота
Молярную массу обычно выражают в г/моль, реже в кг/кмоль. Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr):
M = κ × Mr,
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Относительная молекулярная масса – величина безразмерная. Её вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
Относительная атомная масса атомарного азота равна 14,0067 а.е.м. Его относительная молекулярная масса будет равна 14,0064, а молярная масса:
M(N) = Mr (N) × 1 моль = 14,0067 г/моль.
Известно, что молекула азота двухатомна – N2, тогда, относительная атомная масса молекулы азота будет равна:
Ar(N2) = 14,0067 × 2 = 28,0134 а.е.м.
Относительная молекулярная масса молекулы азота будет равна 28,0134, а молярная масса:
M(N2) = Mr (N2) × 1 моль = 28,0134 г/моль или просто 28 г/моль.
Азот представляет собой бесцветный газ, не обладающий ни запахом, ни вкусом (схема строения атома представлена на рис. 1), плохо растворимый в воде и других растворителях с очень низкими значениями температур плавления (-210oC) и кипения (-195,8oC).
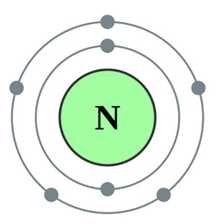
Рис. 1. Строение атома азота.
Известно, что в природе азот может находиться в виде двух изотопов 14N (99,635%) и 15N (0,365%). Эти изотопы характеризуются различным содержанием нейтронов в ядре атома, а значит и молярной массой. В первом случае она будет равна 14 г/моль, а во втором – 15 г/моль.
Молекулярную массу вещества в газообразном состоянии можно определить, используя понятие о его молярном объеме. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества, а затем вычисляют массу 22,4 л этого вещества при тех же условиях.
Для достижения данной цели (вычисление молярной массы) возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
pV = mRT / M,
где p – давление газа (Па), V – объем газа (м3), m – масса вещества (г), M – молярная масса вещества (г/моль), Т – абсолютная температура (К), R – универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
ru.solverbook.com
