Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева

Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. В центре атома находится положительно заряженное ядро. Оно занимает ничтожную часть пространства внутри атома, в нём сосредоточены весь положительный заряд и почти вся масса атома.
Ядро состоит из элементарных частиц — протона и нейтрона; вокруг атомного ядра по замкнутым орбиталям движутся электроны.
Протон (р) — элементарная частица с относительной массой 1,00728 атомной единицы массы и зарядом +1 условную единицу. Число протонов в атомном ядре равно порядковому номеру элемента в Периодической системе Д.И. Менделеева.
Нейтрон (n) — элементарная нейтральная частица с относительной массой 1,00866 атомной единицы массы (а. е. м.).
Число нейтронов в ядре N определяют по формуле:
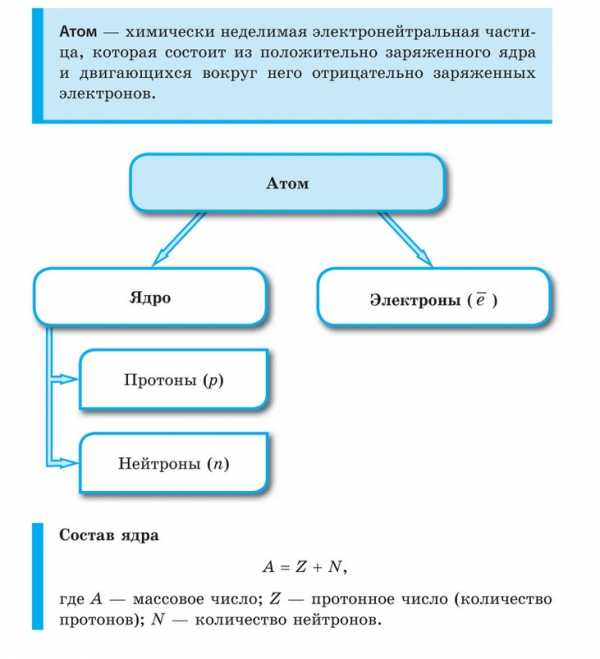
где А — массовое число, Z — заряд ядра, равный числу протонов (порядковому номеру).
Обычно параметры ядра атома записывают следующим образом: слева внизу от символа элемента ставят заряд ядра, а вверху — массовое число, например:
Эта запись показывает, что заряд ядра (следовательно, и число протонов) для атома фосфора равен 15, массовое число равно 31, а число нейтронов равно 31 – 15 = 16. Так как массы протона и нейтрона очень мало отличаются друг от друга, то массовое число приблизительно равно относительной атомной массе ядра.
Электрон ( е–) — элементарная частица с массой 0,00055 а. е. м. и условным зарядом –1. Число электронов в атоме равно заряду ядра атома (порядковому номеру элемента в Периодической системе Д.И. Менделеева).
Электроны движутся вокруг ядра по строго определённым орбиталям, образуя так называемое электронное облако.
Область пространства вокруг атомного ядра, где наиболее (90 и более %) вероятно нахождение электрона, определяет форму электронного облака.
Электронное облако s-электрона имеет сферическую форму; на s-энергетическом подуровне может максимально находиться два электрона.
Электронное облако p-электрона имеет гантелеобразную форму; на трёх p-орбиталях максимально может находиться шесть электронов.
Орбитали изображают в виде квадрата, сверху или снизу которого пишут значения главного и побочного квантовых чисел, описывающих данную орбиталь. Такую запись называют графической электронной формулой, например:
В этой формуле стрелками обозначают электрон, а направление стрелки соответствует направлению спина — собственного магнитного момента электрона. Электроны с противоположными спинами ↑↓ называют спаренными.
Электронные конфигурации атомов элементов можно представить в виде электронных формул, в которых указывают символы подуровня, коэффициент перед символом подуровня показывает его принадлежность к данному уровню, а степень у символа — число электронов данного подуровня.
В таблице 1 приведено строение электронных оболочек атомов первых 20 элементов Периодической системы химических элементов Д.И. Менделеева.
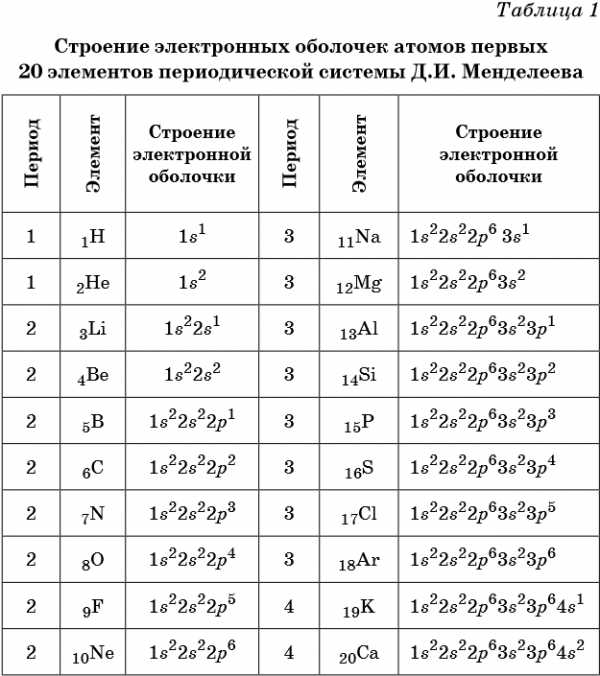
Химические элементы, в атомах которых s-подуровень внешнего уровня пополняется одним или двумя электронами, называют s-элементами. Химические элементы, в атомах которых заполняется p-подуровень (от одного до шести электронов), называют p-элементами.
Число электронных слоёв в атоме химического элемента равно номеру периода.
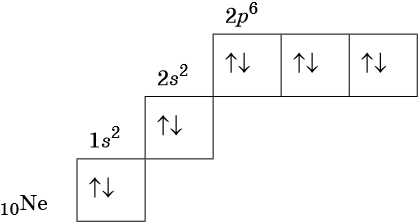
В соответствии с правилом Хунда электроны располагаются на однотипных орбиталях одного энергетического уровня таким образом, чтобы суммарный спин был максимален. Следовательно, при заполнении энергетического подуровня каждый электрон прежде всего занимает отдельную ячейку, а только после этого начинается их спаривание. Например, у атома азота все p-электроны будут находиться в отдельных ячейках, а у кислорода начнётся их спаривание, которое полностью закончится у неона.

Изотопами называют атомы одного и того же элемента, содержащие в своих ядрах одинаковое число протонов, но различное число нейтронов.
Изотопы известны для всех элементов. Поэтому атомные массы элементов в периодической системе являются средним значением из массовых чисел природных смесей изотопов и отличаются от целочисленных значений. Таким образом, атомная масса природной смеси изотопов не может служить главной характеристикой атома, а следовательно, и элемента. Такой характеристикой атома является заряд ядра, определяющий число электронов в электронной оболочке атома и её строение.
Рассмотрим несколько типовых заданий по этому разделу.
Пример 1. Атом какого элемента имеет электронную конфигурацию 1s22s22p63s23p64s1?
- Li
- Na
- K
- Cl
На внешнем энергетическом уровне у данного элемента находится один 4s-электрон. Следовательно, этот химический элемент находится в четвёртом периоде первой группе главной подгруппе. Этот элемент — калий.
К этому ответу можно прийти по-другому. Сложив общее количество всех электронов, получим 19. Общее число электронов равно порядковому номеру элемента. Под номером 19 в периодической системе находится калий.
Пример 2. Химическому элементу соответствует высший оксид RO2. Электронной конфигурации внешнего энергетического уровня атома этого элемента соответствует электронная формула:
- ns2np4
- ns2np2
- ns2np3
- ns2np6
По формуле высшего оксида (смотрите на формулы высших оксидов в Периодической системе) устанавливаем, что этот химический элемент находится в четвёртой группе главной подгруппы. У этих элементов на внешнем энергетическом уровне находятся четыре электрона — два s и два p. Следовательно, правильный ответ 2.
Тренировочные задания
1. Общее число s-электронов в атоме кальция равно
1) 20
2) 40
3) 8
4) 6
2. Число спаренных p-электронов в атоме азота равно
1) 7
2) 14
3) 3
4) 4
3. Число неспаренных s-электронов в атоме азота равно
1) 7
2) 14
3) 3
4) 4
4. Число электронов на внешнем энергетическом уровне атома аргона равно
1) 18
2) 6
3) 4
4) 8
5. Число протонов, нейтронов и электронов в атоме 94Be равно
1) 9, 4, 5
2) 4, 5, 4
3) 4, 4, 5
4) 9, 5, 9
6. Распределение электронов по электронным слоям 2; 8; 4 — соответствует атому, расположенному в(во)
1) 3-м периоде, IА группе
2) 2-м периоде, IVА группе
3) 3-м периоде, IVА группе
4) 3-м периоде, VА группе
7. Химическому элементу, расположенному в 3-м периоде VA группе соответствует схема электронного строения атома
1) 2, 8, 6
2) 2, 6, 4
3) 2, 8, 5
4) 2, 8, 2
8. Химический элемент с электронной конфигурацией 1s22s22p4 образует летучее водородное соединение, формула которого
1) ЭН
2) ЭН2
3) ЭН3
4) ЭН4
9. Число электронных слоёв в атоме химического элемента равно
1) его порядковому номеру
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
10. Число внешних электронов в атомах химических элементов главных подгрупп равно
1) порядковому номеру элемента
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
11. Два электрона находятся во внешнем электронном слое атомов каждого из химических элементов в ряду
1) He, Be, Ba
2) Mg, Si, O
3) C, Mg, Ca
4) Ba, Sr, B
12. Химический элемент, электронная формула которого 1s22s22p63s23p64s1, образует оксид состава
1) Li2O
2) MgO
3) K2O
4) Na2O
13. Число электронных слоев и число p-электронов в атоме серы равно
1) 2, 6
2) 3, 4
3) 3, 16
4) 3, 10
14. Электронная конфигурация ns2np4 соответствует атому
1) хлора
2) серы
3) магния
4) кремния
15. Валентные электроны атома натрия в основном состоянии находятся на энергетическом подуровне
1) 2s
2) 2p
3) 3s
4) 3p
16. Атомы азота и фосфора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковую конфигурацию внешнего электронного слоя
4) одинаковое число электронов
17. Одинаковое число валентных электронов имеют атомы кальция и
1) калия
2) алюминия
3) бериллия
4) бора
18. Атомы углерода и фтора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковое число электронных слоёв
4) одинаковое число электронов
19. У атома углерода в основном состоянии число неспаренных электронов равно
1) 1
3) 3
2) 2
4) 4
20. В атоме кислорода в основном состоянии число спаренных электронов равно
1) 2
3) 4
2) 8
4) 6
Ответы
himi4ka.ru
Тема №1 «Строение атома» | CHEM-MIND.com
Оглавление
Электроны
Понятие атом возникло еще в античном мире для обозначения частиц вещества. В переводе с греческого атом означает «неделимый».
Ирландский физик Стони на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами, сущеетвующими в атомах всех химических элементов. В 1891 г. Стони предложил эти частицы назвать электронами, что по-гречески означает «янтарь». Через несколько лет после того, как электрон получил свое название, английский физик Джозеф Томсон и французский физик Жан Перрен доказали, что электроны несут на себе отрицательный заряд. Это наименьший отрицательный заряд, который в химии принят за единицу (-1). Томсон даже сумел определить скорость движения электрона (скорость электрона на орбите обратно пропорциональна номеру орбиты n. Радиусы орбит растут пропорционально квадрату номера орбиты. На первой орбите атома водорода (n=1; Z=1) скорость равна ≈ 2,2·106 м/с, то есть примерно в сотню раз меньше скорости света с=3·108 м/с.) и массу электрона (она почти в 2000 раз меньше массы атома водорода).

Состояние электронов в атоме
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона и пространстве, в котором он находится. Электрон в атоме не имеет траектории движения, т. е. можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра.
 Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
Он может находиться в любой части этого пространства, окружающего ядро, и совокупность его различных положений рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точек. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек будет больше всего.
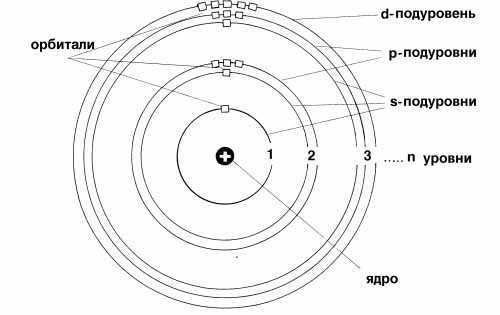
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью. В нем заключено приблизительно 90 % электронного облака, и это означает, что около 90 % времени электрон находится в этой части пространства. По форме различают 4 известных ныне типа орбиталей, которые обозначаются латинскими буквами s, p, d и f. Графическое изображение некоторых форм электронных орбиталей представлено на рисунке.
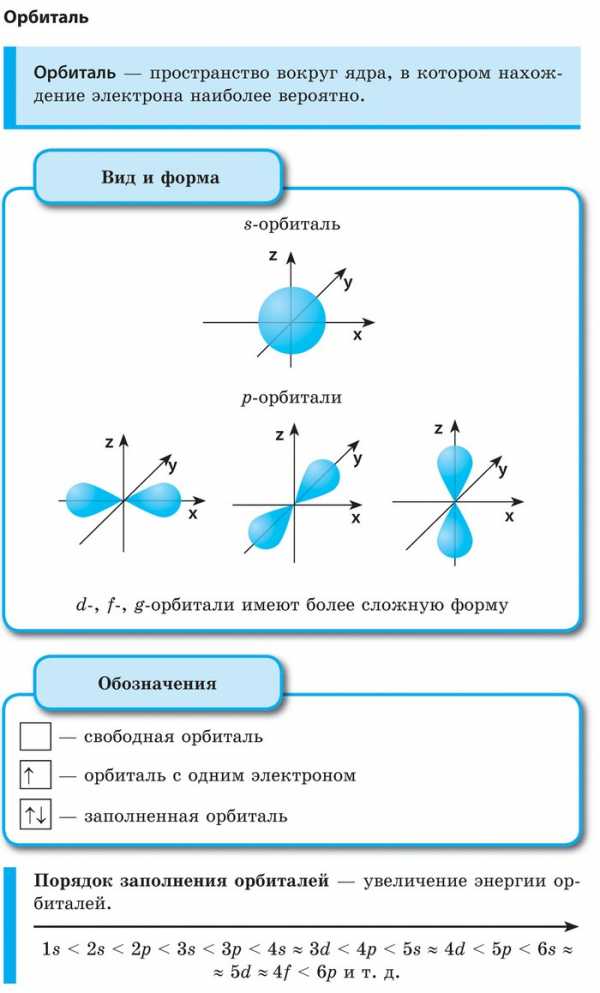
Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром. Электроны, обладающие близкими значениями энергии, образуют единый электронный слои, или энергетический уровень. Энергетические уровни нумеруют, начиная от ядра, — 1, 2, 3, 4, 5, 6 и 7.
Целое число n, обозначающее номер энергетического уровня, называют главным квантовым числом. Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня, электроны последующих уровней будут характеризоваться большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внешнего уровня.
Наибольшее число электронов на энергетическом уровне определяется по формуле:
N = 2n2,
где N — максимальное число электронов; n — номер уровня, или главное квантовое число. Следовательно, на первом, ближайшем к ядру энергетическом уровне может находиться не более двух электронов; на втором — не более 8; на третьем — не более 18; на четвертом — не более 32.
Начиная со второго энергетического уровня (n = 2) каждый из уровней подразделяется на подуровни (подслои), несколько отличающиеся друг от друга энергией связи с ядром. Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один подуровень; второй — два; третий — три; четвертый — четыре подуровня. Подуровни в свою очередь образованы орбиталями. Каждому значению n соответствует число орбиталей, равное n.
Подуровни принято обозначать латинскими буквами, равно как и форму орбиталей, из которых они состоят: s, p, d, f.
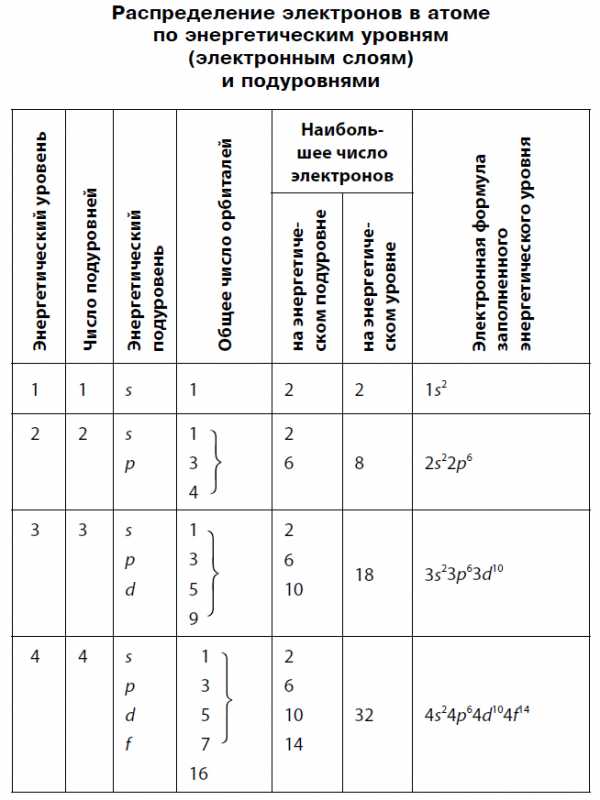
Протоны и нейтроны
Атом любого химического элемента сравним с крохотной Солнечной системой. Поэтому такую модель атома, предложенную Э. Резерфордом, называют планетарной
Атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов — протонов и нейтронов.
Протоны имеют заряд, равный заряду электронов, но противоположный по знаку (+1), и массу, равную массе атома водорода (она принята в химии за единицу). Нейтроны не несут заряда, они нейтральны и имеют массу, равную массе протона.
Протоны и нейтроны вместе называют нуклонами (от лат. nucleus — ядро). Сумма числа протонов и нейтронов в атоме называется массовым числом. Например, массовое число атома алюминия:
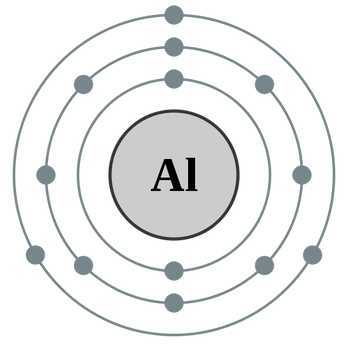
13 + 14 = 27
число протонов 13, число нейтронов 14, массовое число 27
Так как массой электрона, ничтожно малой, можно пренебречь, то очевидно, что в ядре сосредоточена вся масса атома. Электроны обозначают e—.
Поскольку атом электронейтрален, то также очевидно, что число протонов и электронов в атоме одинаково. Оно равно порядковому номеру химического элемента, присвоенному ему в Периодической системе. Масса атома складывается из массы протонов и нейтронов. Зная порядковый номер элемента (Z), т. е. число протонов, и массовое число (А), равное сумме чисел протонов и нейтронов, можно найти число нейтронов (N) по формуле:

N = A — Z
Например, число нейтронов в атоме железа равно:
56 — 26 = 30
Изотопы
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами. Химические элементы, встречающиеся в природе, являются смесью изотопов. Так, углерод имеет три изотопа с массой 12, 13, 14; кислород — три изотопа с массой 16, 17, 18 и т. д. Обычно приводимая в Периодической системе относительная атомная масса химического элемента является средним значением атомных масс природной смеси изотопов данного элемента с учетом их относительного содержания в природе. Химические свойства изотопов большинства химических элементов совершенно одинаковы. Однако изотопы водорода сильно различаются по свойствам из-за резкого кратного увеличения их относительной атомной массы; им даже присвоены индивидуальные названия и химические знаки.

Элементы первого периода
Схема электронного строения атома водорода:

Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).
Графическая электронная формула атома водорода (показывает распределение электронов по энергетическим уровням и подуровням):
Графические электронные формулы атомов показывают распределение электронов не только по уровням и подуровням, но и по орбиталям.
В атоме гелия первый электронный слой завершен — в нем 2 электрона. Водород и гелий — s-элементы; у этих атомов заполняется электронами s-орбиталь.
Элементы второго периода
У всех элементов второго периода первый электронный слой заполнен, и электроны заполняют s- и р-орбитали второго электронного слоя в соответствии с принципом наименьшей энергии (сначала s, а затем р) и правилами Паули и Хунда.
В атоме неона второй электронный слой завершен — в нем 8 электронов.
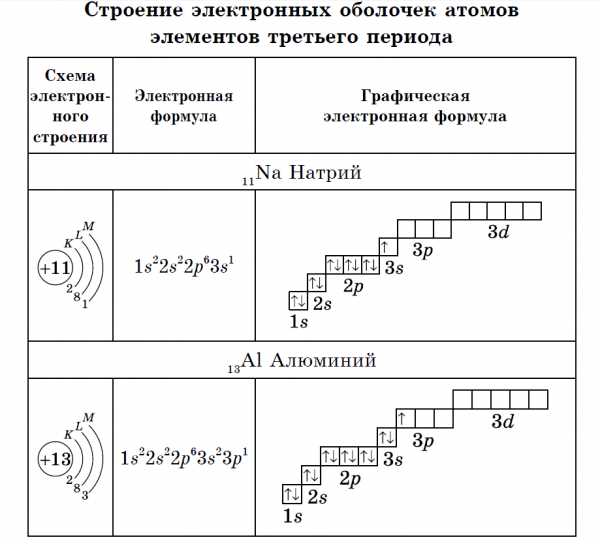
Элементы третьего периода
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d- подуровни.
У атома магния достраивается 3s- электронная орбиталь. Na и Mg — s-элементы.
У алюминия и последующих элементов заполняется электронами 3р-подуровень.
У элементов третьего периода остаются незаполненными 3d-орбитали.
Все элементы от Al до Ar — р-элементы. s- и р-элементы образуют главные подгруппы в Периодической системе.
Элементы четвертого — седьмого периодов
У атомов калия и кальция появляется четвертый электронный слой, заполняется 4s-подуровень, т. к. он имеет меньшую энергию, чем 3d-подуровень.
К, Са — s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами 3d-подуровень. Это 3d-элементы. Они входят в побочные подгруппы, у них заполняется предвнешний электронный слой, их относят к переходным элементам.
Обратите внимание на строение электронных оболочек атомов хрома и меди. В них происходит «провал» одного электрона с 4s- на 3d-подуровень, что объясняется большей энергетической устойчивостью образующихся при этом электронных конфигураций 3d5 и 3d10:
В атоме цинка третий электронный слой завершен — в нем заполнены все подуровни 3s, 3р и 3d, всего на них 18 электронов. У следующих за цинком элементов продолжает заполняться четвертый электронный слой, 4р-подуровень.
Элементы от Ga до Кr — р-элементы.
У атома криптона внешний слой (четвертый) завершен, имеет 8 электронов. Но всего в четвертом электронном слое может быть 32 электрона; у атома криптона пока остаются незаполненными 4d- и 4f-подуровни.У элементов пятого периода идет заполнение по-дуровней в следующем порядке: 5s — 4d — 5р. И так-же встречаются исключения, связанные с «провалом» электронов, у 41Nb, 42Мо, 44Ru, 45Rh, 46Pd, 47Ag.
В шестом и седьмом периодах появляются f-элементы, т. е. элементы, у которых идет заполнение соответственно 4f- и 5f-подуровней третьего снаружи электронного слоя.
4f-элементы называют лантаноидами.
5f-элементы называют актиноидами.
Порядок заполнения электронных подуровней в атомах элементов шестого периода:
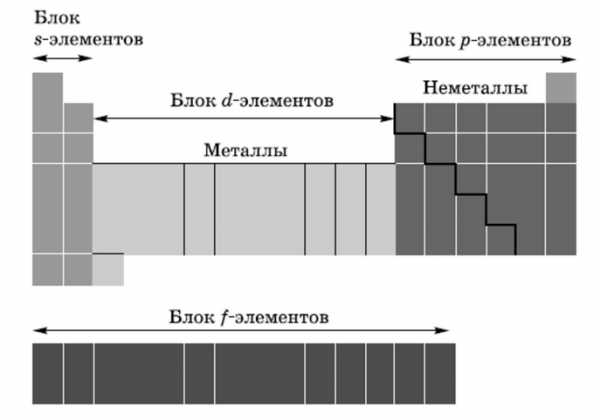
- s-элементы. Электронами заполняется s-подуровень внешнего уровня атома; к s-элементам относятся водород, гелий и элементы главных подгрупп I и II групп.
- p-элементы. Электронами заполняется р-подуровень внешнего уровня атома; к р-элементам относятся элементы главных подгрупп III— VIII групп.
- d-элементы. Электронами заполняется d-подуровень предвнешнего уровня атома; к d-элементам относятся элементы побочных подгрупп I—VIII групп, т. е. элементы вставных декад больших периодов, расположенных между s- и р-элементами. Их также называют переходными элементами.
- f-элементы. Электронами заполняется f-подуровень третьего снаружи уровня атома; к ним относятся лантаноиды и антиноиды.
Основное и возбужденное состояния
Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитали может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского — «веретено»), т. е. обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемый оси: по часовой или против часовой стрелки.
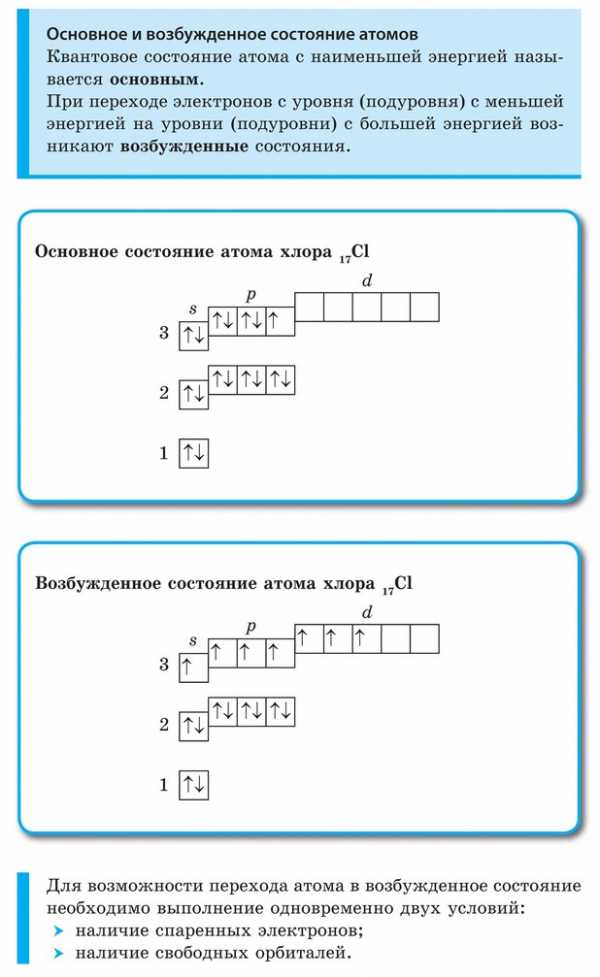
Этот принцип носит название принципа Паули. Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т. е. электроны с противоположными спинами. На рисунке показана схема подразделения энергетических уровней на подуровни и очередность их заполнения.
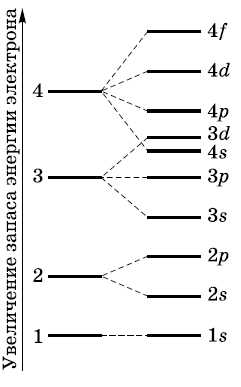

Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек — записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули и правило Ф. Хунда, согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины, при этом по принципу Паули будут уже противоположно направленными.
Правило Хунда и принцип Паули
Правило Хунда — правило квантовой химии, определяющее порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Другая формулировка: Ниже по энергии лежит тот атомный терм, для которого выполняются два условия.
- Мультиплетность максимальна
- При совпадении мультиплетностей суммарный орбитальный момент L максимален.
Разберём это правило на примере заполнения орбиталей p-подуровня p-элементов второго периода (то есть от бора до неона (в приведённой ниже схеме горизонтальными чёрточками обозначены орбитали, вертикальными стрелками — электроны, причём направление стрелки обозначает ориентацию спина).
При́нцип Па́ули (принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона (частицы с полуцелым спином) не могут одновременно находиться в одном и том же квантовом состоянии.
 Правило Хунда и принцип Паули
Правило Хунда и принцип ПаулиПравило Клечковского
Правило Клечковского — по мере увеличения суммарного числа электронов в атомах (при возрастании зарядов их ядер, или порядковых номеров химических элементов) атомные орбитали заселяются таким образом, что появление электронов на орбитали с более высокой энергией зависит только от главного квантового числа n и не зависит от всех остальных квантовых чисел, в том числе и от l. Физически это означает, что в водородоподобном атоме (в отсутствие межэлектронного отталкивания) орбитальная энергия электрона определяется только пространственной удаленностью зарядовой плотности электрона от ядра и не зависит от особенностей его движения в поле ядра.
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречатреальной энергетической последовательности атомых орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место “провал” электрона с s-подуровня внешнего слояна d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, аименно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d,а не 4f, и только затем происходит заселение четырнадцатью электронами 4f орбиталей, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и дляорбиталей 7s, 6d и 5f.
Распределение элекронов в атоме хрома — согласно правилам(сверху) и реальное(снизу), согласно исключениям из правила Клечковского:
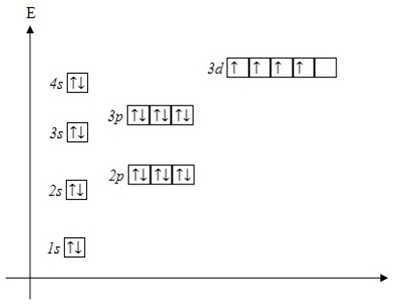
 Распределение элекронов в атоме меди — согласно правилам(сверху) и реальное(снизу), согласно исключениям из правила Клечковского:
Распределение элекронов в атоме меди — согласно правилам(сверху) и реальное(снизу), согласно исключениям из правила Клечковского:
Справочный материал для прохождения тестирования:
Таблица Менделеева Таблица растворимостиwww.chem-mind.com
Медь электронное строение — Справочник химика 21
Медь, серебро и золото несколько выпадают из общей для переходных металлов закономерности по своему электронному строению с валентной конфигурацией Они характеризуются более низкими температурами плавления и кипения, чем предшествующие им переходные элементы, и являются довольно мягкими металлами. Проявление таких свойств соответствует закономерной тенденции к ослаблению металлических связей, обнаруживаемой начиная с группы У1Б(Сг-Мо- У). Эта тенденция объясняется постепенным уменьшением числа неспаренных -электронов у атомов металлов второй половины переходных рядов. Медь, серебро и золото обладают очень большой электро- и теплопроводностью, поскольку их электронное строение обусловливает высокую подвижность 5-электронов. Эти металлы ковки, пластичны и инертны и могут находиться в природе в металлическом состоянии. Они встречаются довольно редко и поэтому имеют высокую стоимость, но все же распространены значительно больше, чем платиновые металлы. Относительно большая распространенность и возможность существования этих металлов в природе в несвязанном виде послужили причиной того, что они явились первыми металлами, с которыми познакомился чёловск и кошрые иН научился обрабатывать. По-видимому, первым металлом, который стали восстанавливать из его руды, была медь. Металлургия началась с открытия того, что сплав меди с оловом (естественно встречающаяся примесь) дает намного более твердый материал — бронзу. Медные предметы были найдены [c.446]Несмотря на сходство в электронном строении атомов, которые имеют один s-электрон над заполненной af-оболочкой, и высокие потенциалы ионизации, сходство между серебром, золотом и медью весьма ограниченно. Оно состоит в следующем [c.517]
Следует иметь в виду, что последняя схема (как и сами правила Клечковского) не отражает частных особенностей электронной структуры атомов некоторых элементов. Например, при переходе от атома никеля (2 = 28) к атому меди Z = 29) число Зй-электронов увеличивается не на один, а сразу на два за счет проскока одного из 4 -электронов на подуровень Зй. Таким образом, электронное строение атома меди выражается формулой Аналогичный проскок электрона с внешнего — на -подуровень предыдущего слоя происходит и в атомах аналогов меди — серебра и золота. Это явление связано с повышенной энергетической устойчивостью электронных структур, отвечающих полностью занятым энергетическим подуровням (см. 34). Переход электрона в атоме меди с подуровня 4х на подуровень Зс/ (и аналогичные переходы в атомах серебра и золота) приводит к образованию целиком заполненного -подуровня и поэтому оказывается энергетически выгодным. [c.98]
В дополнение следует указать, что важное значение имеет электронное строение металла наилучшими катализаторами гидрирования являются переходные металлы с незаполненными электронными уровнями в зонах 3 , и 5[c.382]
Известны соединения меди в степенях окисления +1, +2 и +3. Последние, однако, малочисленны и ограничиваются простми и сложными оксидами и фторидами. Гораздо более распространены соединения меди (I) и меди (II). Соединения одновалентной меди менее устойчивы и похожи на аналогичные соединения серебра и золота (I). Соли двухвалентной меди по свойствам гораздо ближе к солям других двухзарядпых катионов переходных металлов. Эти особенности меди неразрывно связаны с ее электронным строением. Основное состояние атома меди 3[c.159]
Электролиз расплавленных солей подчиняется тем же основным законам, которые выведены для электрохимии водных растворов. Ток через расплавленные соли проходит так же, как и в водных растворах электролитов, с помощью ионов, поэтому электролиз солевых расплавов подчиняется законам Фарадея. Электропроводность солевых расплавов при высоких температурах несколько выше, чем электропроводность водных электролитов при комнатной температуре. Положение металлов в ряде напряжений для расплавленных солей [364] и в водных электролитах принципиально мало различается между собой. Как и в водных растворах, наиболее отрицательные значения электродных потенциалов имеют щелочные и щелочноземельные металлы более положительные потенциалы имеют сурьма, висмут, медь, ртуть и серебро. Электродные потенциалы одних и тех же металлов в расплавленных хлоридах, бромидах и йодидах сравнительно мало отличаются. Это объяснимо, если считать, что электродные потенциалы металлов в основном определяются, электронным строением атомов, т. е. положением их в периодической системе элементов Д. И. Менделеева. Как и в водных электролитах, электроосаждение металлов из солевых расплавов протекает с поляризацией, однако степень ее значительно меньше, чем в водных растворах. Электролиз расплавленных солей проводится при высоких температурах в электролизерах, обычно имеющих огнеупорную футеровку, диафрагму, отделяющую анодное пространство от катодного. В ряде случаев необходима герметизация электролизера или защитная атмосфера. [c.102]
Эти особенности меди неразрывно связаны с ее электронным строением. Основное состояние атома меди. Зс/ °4 обусловлено устойчивостью заполненной й-оболочки (ср. с атомом хрома), однако первое возбужденное состояние превышает основное по энергии всего на 1,4 эВ (около 125 кДж/моль). Поэтому в химических соединениях проявляются в одинаковой мере оба состояния, дающие начало двум рядам соединений меди (I) и (II). [c.159]
Резкая разница в электронном строении двух атомов также препятствует образованию твердых растворов и способствует появлению двух жидких слоев илиэвтектик. Так, например, в системах Си — V, Сг, Мо, образуются два жидких слоя, в системе Си — Т1 — эвтектика. Аналогично меди ведет себя серебро с вышеперечисленными металлами. Та же картина наблюдается в системах Си и Ад с далеко отстоящими от них металлами VI П-а подгруппы. [c.286]
Подобно меди, эти элементы имеют один -электрон сверх заполненной -оболочки, и, несмотря на сходство электронного строения и близкие значения потенциалов ионизации, между А , Ли и Си можно найти сравнительно мало общего, а большинство различий до сих пор не имеет простого объяснения. [c.476]
Этими правилами определяется порядок заполнения орбиталей электронами и образование характерных электронных конфигураций атомов, что и отражено в приведенной периодической системе Д. И. Менделеева. Однако необходимо иметь в виду, что правила Клечковского не полностью охватывают все частные особенности электронной структуры атомов. Например, при переходе от атома никеля к атому меди число Зй-электронов увеличивается не на один, а сразу на два электрона за счет проскока одного 45-электрона на подуровень Зй. Таким образом, электронное строение атома меди выражается формулой 15 28 2р 35 3/7 3 г 45 . Аналогичный провал электрона с внешнего 5- на р-подуровень происходит и в атомах [c.18]
В кристаллохимии следует различать локальный и коллектив-, ный аспекты. Первый заключается в выявлении стереохимии отдельных структурных элементов кристалла, в то время как коллективный аспект учитывает их взаимодействие между собой и упаковку в кристалле. Оба аспекта одинаково важны в объяснении происхождения кристаллической структуры и ее свойств, хотя в литературе по кристаллохимии до сих пор обычно отдается предпочтение коллективному (кристаллическому) аспекту. Больше всего электронное строение влияет на кристаллохимию через ее локальный аспект и примером этого служит рассмотренная выше зависимость координации от электронных свойств ц. а. и лигандов. В следующем разделе это утверждение иллюстрируется также на примере анализа происхождения изомеров двухвалентной меди. [c.284]
Электронное строение примесей меди в ZnO. [c.216]
Lo] и [ uo] — соответственно концентрации лиганда и меди в растворе), будут представлять собой наложение спектров ЭПР нескольких различных комплексов. Интерпретация таких спектров как спектров индивидуальных соединений uL может привести к ошибочным выводам о значениях -фактора и констант СТС для этих соединений. Из сказанного выше следует, что исследование влияния ступенчатого характера комп-лексообразования на спектры ЭПР комплексов является необходимым этапом в изучении электронного строения этих соединений [64—68]. [c.146]
Америций (5/ 6s 6p 7s ) по имеющимся данным имеет гексагональную плотную упаковку типа a-La и, вероятно, должен переходить в объемноцентрированную кубическую форму при повышении температуры вследствие перекрытия и обменного взаимодействия внешних р -оболочек. Ввиду идентичности электронного строения и возрастания энергии связи 5/-электронов по мере увеличения их числа можно ожидать, что кристаллические структуры и модификации тяжелых актиноидов, от кюрия до лоуренсия, будут изоморфны структурам их аналогов — тяжелых лантаноидов, от гадолиния до лютеция. При этом их плотные упаковки могут быть не только типа магния, но и типов а-лантана и меди, а высокотемпературные объемноцентрированные кубические фазы, вероятно, могут появляться при более низких температурах. [c.241]
Решение. При одинаковых зарядах и размерах ионов Na и Си+ различие в их поляризующем действии определяется особенностями нх электронного строения. Ион Си+ имеет 18-элск-тронную внешнюю оболочку н более сильно поляризует анион С1 , чем ион N3+, обладающий благородногазовой электронной структурой. Поэтому в хлориде меди(1) в результате поляриза- [c.68]
Не только магнитные, но и каталитические свойства разбавленных атомизированных слоев металлических катализаторов на дисперсных носителях Существенно определяются электронной структурой атома — его местом в периодической системе Менделеева и наличием холостых электронов. Роль электронного строения атомов в разведенных слоях особенно отчетливо проявляется при катализе смешанными слоями и в явлении спинового отравления , найденного Зубовичем [53]. При этом адсорбционные катализаторы, содержащие весьма каталитически активные атомы с неспаренными электронами, например атомы серебра, начинают сильно снижать (иногда почти до нуля) каталитическую способность других также весьма активных атомов с неспаренными электронами, например Р1. Этот вид взаимного отравления в результате спаривания электронов контрастно проявляется в смешанных слоях серебра с платиной и палладием при распаде перекиси водорода. Также действуют атомы меди, обладающие одним неспаренным электроном, но ионы меди, лишенные этого электрона, почти не оказывают токсического действия. Резкий провал парамагнитизма слоя в области отравления и его рост в области активации экапериментально демонстрирует определяющую роль спин-валентности в катализе. [c.27]
Часто каталитическая активность металлов сопоставляется с наличием вакансий в -зоне металла. Так, для реакций с участием молекулярного водорода (гидрирование, дейтеро-водородный обмен, о-п-превращение) Боресковым 114] было установлено, что удельная каталитическая активность растет с заполнением -зоны металла, т. е. с уменьшением числа неспаренных электронов в -зоне, и достигает максимума у последних металлов VHI группы периодической системы элементов. Завершение заполнения -зоны при переходе от никеля к меди или от платины к золоту приводит к резкому снижению каталитической активности. При полном заполнении -уровней металлы совсем теряют каталитическую активность. Используя в качестве характеристики электронного строения переходных металлов критерий недостроенности их -электронного подуровня , Самсонов [115] получил удовлетворительную корреляцию между этой величиной и скоростью гидрирования этилена на пленках различных металлов. [c.64]
Не менее интересно рассмотреть переходную облас гь между /- и /-металлами. Лютеций и лоуренсий, завершающие ряд лантаноидов и актиноидов, имеют валентно-электронную конфигурацию (п—2)/ (п—1)с1 п5 . Предыдущие элементы иттербий у элемент 102 также имеют завершенную /-электронную оболочку (п — —2)/ я5 а электроны на п—1)с(-уровне отсутствуют. В соответствии с электронным строением отмеченные 4 элемента в основном состоянии, строго говоря, не могут быть отнесены к /-элементам, поскольку сформированный / -электронный слой обладает повышенной стабильностью и во взаимодействии может не участвовать. Действительно, для иттербия, например, весьма характерны производные со степенью окисления +2, а для лютеция и лоур( нсия, как и следовало ожидать, 4-3. В то же время иттербий в стегени окисления + 3 выступает как типичный /-элемент. Таким образом, на границе между /- и /-элементами наблюдается такая же двойственность в поведении, как и у элементов подгруппы мед и цинка при переходе от /- к 5р-металлам. [c.368]
Свойства меди и ее соединений. Медь — элемент I группы В подгруппы Периодической системы Д. И. Менделеева. Электронное строение атомов в основном состоянии ls 2s 2p 3s 3p 3d 4s Наиболее устойчивая степень окисления атома 4-2, менее устойчивая -fl. Известны соедпне чия Си (1П), которые считаются сильными окислителями. [c.83]
Исследование сплавов никеля и меди разного состава, а следовательно, с разным весом -состояний, позволило установить влияние электронного строения на адсорбцию и механизм электровосстановления п-нитробензойной кислоты. На сплавах, содержащих больше 60% никеля, энергия активаций ниже, что указывает на ослабление связи металл — водород и на электрокаталитический механизм восстановления адсорбированным водородом. При переходе к сплавам с ме ньшйм содержанием никеля возрастает доля тока, расходуемая на восстановление органического вещества по электронному механизму [55], [c.29]
Магнитные свойства кластеров определяются такими факторами, как электронная конфигурация металла, расстояние металл — металл, электронное строение анионов и других связанных с металлом лигандов, а также геометрическим расположением атомов металла и лигандов. Например, двухъядерный моногидрат ацетата хрома(П) (рис. 1) с конфигурацией металла й диамагнитен, тогда как аналогичный комплекс меди(И) с конфигурацией парамагнитен [1], несмотря на то, что оба соединения изоструктурны [2]. Очень небольшие отличия в стереохимии [3—5] димерных анионов [Сг2С19] и приводят к тому, что первый из них пара- [c.293]
Типичными примерами такой двухуровневой парамагнитной восприимчивости могут служить широко исследованные двуядерные соединения меди с монокарбоновыми кислотами [239], в которых два неспаренных электрона ионов Си + благодаря непосредственной связи Си—Си образуют основное синглетное состояние 5 = 0 и близколежащее возбужденное триплетное состояние 5 = 1 (более детально электронное строение и происхождение связи в этих системах см. в работе [108]). В этом случае, следовательно, д,(1)эфф 0 и уравнение (VI. 13) упрощается yi = ае и г/г = —1 + л . Если предположить, что триплетное состояние отличается от основного синглетного только спином, то а = (gilgi) = 3 и пересечение yi и происходит при = A/feTi 1,6 это позволяет непосредственно найти А, если известны из опыта температуры максимума магнитной восприимчивости для двуядерного ацетата меди А 300 см [240]. [c.150]
Положительные и отрицательные количества электричества. Электрон. Строение ато.ма ). До сих пор мы рассматривали электрический ток, проводя аналогию с потоком жидкости такой способ особенно полезен для начала и облегчает понимание явлений. В действительности же отношения здесь значительно сложнее. Если включить в цепь раствор хлористой меди таким образом, как было указано выше, то на одной платиновой пластинке наблюдается выделение металлической меди, на другой — выделение хлора. С одной стороны, выделение меди приводит нас к представлению, что растворенная в жидкости медь переносится электрическим током к одному электроду и там осаждается, с другой стороны, — выде- [c.16]
Изучение методом ЭПР электронного строения комплексов бис-малеонитрилдитиолат-меди(П), -никеля(1П), -кобаль-та(П) и -родия(П). [c.197]
Электронное строение плоских квадратных комплексов металлов. П. Комплексы малеонитрилдитиолата с медью(П), никелем(П), палладием(П) и платиной(И). [c.201]
В основном состоянии элементы подгруппы меди имеют строение внешних электронных оболочек Зс( 45(Си), 4с( 5 (Ag), (Аи) и одновалентны. Возбуждение ближайших потенциально трехвалентных состояний Си (3(з М54р), А5 4ё 5 5р) и Аи (5й 05бр) требует затраты соответственно 111, 161 и 120 ккал/г-атом. Последовательные ионизационные потенциалы Си равны 7,72 20,29 36,83 в, А —7,57 21,48 34,82 8, Аи — 9,22 20,5 (30,5) б. Сродство атомов к электрону составляет 35 (Си), 46 (А ), 65 (Аи) ккал/г-атом, т. е. золото в этом отношении не очень отличается от галоидов (VII 4). [c.44]
chem21.info
Строение электронных оболочек атомов элементов первых четырех периодов периодической системы Д. И. Менделеева — ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ — ХИМИЯ — УНИВЕРСАЛЬНЫЙ СПРАВОЧНИК ШКОЛЬНИКА
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
Строение электронных оболочек атомов элементов первых четырех периодов периодической системы Д. И. Менделеева
Элементы первого периода
Схема электронного строения атома водорода:
Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).
Электронная формула атома водорода (читается: один-эс-один):
Графическая электронная формула атома водорода (показывает распределение электронов по энергетическим уровням и подуровням):
Графические электронные формулы атомов показывают распределение электронов не только по уровням и подуровням, но и по орбиталям.
В атоме гелия первый электронный слой завершен — в нем 2 электрона.
Водород и гелий — s-элементы; у этих атомов заполняется электронами s-орбиталь.
Элементы второго периода
У всех элементов второго периода первый электронный слой заполнен, и электроны заполняют s- и р-орбитали второго электронного слоя в соответствии с принципом наименьшей энергии (сначала s, а затем р) и правилами Паули и Хунда.
В атоме неона второй электронный слой завершен — в нем 8 электронов.
Элементы третьего периода
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d-подуровни (табл. 1).
Таблица 1
Строение электронных оболочек атомов элементов третьего периода
Схема электронного строения | Электронная формула | Графическая электронная формула |
11Na Натрий | ||
13Al Алюминий | ||
У атома магния достраивается 3s-электронная орбиталь. Na и Mg — s-элементы.
У алюминия и последующих элементов заполняется электронами 3р-подуровень.
У элементов третьего периода остаются незаполненными 3d-орбитали.
Все элементы от Al до Ar — р-элементы. s- и p-элементы образуют главные подгруппы в Периодической системе.
Элементы четвертого — седьмого периодов
У атомов калия и кальция появляется четвертый электронный слой, заполняется 4s-подуровень, т. к. он имеет меньшую энергию, чем 3d-подуровень.
К, Са — s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами 3d-подуровень. Это 3d-элементы. Они входят в побочные подгруппы, у них заполняется предвнешний электронный слой, их относят к переходным элементам.
Обратите внимание на строение электронных оболочек атомов хрома и меди. В них происходит «провал» одного электрона с 4s- на 3d-подуровень, что объясняется большей энергетической устойчивостью образующихся при этом электронных конфигураций 3d5 и 3d10:
В атоме цинка третий электронный слой завершен — в нем заполнены все подуровни 3s, 3р и 3d, всего на них 18 электронов. У следующих за цинком элементов продолжает заполняться четвертый электронный слой, 4р-подуровень.
Элементы от Ga до Кr — р-элементы.
У атома криптона внешний слой (четвертый) завершен, имеет 8 электронов. Но всего в четвертом электронном слое может быть 32 электрона; у атома криптона пока остаются незаполненными 4d- и 4f-подуровни.
У элементов пятого периода идет заполнение подуровней в следующем порядке: 5s → 4d → 5р. И также встречаются исключения, связанные с «провалом» электронов, у 41Nb, 42Мо, 44Ru,45Rh, 46Pd, 47Ag.
В шестом и седьмом периодах появляются f-элементы, т. е. элементы, у которых идет заполнение соответственно 4f- и 5f-подуровней третьего снаружи электронного слоя.
4f-элементы называют лантаноидами.
5f-элементы называют актиноидами.
Порядок заполнения электронных подуровней в атомах элементов шестого периода: 55Cs и 56Ва — 6s-элементы; 57La … 6s25d1 — 5d-элемент; 58Се — 71Lu — 4f-элементы; 72Hf — 80Hg — 5d-элементы; 81Тl — 86Rn — 6d-элементы. Но и здесь встречаются элементы, у которых «нарушается» порядок заполнения электронных орбиталей, что, например, связано с большей энергетической устойчивостью наполовину и полностью заполненных f-подуровней, т. е. nf7 и nf14.
В зависимости от того, какой подуровень атома заполняется электронами последним, все элементы делят на четыре электронных семейства, или блока (рис. 4):
1. s-элементы. Электронами заполняется s-подуровень внешнего уровня атома; к s-элементам относятся водород, гелий и элементы главных подгрупп I и II групп.
2. p-элементы. Электронами заполняется р-подуровень внешнего уровня атома; к р-элементам относятся элементы главных подгрупп III- VIII групп.
3. d-элементы. Электронами заполняется d-подуровень предвнешнего уровня атома; к d-элементам относятся элементы побочных подгрупп I—VIII групп, т. е. элементы вставных декад больших периодов, расположенных между s- и р-элементами. Их также называют переходными элементами.
4. f-элементы. Электронами заполняется f-подуровень третьего снаружи уровня атома; к ним относятся лантаноиды и антиноиды.
Рис. 4. Блоки химических элементов
Электронная конфигурация атома. Основное и возбужденное состояния
Швейцарский физик В. Паули в 1925 г. установил, что в атоме на одной орбитали может находиться не более двух электронов, имеющих противоположные (антипараллельные) спины (в переводе с английского — «веретено»), т. е. обладающих такими свойствами, которые условно можно представить себе как вращение электрона вокруг своей воображаемый оси: по часовой или против часовой стрелки. Этот принцип носит название принципа Паули. Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т. е. электроны с противоположными спинами.
На рис. 5 показана схема подразделения энергетических уровней на подуровни.
Рис. 5. Схема подразделения энергетических уровней
Очень часто строение электронных оболочек атомов изображают с помощью энергетических или квантовых ячеек — записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули и правило Ф. Хунда, согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, а лишь затем спариваются, но спины при этом по принципу Паули будут уже противоположно направленными.
compendium.su
Строение электронных оболочек атомов
Осознание содержания этого пункта позволяет:
объяснять значение понятий «электронная оболочка атома», «квантовое число», «электронная конфигурация атома»; характеризовать закономерности распределения электронов в атомах; составлять схемы строения атомов, электронные формулы атомов химических элементов и электронно — графические формулы.
Вспомним, что атом состоит из ядра и электронной оболочки, то есть совокупности движущихся в атоме у ядра. Электрон в атоме можно представить как облако с определенной плотностью отрицательного электрического заряда в определенном объеме пространства вокруг ядра. Такое пространство, в котором пребывания электрона скорее, называется атомной орбиталью.
Орбитали располагаются на определенных расстояниях от ядра, имеют определенную форму и ориентацию в пространстве. Для их характеристики используют набор квантовых чисел, которых четыре. Каждое из них все больше уточняет состояние электрона в атоме, его местонахождение в электронной оболочке.
Главное квантовое число n определяет номер энергетического уровня (электронного слоя), на котором размещается электрон, а также энергию электрона в атоме и степень его удаленности от ядра.
Энергетический уровень — это совокупность орбиталей, характеризующихся одинаковым значением главного квантового числа n
Главное квантовое число приобретает целочисленных значений, начиная единицы (n = 1, 2, 3,… да). Чем больше n тем больше будет энергия.
С числом n соединены и другие характеристики энергетического уровня. Например, число подуровней на энергетическом уровне равна n — номера уровня, а число орбиталей на энергетическом уровне n — квадрату номера уровня n2. Итак, максимальное число электронов, которые могут разместиться на n — м уровне (по два на каждой орбитали), равна 2n2.
Побочное (орбитальное) квантовое число l определяет форму атомной орбитали (АО), на котором размещен электрон. Оно может принимать целочисленных значений от 0 до nl (подуровни обозначаются буквами).
Поскольку электроны имеют разный запас энергии, они размещаются в атоме на разном расстоянии от ядра, образуя электронные слои. Каждому электронному слоя соответствует определенный уровень энергии электронов, размещаемых на нем, поэтому электронные слои называют еще энергетическими уровнями.
Число энергетических уровней в атоме элемента соответствует главному квантовому числу n, т.е. номера периода в периодической системе. Энергетические уровни атомов обозначаются также латинскими буквами К, L, M, N, O, P, Q.
Каждый энергетический уровень делится на подуровни, число которых равно номеру уровня.
На одной орбитали может быть только два электрона с противоположными спинами.
Электроны размещаются сначала по одному на каждой из орбиталей, а затем — по два.
Распределение электронов в атоме по орбиталях на энергетических уровнях и подуровнях называется электронной конфигурацией атома. Графически она передается с помощью электронных формул или квантовых ячеек. Для составления электронной конфигурации атома следует помнить определенные принципы и правила.
категория: Химияmoykonspekt.ru
Строение электронных оболочек атомов » HimEge.ru
Атомы, первоначально считавшиеся неделимыми, представляют собой сложные системы.
•Атом состоит из ядра и электронной оболочки
•Электронная оболочка – совокупность движущихся вокруг ядра электронов
•Ядра атомов заряжены положительно, они состоят из протонов (положительно заряженных частиц) p+ и нейтронов (не имеющих заряда) no
•Атом в целом электронейтрален, число электронов е– равно числу протонов p+, равно порядковому номеру элемента в таблице Менделеева.
На рисунке изображена планетарная модель атома, согласно которой электроны движутся по стационарным круговым орбитам. Она очень наглядна, но не отражает сути, т.к в действительности законы микромира подчиняются на классической механике, а квантовой, которая учитывает волновые свойства электрона.
Согласно квантовой механике электрон в атоме не движется по определенным траекториям, а может находиться в любой части околоядерного пространства, однако вероятность его нахождения в разных частях этого пространства неодинакова.
Пространство вокруг ядра, в котором вероятность нахождения электрона достаточно велика, называют орбиталью (не путать с орбитой!) или электронным облаком.
Т.е у электрона отсутствует понятие «траектория», электроны не движутся ни по круговым орбитам, ни по каким-либо другим. Самая большая сложность квантовой механики заключается в том, что это невозможно представить, мы все привыкли к явлениям макромира, подчиняющегося классической механике, где любая движущаяся частица имеет свою траекторию.
Итак, электрон имеет сложное движение, может находится в любом месте пространства около ядра, но с разной вероятностью. Давайте теперь рассмотрим те части пространства, где вероятность нахождения электрона достаточно высока — орбитали — их формы и последовательность заполнения орбиталей электронами.
Представим себе трехмерную систему координат, в центре которой находится ядро атома.
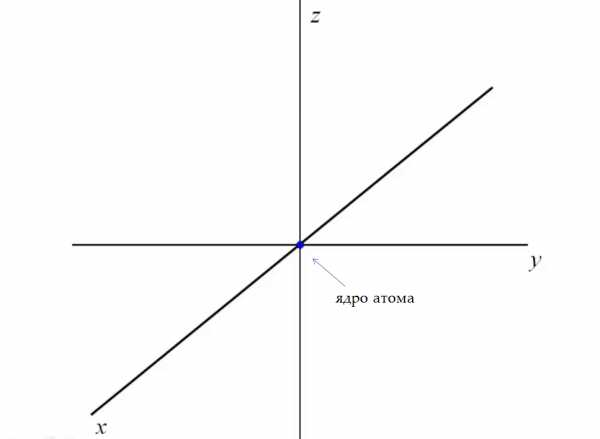
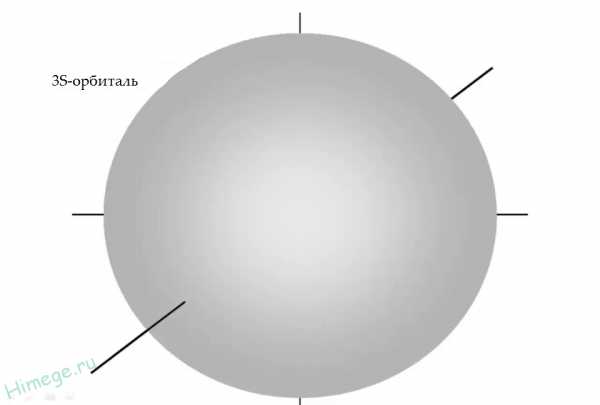
Вначале идет заполнение 1s орбитали, она располагается ближе всего к ядру и имеет форму сферы.
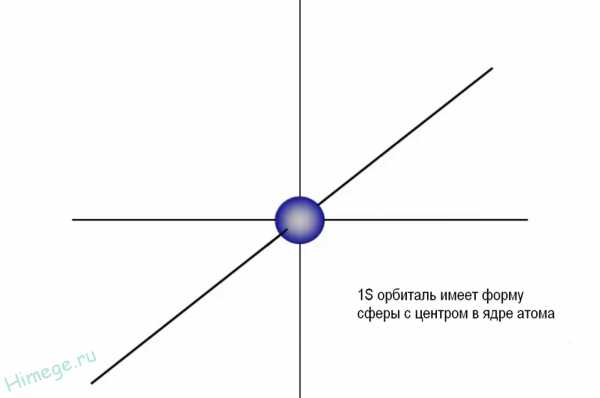
Обозначение любой орбитали складывается из цифры и латинской буквы. Цифра показывает уровень энергии, а буква — форму орбитали.
1s орбиталь имеет наименьшую энергию и электроны находящиеся на этой орбитали имеют наименьшую энергию.
На этой орбитали могут находиться не более двух электронов. Электроны атомов водорода и гелия (первых двух элементов) находятся именно на этой орбитали.
Электронная конфигурация водорода: 1s1
Электронная конфигурация гелия: 1s2
Верхний индекс показывает количество электронов на этой орбитали.
Следующий элемент — литий, у него 3 электрона, два из которых располагаются на 1s орбитали, а где же располагается третий электрон?
Он занимает следующую по энергии орбиталь — 2s орбиталь . Она также имеет форму сферы, но большего радиуса (1s орбиталь находится внутри 2s орбитали).

Электроны, находящиеся на этой орбитали имеют большую энергию, по сравнению с 1s орбиталью, т.к они расположены дальше от ядра. Максимум на этой орбитали может находится также 2 электрона.
Электронная конфигурация лития: 1s2 2s1
Электронная конфигурация бериллия: 1s2 2s2
У следующего элемента — бора — уже 5 электронов, и пятый электрон будет заполнять орбиталь, обладающую ещё большей энергией- 2р орбиталь. Р-орбитали имеют форму гантели или восьмерки и располагаются вдоль координатных осей перпендикулярно друг другу.

На каждой р-орбитали может находится не более двух электронов, таким образом на трех р-орбиталях — не более шести. Валентные электроны следующих шести элементов заполняют р-орбитали, поэтому их относят к р-элементам.
Электронная конфигурация атома бора: 1s2 2s2 2р1
Электронная конфигурация атома углерода: 1s2 2s2 2р2
Электронная конфигурация атома азота: 1s2 2s2 2р3
Электронная конфигурация атома кислорода: 1s2 2s2 2р4
Электронная конфигурация атома фтора: 1s2 2s2 2р5
Электронная конфигурация атома неона: 1s2 2s2 2р6
Графически электронные формулы этих атомов изображены ниже:
Квадратик — это орбиталь или квантовая ячейка, стрелочкой обозначается электрон, направление стрелочки — это особая характеристика движения электрона — спин (упрощенно можно представить как вращение электрона вокруг своей оси по часовой и против часовой стрелки). Нужно знать то, что на одной орбитали не может быть двух электронов с одинаковыми спинами (в одном квадратике нельзя рисовать две стрелочки в одном направлении!). Это и есть принцип запрета В.Паули: «В атоме не может быть даже двух электронов, у которых все четыре квантовых числа были бы одинаковыми»
Существует ещё одно правило (правило Гунда), по которому электроны расселяются на одинаковых по энергии орбиталях сначала по одиночке, и лишь когда в каждой такой орбитали уже находится по одному электрону, начинается заполнение этих орбиталей вторыми электронами. Когда орбиталь заселяется двумя электронами, такие электроны называют спаренными.
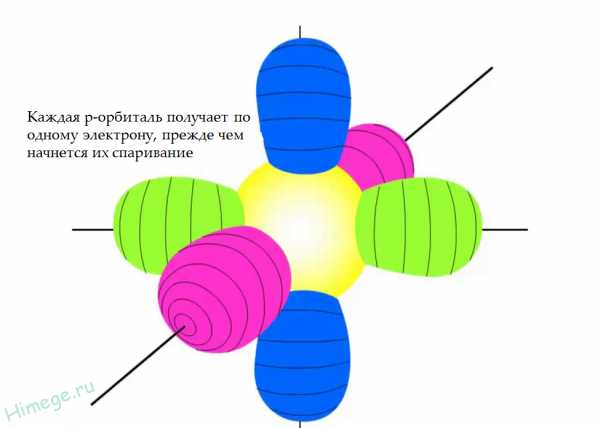
Атом неона имеет завершенный внешний уровень из восьми электронов (2 s-электрона+6 p-электронов =8 электронов на втором энергетическом уровне), такая конфигурация является энергетически выгодной, и её стремятся приобрести все другие атомы. Именно поэтому элементы 8 А группы — благородные газы — столь инертны в химическом отношении.
Следующий элемент — натрий, порядковый номер 11, первый элемент третьего периода, у него появляется ещё один энергетический уровень — третий. Одиннадцатый электрон будет заселять следующую по энергии орбиталь -3s орбиталь.
Электронная конфигурация атома натрия: 1s2 2s2 2р6 3s1
Далее происходит заполнение орбиталей элементов третьего периода, сначала заполняется 3s подуровень с двумя электронами, а потом 3р подуровень с шестью электронами (аналогично второму периоду) до благородного газа аргона, имеющего, подобно неону, завершенный восьмиэлектронный внешний уровень. Электронная конфигурация атома аргона (18 электронов): 1s2 2s2 2р6 3s2 3р6
Четвертый период начинается с элемента калия (порядковый номер 19), последний внешний электрон которого располагается на 4s орбитали. Двадцатый электрон кальция также заполняет 4s орбиталь.
За кальцием идет ряд из 10 d-элементов, начиная со скандия (порядковый номер 21) и заканчивая цинком (порядковый номер 30). Электроны этих атомов заполняют 3d орбитали, внешний вид которых представлен на рисунке ниже.
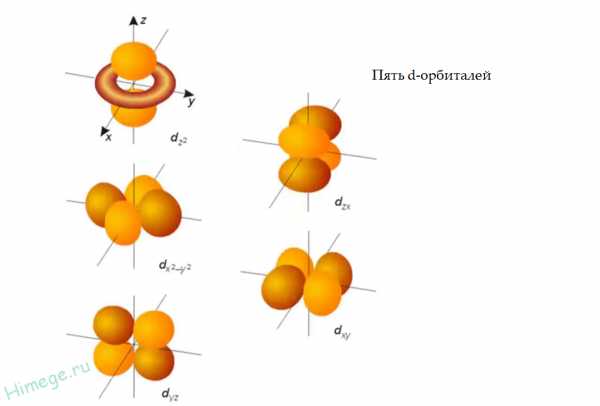
Далее идут шесть р-элементов (происходит заполнение 4р орбиталей). Заканчивается четвертый период инертным газом криптоном, электронная конфигурация которого 1s2 2s2 2р6 3s2 3p6 4s2 3d10 4р6
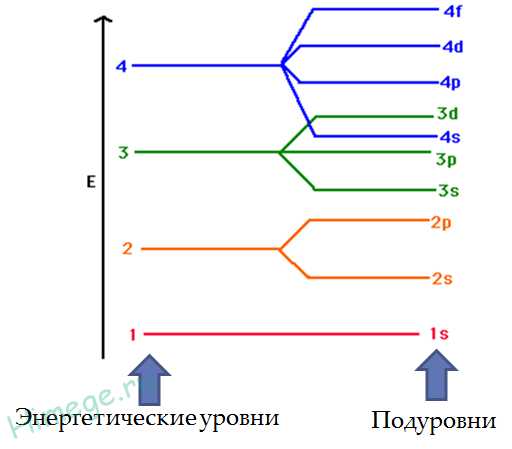 Итак, подведем итоги:
Итак, подведем итоги:
- Энергетические уровни соответствуют номеру периода. Энергетические уровни делятся на подуровни (первый уровень состоит из одного подуровня, второй уровень из двух подуровней, третий — из трех и т.д).
- s подуровень состоит из одной s орбитали, p подуровень — из трех р орбиталей, d подуровень из 5 d орбиталей.
- На каждой орбитали может находится не более двух электронов.

Смотрите также Атомная теория
и явление «проскока» электрона.
himege.ru
СТРОЕНИЕ ЭЛЕКТРОННЫХ ОБОЛОЧЕК АТОМОВ — МегаЛекции
Институт нефти, газа, энергетики и безопасности
Кафедра неорганической химии
Неорганическая химия
Конспект лекций
СТРОЕНИЕ АТОМА
До конца 19 века считалось, что атомы являются неделимыми час-тицами, однако открытие катодных лучей, термоэлектронной эмиссии, фо-тоэффекта, явления радиоактивности, говорило о том, что атом частица сложная. В начале ХХ века появляются первые модели строения атома, которые были предложены Резерфордом, Бором, Зоммерфельдом, однако недостатком всех этих теорий было то, что их авторы пытались применить к микрообъектам законы классической механики, которым они не подчиняют-ся.
Было установлено что атом состоит из ядра и электронной оболочки. Ядро имеет положительный заряд. Величина заряда определяется числом протонов. Каждый протон имеет единичный положительный заряд. Кроме протонов в состав ядра входят электронейтральные частицы — нейтроны. Их общее название — нуклоны.
Число нуклонов называется массовым числом атомов, его обозначают символом А:
А=Z+N
где Z- число протонов, а N- число нейтронов.
Массовое число приблизительно равно массе атома, так как масса электронов незначительна, и ею можно пренебречь. Порядковый номер элемента в таблице Менделеева соответствует числу протонов в ядре (Z), т.е. он соответствует заряду ядра, следовательно разность между массовым числом (А) и его порядковым номером является числом нейтронов (N).
N=A-Z
Для одного и того же элемента атом всегда содержит определённое число протонов, а число нейтронов является различным. Значит один и тот же элемент может иметь разные массовые числа. Атомы, имеющие одинаковое число протонов (Z), но разное число нейтронов (N), называются изотопами.
Массовые числа элементов, указываемые в периодической таблице, яв-ляются средней арифметической величиной масс всех изотопов элементов и поэтому часто имеют дробные значения.
Ядро атома не участвует в химических реакциях. Химические свойства элементов определяются только числом электронов и строением их элект-ронной оболочки.
Современная теория строения атома базируется на законах квантовой механики, одним из важнейших положений которой является представле-ние о двойственной природе быстро движущихся микрообъектов , которые проявляют себя и как частицы, и как волны. Впервые дуализм свойств мик-рочастиц был установлен в 1905 году Энштейном для квантов света, в 1924 году Луи де Бройль распространил эти представления на все микрочастицы, в том числе и на электроны. Математическое выражение уравнения Луи де Бройль имеет вид :
υ = h / mv
Двойственная природа электрона приводит к тому, что его движение не может быть описано определенной траекторией, траектория размывается, возникает « полоса неопределенности» в которой находится электрон, чем точнее мы будем стараться определить его местонахождения, тем меньше узнаем о скорости его движения. Второй закон квантово-волновой теории формулируется следующим образом : Невозможно одновременно с любой заданной точностью определить координаты электрона и его скорость.
Одной из основных характеристик движущегося электрона является волновая функция Y (пси). Сама волновая функция физического смысла не имеет, а |Y| 2 показывает вероятность нахождения электрона в данной точке пространства. Более точным является выражение |Y| 2 dv -это веро-ятность нахождения электрона в элементарном объеме dv , она оценивается уравнением Шреденгера :
НY = ЕY ,
где Н – оператор Гамельтона, указывающий на последовательность операций с Y.
Данное уравнение имеет несколько решений, т.е. Y квантуется, однако волновая функция должна удовлетворять ряду условий : она должна быть однозначной, конечной, непрерывной и нормируемой.
В качестве модели состояния электрона в атоме в квантовой механике принято представление об электронном облаке. Пространство вокруг ядра, пребывание электрона в котором составляет 80 % называется атомной орби-талью. Волновая функция, являющаяся решением уравнения Шреденгера есть атомная орбиталь.
Волновая функция Y всегда содержит безразмерные параметры, кото-рые могут принимать ряд целочисленных значений. Эти величины называ-ются квантовыми числами.
n — главное квантовое число, характеризует запас энергии на энергетическом уровне и размеры атомной орбитали. Изменяется от 1 до 7, в электронных формулах обозначается арабскими цифрами;
l – орбитальное квантовое число, характеризует запас энергии на подуровне и форму атомной орбитали. Изменяется от 0 до (n – 1), принимает n значений, в электронных формулах обозначается латинскими буквами s- ( l = 0) , p- ( l =1 ), d- (l = 2 ) , f ( l = 3 ).
Электроны s-подуровня имеют орбиталь в виде полного шара, р-подуровня в виде объемной восьмерки, а d-подуровня имеют две формы орбиталей: веретена и розетки, у f-электронов орбитали имеют более сложную форму.
m – магнитное квантовое число, показывает число ориентаций атомных орбиталей в пространстве. Изменяется от –l до + l через 0, принимает
(2l + 1) значений. Так шарообразная s-орбиталь может иметь только одну ориентацию, а р — три ориентации , d –пять , f – семь.
Отсюда следует, что s — подуровень состоит из одной орбитали, р-подуровень – из трех орбиталей , d – из пяти орбиталей, f – подуровень из семи орбиталей.
s – спиновое квантовое число показывает направление вращения электрона вокруг своей оси, принимает два значения, равные + 1/ 2.
СТРОЕНИЕ ЭЛЕКТРОННЫХ ОБОЛОЧЕК АТОМОВ
Состояние электрона в многоэлектронных атомах всегда отвечает закону, сформулированному Паули : в атоме не может быть даже двух электронов, обладающих одинаковым набором всех четырех квантовых чисел. Это говорит о том, что на атомной орбитале может находится не более двух электронов.
Электронная оболочка имеет упорядоченное строение. Она состоит из электронных уровней (слоев), число которых равно номеру периода. В соответствии с принципом Паули максимальное число электронов на энергетическом уровне равно 2n2.
Каждый уровень, кроме первого, делится на подуровни. Число подуровней равно номеру уровня, максимальное число электронов на подуровне-2( 2l +1).
Чем выше расположен уровень, тем больше энергия его электронов.
Наименьшей энергией обладают электроны первого уровня а наибольшей -внешнего уровня. Наиболее устойчиво состояние атома, в котором электроны имеют наименьшую энергию.
Заполнение электронной оболочки происходит в соответствии с тремя правилами:
1. Заполнение электронной оболочки происходит в порядке возрастания энергии уровней (принцип наименьших энергий) .
2. Заполнение подуровней происходит в соответствии с правилом Клечковского :
— электроны заполняют тот подуровень для которого сумма значений главного и орбитального квантовых числе наименьшая;
— если сумма значений главного и орбитального квантовых чисел одинакова, то электроны заполняют тот подуровень для которого меньше значение главного квантового числа.
Отсюда следует следующий порядок заполнения уровней и подуровней : 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
3. Порядок заполнения атомных орбиталей происходит в соответствии с правилом Хунда : электроны заполняют атомные орбитали таким образом чтобы спин был максимальным.
Например:
+15 Р 1s2 2s2 2p63s2 3p3
+25 Mn 1s2 2s2 2p6 3s2 3p33d5 4s2
Приведённые формулы называются полными электронными формулами элемента. В зависимости от того электроны какого подуровня заполняются у данного элемента, они делятся на s-,p-,d- , f- элементы.
К s-элементам относятся элементы главных подгрупп первой и второй групп, р-элементы — это элементы главных подгрупп всех остальных групп. К d-элементам относятся элементы побочных подгрупп, а к f-элементам — лантаноиды и актиноиды.
Обычно используют сокращённые электронные формулы, содержащие только электроны валентного уровня, число которых равно номеру группы. ( для элементов главных подгрупп валентными являются электроны последнего энергетического уровня, для элементов побочных подгрупп последнего s и предпоследнего d).
Эти формулы используют для определения валентных возможностей атома. Их легко составить, зная период и группу атома. Например, бром-это элемент четвертого периода седьмой группы главной подгруппы, поэтому его сокращенная электронная формула: +35Вr…4s2 4p5 ; ванадий элемент четвертого периода пятой группы побочной подгрупп : +23V …3d3 4s2
2. Электронно-графические формулы
Эти схемы используют для определения валентных возможностей
атома. Уровни и подуровни должны располагаться в соответствии с их энергией: чем выше подуровень, тем выше его располагают. Орбитали изоб-ражают квадратиком или черточкой .
Например: Е 3d
17Cl…3s2 3p5
3p
3s
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
megalektsii.ru
