Строение атома кислорода (O), схема и примеры
Общие сведения о строении атома кислорода
Порядковый номер равен 8. Заряд ядра равен +8. Атомный вес – 15,999а.е.м. В природе встречаются три изотопа кислорода: 16O,17O и 18O, из которых наиболее распространенным является 16O (99,762 %).
Электронное строение атома кислорода
Атом кислорода имеет две оболочки, как и все элементы, расположенные во втором периоде. Номер группы –VI (халькогены) – свидетельствует о том, что на внешнем электронном уровне атома азота находится 6 валентных электронов. Обладает высокой окислительной способностью (выше только у фтора).
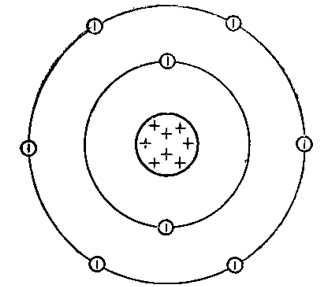
Рис. 1. Схематичное изображение строения атома кислорода.
Электронная конфигурация основного состояния записывается следующим образом:
1s22s22p4.
Кислород – элемент p-семейства. Энергетическая диаграмма для валентных электронов в невозбужденном состоянии выглядит следующим образом:
У кислорода есть 2 пары спаренных электронов и два неспаренных электрона. Во всех своих соединениях кислород проявляет валентность II.
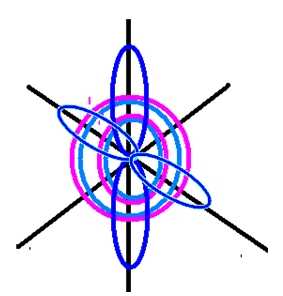
Рис. 2. Пространственное изображение строения атома кислорода.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Формула кислорода. Периодическая таблица Менделеева
Химический элемент кислород находится во втором периоде VI-ой главной группы устаревшего короткого варианта периодической таблицы. По новым стандартам нумерации — это 16-я группа. Соответствующее решение принято ИЮПАК в 1988 году. Формула кислорода как простого вещества — О2. Рассмотрим его основные свойства, роль в природе и хозяйстве. Начнем с характеристики всей группы периодической системы, которую возглавляет кислород. Элемент отличается от родственных ему халькогенов, а вода отличается от водородных соединений серы, селена и теллура. Объяснение всем отличительным чертам можно найти, только узнав о строении и свойствах атома.
Халькогены — родственные кислороду элементы
Сходные по свойствам атомы образуют одну группу в периодической системе. Кислород возглавляет семейство халькогенов, но отличается от них по ряду свойств.
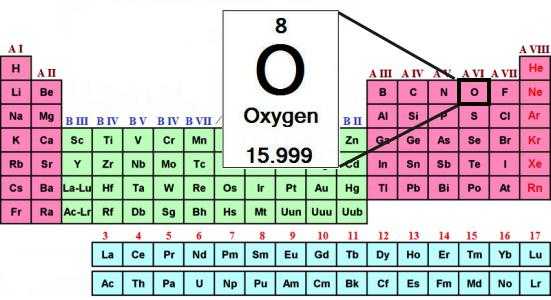
Атомная масса кислорода — родоначальника группы — составляет 16 а. е. м. Халькогены при образовании соединений с водородом и металлами проявляют свою обычную степень окисления: –2. Например, в составе воды (Н2О) окислительное число кислорода равно –2.
Состав типичных водородных соединений халькогенов отвечает общей формуле: Н2R. При растворении этих веществ образуются кислоты. Только водородное соединение кислорода — вода — обладает особыми свойствами. Согласно выводам ученых, это необычное вещество является и очень слабой кислотой, и очень слабым основанием.
Сера, селен и теллур имеют типичные положительные степени окисления (+4, +6) в соединениях с кислородом и другими неметаллами, обладающими высокой электроотрицательностью (ЭО). Состав оксидов халькогенов отражают общие формулы: RO2, RO3. Соответствующие им кислоты имеют состав: H2RO3, H2RO4.
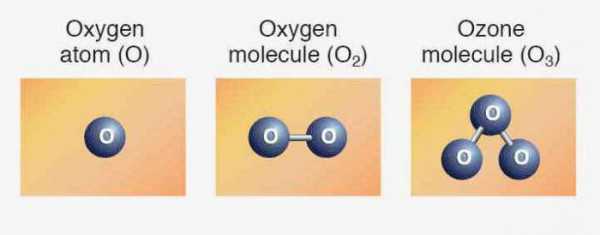
Элементам соответствуют простые вещества: кислород, сера, селен, теллур и полоний. Первые три представителя проявляют неметаллические свойства. Формула кислорода — О2. Аллотропное видоизменение того же элемента — озон (О3). Обе модификации являются газами. Сера и селен — твердые неметаллы. Теллур — металлоидное вещество, проводник электрического тока, полоний — металл.
Кислород — самый распространенный элемент
Общее содержание атомов элемента в земной коре составляет примерно 47 % (по весу). Кислород встречается как в свободном виде, так и в составе многочисленных соединений. Простое вещество, формула которого О2, находится в составе атмосферы, составляя 21 % воздуха (по объему). Молекулярный кислород растворен в воде, находится между частичками почвы.
Мы уже знаем, что есть другая разновидность существования того же самого химического элемента в форме простого вещества. Это озон — газ, образующий на высоте около 30 км от поверхности земли слой, часто называемый озоновым экраном. Связанный кислород входит в молекулы воды, в состав многих горных пород и минералов, органических соединений.
Строение атома кислорода
Периодическая таблица Менделеева содержит полную информацию о кислороде:
- Порядковый номер элемента — 8.
- Заряд ядра — +8.
- Общее число электронов — 8.
- Электронная формула кислорода — 1s22s22p4.
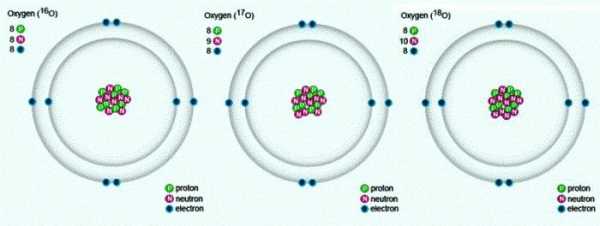
В природе встречаются три стабильных изотопа, которые имеют одинаковый порядковый номер в таблице Менделеева, идентичный состав протонов и электронов, но разное число нейтронов. Обозначаются изотопы одним и тем же символом — О. Для сравнения приведем схему, отражающую состав трех изотопов кислорода:
Свойства кислорода — химического элемента
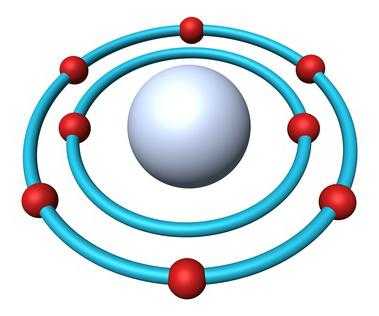
На 2р-подуровне атома имеются два неспаренных электрона, что объясняет появление степеней окисления –2 и +2. Два спаренных электрона не могут разъединиться, чтобы степень окисления возросла до +4, как у серы и других халькогенов. Причина — отсутствие свободного подуровня. Поэтому в соединениях химический элемент кислород не проявляет валентность и степень окисления, равные номеру группы в коротком варианте периодической системы (6). Обычное для него окислительное число равно –2.
Только в соединениях с фтором кислород проявляет нехарактерную для него положительную степень окисления +2. Значение ЭО двух сильных неметаллов отличается: ЭО (О) = 3,5; ЭО (F) = 4. Как более электроотрицательный химический элемент, фтор сильнее удерживает свои электроны и притягивает валентные частицы на внешнем энергетическом уровне атома кислорода. Поэтому в реакции с фтором кислород является восстановителем, отдает электроны.
Кислород — простое вещество
Английский исследователь Д. Пристли в 1774 году в ходе опытов выделил газ при разложении оксида ртути. Двумя годами ранее это же вещество в чистом виде получил К. Шееле. Лишь спустя несколько лет французский химик А. Лавуазье установил, что за газ входит в состав воздуха, изучил свойства. Химическая формула кислорода — О2. Отразим в записи состава вещества электроны, участвующие в образовании неполярной ковалентной связи — О::О. Заменим каждую связывающую электронную пару одной чертой: О=О. Такая формула кислорода наглядно показывает, что атомы в молекуле связаны между двумя общими парами электронов.

Выполним несложные расчеты и определим, чему равна относительная молекулярная масса кислорода: Mr(O2) = Ar(O) х 2 = 16 х 2 = 32. Для сравнения: Mr(возд.) = 29. Химическая формула кислорода отличается от формулы озона на один атом кислорода. Значит, Mr(O3) = Ar(O) х 3 = 48. Озон в 1,5 раза тяжелее кислорода.
Физические свойства
Кислород — это газ без цвета, вкуса и запаха (при обычной температуре и давлении, равном атмосферному). Вещество немного тяжелее воздуха; растворяется в воде, но в небольших количествах. Температура плавления кислорода является отрицательной величиной и составляет –218,3 °C. Точка, в которой жидкий кислород вновь превращается в газообразный, — это его температура кипения. Для молекул О2 значение этой физической величины достигает –182,96 °C. В жидком и твердом состоянии кислород приобретает светло-синюю окраску.
Получение кислорода в лаборатории
При нагревании кислородосодержащих веществ, например перманганата калия, выделяется бесцветный газ, который можно собрать в колбу или пробирку. Если внести в чистый кислород зажженную лучину, то она горит более ярко, чем в воздухе. Два других лабораторных способа получения кислорода — разложение пероксида водорода и хлората калия (бертолетовой соли). Рассмотрим схему прибора, который применяется для термического разложения.
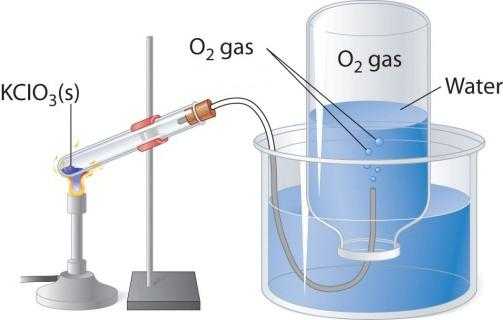
В пробирку или круглодонную колбу надо насыпать немного бертолетовой соли, закрыть пробкой с газоотводной трубочкой. Ее противоположный конец следует направить (под водой) в опрокинутую вверх дном колбу. Горлышко должно быть опущено в широкий стакан или кристаллизатор, наполненный водой. При нагревании пробирки с бертолетовой солью выделяется кислород. По газоотводной трубке он поступает в колбу, вытесняя из нее воду. Когда колба наполнится газом, ее закрывают под водой пробкой и переворачивают. Полученный в этом лабораторном опыте кислород можно использовать для изучения химических свойств простого вещества.
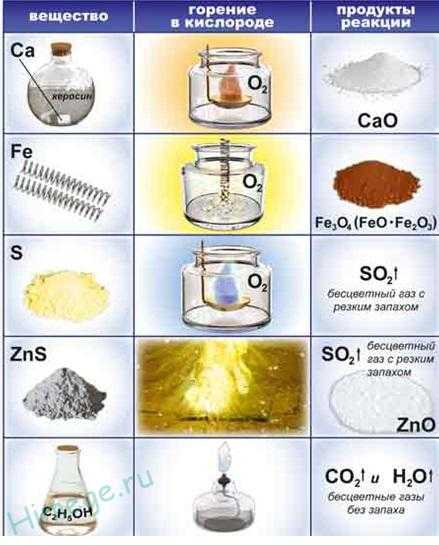
Горение
Если в лаборатории проводится сжигание веществ в кислороде, то нужно знать и соблюдать противопожарные правила. Водород мгновенно сгорает в воздухе, а смешанный с кислородом в соотношении 2:1, он взрывоопасен. Горение веществ в чистом кислороде происходит намного интенсивнее, чем в воздухе. Объясняется это явление составом воздуха. Кислород в атмосфере составляет чуть больше 1/5 части (21%). Горение — это реакция веществ с кислородом, в результате которой образуются разные продукты, в основном оксиды металлов и неметаллов. Пожароопасны смеси О2 с горючими веществами, кроме того, получившиеся соединения могут быть токсичными.
Горение обычной свечки (или спички) сопровождается образованием диоксида углерода. Следующий опыт можно провести в домашних условиях. Если сжигать вещество под стеклянной банкой или большим стаканом, то горение прекратится, как только израсходуется весь кислород. Азот не поддерживает дыхание и горение. Углекислый газ — продукт окисления — больше не вступает в реакцию с кислородом. Прозрачная известковая вода позволяет обнаружить присутствие диоксида углерода после горения свечи. Если пропускать продукты горения через гидроксид кальция, то раствор мутнеет. Происходит химическая реакция между известковой водой и углекислым газом, получается нерастворимый карбонат кальция.

Получение кислорода в промышленных масштабах
Самый дешевый процесс, в результате которого получаются свободные от воздуха молекулы О2, не связан с проведением химических реакций. В промышленности, скажем, на металлургических комбинатах, воздух при низкой температуре и высоком давлении сжижают. Такие важнейшие компоненты атмосферы, как азот и кислород, кипят при разных температурах. Разделяют воздушную смесь при постепенном нагревании до обычной температуры. Сначала выделяются молекулы азота, затем кислорода. Способ разделения основан на разных физических свойствах простых веществ. Формула простого вещества кислорода такая же, как была до охлаждения и сжижения воздуха, — О2.
В результате некоторых реакций электролиза тоже выделяется кислород, его собирают над соответствующим электродом. Газ нужен промышленным, строительным предприятиям в больших объемах. Потребности в кислороде постоянно растут, особенно нуждается в нем химическая промышленность. Хранят полученный газ для производственных и медицинских целей в стальных баллонах, снабженных маркировкой. Емкости с кислородом окрашивают в синий или голубой цвет, чтобы отличать от других сжиженных газов — азота, метана, аммиака.

Химические расчеты по формуле и уравнениям реакций с участием молекул О2
Численное значение молярной массы кислорода совпадает с другой величиной — относительной молекулярной массой. Только в первом случае присутствуют единицы измерения. Коротко формула вещества кислорода и его молярной массы должна быть записана так: М(О2) = 32 г/моль. При нормальных условиях молю любого газа соответствует объем 22,4 л. Значит, 1 моль О2 — это 22,4 л вещества, 2 моль О2 — 44,8 л. По уравнению реакции между кислородом и водородом можно заметить, что взаимодействуют 2 моля водорода и 1 моль кислорода:
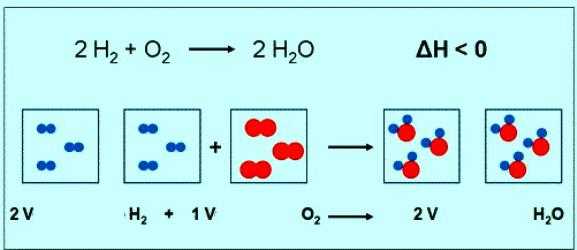
Если в реакции участвует 1 моль водорода, то объем кислорода составит 0,5 моль • 22,4 л/моль = 11,2 л.
Роль молекул О2 в природе и жизни человека
Кислород потребляется живыми организмами на Земле и участвует в круговороте веществ свыше 3 млрд лет. Это главное вещество для дыхания и метаболизма, с его помощью происходит разложение молекул питательных веществ, синтезируется необходимая для организмов энергия. Кислород постоянно расходуется на Земле, но его запасы пополняются благодаря фотосинтезу. Русский ученый К. Тимирязев считал, что благодаря именно этому процессу до сих пор существует жизнь на нашей планете.

Велика роль кислорода в природе и хозяйстве:
- поглощается в процессе дыхания живыми организмами;
- участвует в реакциях фотосинтеза в растениях;
- входит в состав органических молекул;
- процессы гниения, брожения, ржавления протекают при участии кислорода, выступающего в качестве окислителя;
- используется для получения ценных продуктов органического синтеза.
Сжиженный кислород в баллонах используют для резки и сварки металлов при высоких температурах. Эти процессы проводят на машиностроительных заводах, на транспортных и строительных предприятиях. Для проведения работ под водой, под землей, на большой высоте в безвоздушном пространстве люди тоже нуждаются в молекулах О2. Кислородные подушки применяются в медицине для обогащения состава воздуха, вдыхаемого больными людьми. Газ для медицинских целей отличается от технического практически полным отсутствием посторонних примесей, запаха.

Кислород — идеальный окислитель
Известны соединения кислорода со всеми химическими элементами таблицы Менделеева, кроме первых представителей семейства благородных газов. Многие вещества непосредственно вступают в реакции с атомами О, исключая галогены, золото и платину. Большое значение имеют явления с участием кислорода, которые сопровождаются выделением света и тепла. Такие процессы широко используются в быту, промышленности. В металлургии взаимодействие руд с кислородом называют обжигом. Предварительно измельченную руду смешивают с воздухом, обогащенным кислородом. При высоких температурах происходит восстановление металлов из сульфидов до простых веществ. Так получают железо и некоторые цветные металлы. Присутствие чистого кислорода повышает скорость технологических процессов в разных отраслях химии, технике и металлургии.
Появление дешевого способа получения кислорода из воздуха методом разделения на компоненты при низкой температуре стимулировало развитие многих направлений промышленного производства. Химики считают молекулы О2 и атомы О идеальными окислительными агентами. Это естественные материалы, они постоянно возобновляются в природе, не загрязняют окружающую среду. Кроме того, химические реакции с участием кислорода чаще всего завершаются синтезом еще одного натурального и безопасного продукта — воды. Велика роль О2 в обезвреживании токсичных производственных отходов, очистке воды от загрязнений. Кроме кислорода, для обеззараживания используется его аллотропная модификация — озон. Это простое вещество обладает высокой окислительной активностью. При озонировании воды разлагаются загрязняющие вещества. Озон также губительно действует на болезнетворную микрофлору.
fb.ru
Кислород – характеристика элемента, распространённость в природе, физические и химические свойства, получение » HimEge.ru
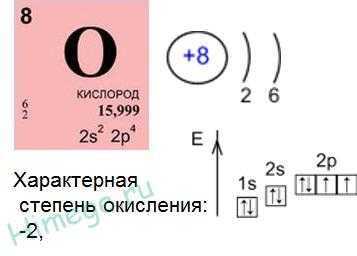 Кислород О имеет атомный номер 8, расположен в главной подгруппе (подгруппе а) VI группе, во втором периоде. В атомах кислорода валентные электроны размещаются на 2-м энергетическом уровне, имеющем только s— и p-орбитали. Это исключает возможность перехода атомов О в возбуждённое состояние, поэтому кислород во всех соединениях проявляет постоянную валентность, равную II. Имея высокую электроотрицательность, атомы кислорода всегда в соединениях заряжены отрицательно (с.о. = -2 или -1). Исключение – фториды OF2 и O2F2.
Кислород О имеет атомный номер 8, расположен в главной подгруппе (подгруппе а) VI группе, во втором периоде. В атомах кислорода валентные электроны размещаются на 2-м энергетическом уровне, имеющем только s— и p-орбитали. Это исключает возможность перехода атомов О в возбуждённое состояние, поэтому кислород во всех соединениях проявляет постоянную валентность, равную II. Имея высокую электроотрицательность, атомы кислорода всегда в соединениях заряжены отрицательно (с.о. = -2 или -1). Исключение – фториды OF2 и O2F2.
Для кислорода известны степени окисления -2, -1, +1, +2
Общая характеристика элемента
Кислород – самый распространенный элемент на Земле, на его долю приходится чуть меньше половины, 49 % от общей массы земной коры. Природный кислород состоит из 3 стабильных изотопов 16О, 17О и 18О (преобладает 16О). Кислород входит в состав атмосферы (20,9 % по объему, 23,2 по массе), в состав воды и более 1400 минералов: кремнезема, силикатов и алюмосиликатов, мраморов, базальтов, гематита и других минералов и горных пород. Кислород составляет 50-85% массы тканей растений и животных, т.к содержится в белках, жирах и углеводах, из которых состоят живые организмы. Общеизвестна роль кислорода для дыхания, для процессов окисления.
Кислород сравнительно мало растворим в воде – 5 объемов в 100 объемах воды. Однако, если бы весь растворенный в воде кислород перешел в атмосферу, то он занял бы огромный объем – 10 млн км3 ( н.у). Это равно примерно 1% всего кислорода в атмосфере. Образование на земле кислородной атмосферы обусловлено процессами фотосинтеза.
Открыт шведом К. Шееле ( 1771 – 1772 г.г) и англичанином Дж. Пристли ( 1774г.). Первый использовал нагревание селитры, второй – оксида ртути (+2). Название дал А.Лавуазье («оксигениум» — «рождающий кислоты»).
В свободном виде существует в двух аллотропных модификациях – «обыкновенного» кислорода О2 и озона О3
.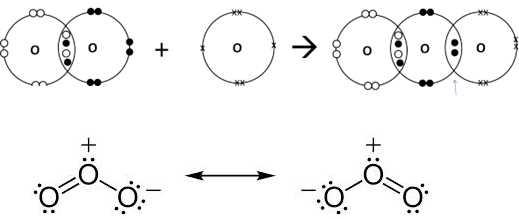
Строение молекулы озона
3О2 = 2О3 – 285 кДж
Озон в стратосфере образует тонкий слой, который поглощает большую часть биологически вредного ультрафиолетового излучения.
При хранении озон самопроизвольно превращается в кислород. Химически кислород О2 менее активен, чем озон. Электроотрицательность кислорода 3,5.
Физические свойства кислорода
O2 – газ без цвета, запаха и вкуса, т.пл. –218,7 °С, т.кип. –182,96 °С, парамагнитен.
Жидкий O2 голубого, твердый – синего цвета. O2 растворим в воде (лучше, чем азот и водород).
Получение кислорода
1. Промышленный способ — перегонка жидкого воздуха и электролиз воды:
2Н2О → 2Н2 + О2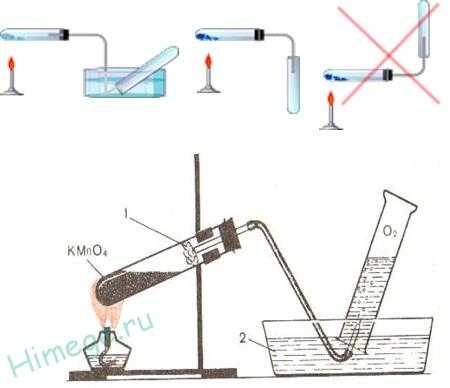
2. В лаборатории кислород получают:
1.Электролизом щелочных водных растворов или водных растворов кислородосодержащих солей (Na
2. Термическим разложением перманганата калия KMnO4:
2KMnO4 = K2MnO4 + MnO2 + O2↑,
Бертолетовой соли KClO3:
2KClO3 = 2KCl + 3O2↑ (катализатор MnO2)
Оксида марганца (+4) MnO2:
4MnO2 = 2Mn2O3 + O2↑ (700 oC),
3MnO2 = 2Mn3O4 + O2↑ (1000 oC),
Пероксид бария BaO2 :
2BaO2 = 2BaO + O2↑
3. Разложением пероксида водорода:
2H2O2 = H2O + O2↑ (катализатор MnO2)
4. Разложение нитратов:
2KNO3 → 2KNO2 + O2
На космических кораблях и подводных лодках кислород получают из смеси K2O 2 и K2O4:
2K2O4 + 2H2O = 4KOH +3O2↑
4KOH + 2CO2 = 2K2CO3 + 2H2O
Суммарно:
2K2O4 + 2CO2 = 2K2CO3 + 3О2 ↑
Когда используют K2O2, то суммарная реакция выглядит так:
2K2O2 + 2CO2 = 2K2CO3 + O2 ↑
Если смешать K2O2 и K2O4 в равномолярных (т.е. эквимолярных) количествах, то на 1 моль поглощенного СО2 выделится один моль О2.
Химические свойства кислорода
Кислород поддерживает горение. Горение — быстрый процесс окисления вещества, сопровождающийся выделением большого количества теплоты и света. Чтобы доказать, что в склянке находится кислород, а не какой-то другой газ, надо в склянку опустить тлеющую лучинку. В кислороде тлеющая лучинка ярко вспыхивает. Горение различных веществ на воздухе – это окислительно-восстановительный процесс, в котором окислителем является кислород. Окислители – это вещества, «отбирающие» электроны у веществ-восстановителей. Хорошие окислительные свойства кислорода можно легко объяснить строением его внешней электронной оболочки.
Валентная оболочка кислорода расположена на 2-м уровне – относительно близко к ядру. Поэтому ядро сильно притягивает к себе электроны. На валентной оболочке кислорода 2s2 2p4 находится 6 электронов. Следовательно, до октета недостает двух электронов, которые кислород стремится принять с электронных оболочек других элементов, вступая с ними в реакции в качестве окислителя.
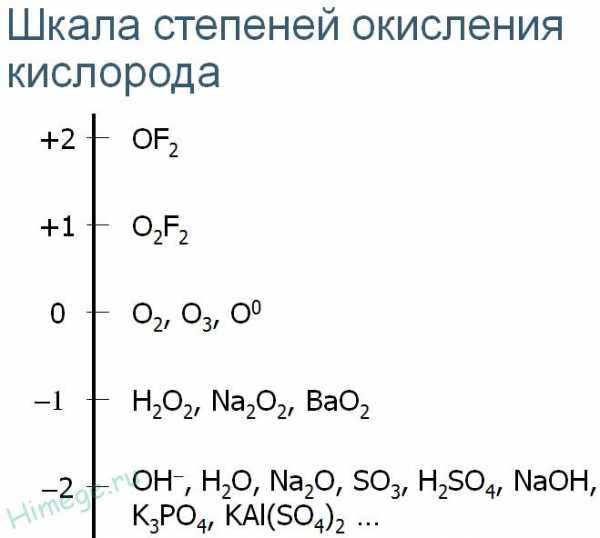 Кислород имеет вторую (после фтора) электроотрицательность в шкале Полинга. Поэтому в подавляющем большинстве своих соединений с другими элементами кислород имеет отрицательную степень окисления. Более сильным окислителем, чем кислород, является только его сосед по периоду – фтор. Поэтому соединения кислорода с фтором – единственные, где кислород имеет положительную степень окисления.
Кислород имеет вторую (после фтора) электроотрицательность в шкале Полинга. Поэтому в подавляющем большинстве своих соединений с другими элементами кислород имеет отрицательную степень окисления. Более сильным окислителем, чем кислород, является только его сосед по периоду – фтор. Поэтому соединения кислорода с фтором – единственные, где кислород имеет положительную степень окисления.
Итак, кислород – второй по силе окислитель среди всех элементов Периодической системы. С этим связано большинство его важнейших химических свойств.
С кислородом реагируют все элементы, кроме Au, Pt, He, Ne и Ar, во всех реакциях (кроме взаимодействия со фтором) кислород — окислитель.
 Кислород легко реагирует с щелочными и щелочноземельными металлами:
Кислород легко реагирует с щелочными и щелочноземельными металлами:
4Li + O2 → 2Li2O,
2K + O2 → K2O2,
2Ca + O2 → 2CaO,
2Na + O2 → Na2O2,
2K + 2O2 → K2O4
Мелкий порошок железа ( так называемого пирофорного железа) самовоспламеняется на воздухе, образуя Fe
3 Fe + 2O2 → Fe3O4
2Mg + O2 → 2MgO
2Cu + O2 → 2CuO
С неметаллами (серой, графитом, водородом, фосфором и др.) кислород реагирует при нагревании:
S + O2 → SO2,
C + O2 → CO2,
2H2 + O2 → H2O,
4P + 5O2 → 2P2O5,
Si + O2 → SiO2, и т.д
Почти все реакции с участием кислорода O2 экзотермичны, за редким исключением, например:
N2 + O2 → 2NO – Q
Эта реакция протекает при температуре выше 1200 oC или в электрическом разряде.
Кислород способен окислить сложные вещества, например:
2H2S + 3O2 → 2SO2 + 2H2O (избыток кислорода),
2H2S + O2 → 2S + 2H2O (недостаток кислорода),
4NH3 + 3O2 → 2N2 + 6H2O (без катализатора),
4NH3 + 5O2 → 4NO + 6H2O (в присутствии катализатора Pt ),
CH4 (метан) + 2O2 → CO2 + 2H2O,
4FeS2 (пирит) + 11O2 → 2Fe2O3 + 8SO2.
Известны соединения, содержащие катион диоксигенила O2+, например, O2+ [PtF6]— (успешный синтез этого соединения побудил Н. Бартлетта попытаться получить соединения инертных газов).

Озон химически более активен, чем кислород O2. Так, озон окисляет иодид — ионы I— в растворе Kl:
O3 + 2Kl + H2
Озон сильно ядовит, его ядовитые свойства сильнее, чем, например, у сероводорода. Однако в природе озон, содержащийся в высоких слоях атмосферы, выполняет роль защитника всего живого на Земле от губительного ультрафиолетового излучения солнца. Тонкий озоновый слой поглощает это излучение, и оно не достигает поверхности Земли. Наблюдаются значительные колебания в толщине и протяженности этого слоя с течением времени (так называемые озоновые дыры) причины таких колебаний пока не выяснены.
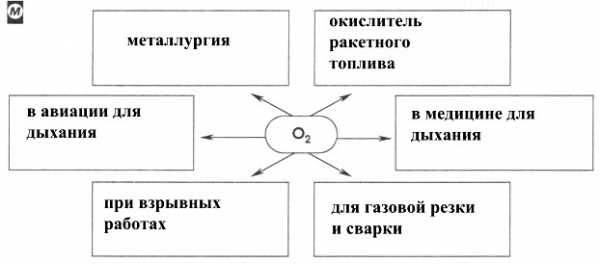
Применение кислорода O2: для интенсификации процессов получения чугуна и стали, при выплавке цветных металлов, как окислитель в различных химических производствах, для жизнеобеспечения на подводных кораблях, как окислитель ракетного топлива (жидкий кислород), в медицине, при сварке и резке металлов.
Применение озона О3: для обеззараживания питьевой воды, сточных вод, воздуха, для отбеливания тканей.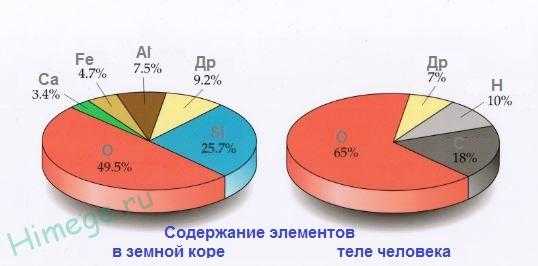
Биологическая роль р-элементов VIA группы. Применение их соединений в медицине
himege.ru
Тема 24. Кислород. | 9 класс
Часть I
1. Строение атома
2. Молекулярная формула – О2, другая аллотропная модификация имеет формулу О3 и носит название – озон.
3. Физические свойства кислорода: газ без цвета и запаха, тяжелее воздуха.
4. Химические свойства кислорода.
Взаимодействует (закончите уравнения реакций и рассмотрите их с позиций окисления-восстановления):

5. Получение кислорода:
1) в промышленности – из жидкого воздуха
2) в лаборатории – разложением (закончите уравнения реакций, назовите соединения и процессы, укажите условия их протекания):

3) в природе (запишите уравнение и название процесса):
Часть II
1. Заполните схему «Применение кислорода».
2. С помощью Интернета подготовьте небольшое сообщение по теме «Интенсификация металлургических и других промышленных процессов с помощью кислорода». Запишите план или тезисы сообщения в особой тетради.
Кислород в металлургии широко применяется для интенсификации ряда металлургических процессов. Полная или частичная замена поступающего в металлургические агрегаты воздуха кислородом изменила химизм процессов, их технические параметры. Кислородное дутье позволило сократить потери тепла с уходящими газами, значительная часть которых при воздушном дутье составлял азот, который замедлял течение реакций. При продувке кислородом снижается расход топлива, улучшается качество металла, в металлургических агрегатах возможно получение новых видов продукции (например, шлаков и газов необычного для данного процесса состава, находящих специальное техническое применение) и др.
Большие перспективы имеет интенсификация металлургических процессов путем введения в металлургические агрегаты (доменная печь, конвертор, мартеновская печь) воздуха, обогащенного кислородом. Применение кислородного дутья повышает температуру процесса, уменьшает содержание вредных газов в стали, повышая тем самым ее механические качества. Уменьшение общего количества газов при кислородном дутье уменьшает и потерю теплоты, уносимой газами. Кислородное дутье сокращает время продувки, повышая производительность конвертора.
3. Запишите схемы реакций, протекание которых возможно. Рассмотрите уравнения реакций с позиций окисления-восстановления.

4. В лаборатории собирают кислород в сосуд с помощью вытеснения воды или воздуха. Распознают с помощью тлеющей лучинки, которая загорается (вспыхивает).
5. Сравните свойства и области применения кислорода и озона.

6. Дополните цепочку переходов. Составьте уравнения реакций, с помощью которых можно осуществить превращения по схеме:
7. Придумайте и запишите условия задачи на нахождение объёма воздуха, необходимого для сжигания известного объёма этана (С2Н2). Решите задачу, используя правило Гей-Люссака.
Найти объём воздуха, необходимого на сжигание 44,8 л С2Н2 (н.у.)?

superhimik.ru
— строение кислорода — Биохимия
Возникновение аэробного метаболизма у древних организмов принесло им не только выгоды в виде более эффективного метаболизма, но и проблемы, связанные с особенностями строения молекулы кислорода.
Порядковый номер кислорода в таблице Менделеева – 8, заряд ядра – +8, общее число электронов – 8, электронная формула кислорода – 1s22s22p4. На 2р-подуровне атома имеются два неспаренных электрона, обычное для кислорода окислительное число равно -2.
Диаграмма строениz атома кислорода |
Строение молекулы кислорода |
Молекула кислорода в своем обычном состоянии отличается от других газообразных элементов тем, что имеет два неспаренных электрона, т.е. является бирадикалом. В целом, общие механизмы восстановления кислорода в биохимических реакциях происходят с участием только одного электрона, а кислород является довольно стабильной молекулой, обладающей свойством сильного окислителя.
Упомянутые неспаренные электроны обладают параллельными спинами. Это, в соответствии с принципом Паули, выдвигает условие, что с кислородом могут взаимодействовать только такие двухвалентные восстановители, которые имеют два неспаренных электрона с параллельными спинами, но спины приносимых электронов должны быть противоположны имеющимся в кислороде.
Поскольку каждая молекула кислорода имеет два неспаренных электрона на внешней орбитали, то в клетке она легко вовлекается в реакции, связанные с захватом «недополученных» электронов, и в итоге восстанавливается до воды, конечного продукта биологического окисления. В идеальном мире именно так и происходит. Однако в реальности часто образуются продукты неполного восстановления кислорода, называемые активные формы кислорода (АФК). АФК являются нестабильными молекулами, что и определяет их высокие реакционные свойства.

Активные формы кислорода
Любые свободные радикалы — это высоко реактивные молекулы с неспаренными электронами, находящимися на внешней оболочке атома или молекулы, обладающие очень высокой реакционной способностью. Они стремятся получить дополнительные электроны так, чтобы появилась стабильная пара. Накопление свободных радикалов в клетке, как правило, является результатом превращения кислорода в АФК, которые могут реагировать с другими клеточными молекулами и вызывать их радикализацию.
Кроме активных радикалов кислорода существуют и другие реактивные молекулы.
Активные формы азота и хлора
Вы можете спросить или оставить свое мнение.
biokhimija.ru
Кислород и его характеристики
Общая характеристика кислорода
Кислород – самый распространенный элемент земной коры. В свободном состоянии он находится в атмосферном воздухе, в связанном виде входит в состав воды, минералов, горных пород и всех веществ, из которых построены организмы растений и животных. Массовая доля кислорода в земной коре составляет около 47%.
В виде простого вещества кислород представляет собой бесцветный газ, не имеющий запаха. Он немного тяжелее воздуха: масса 1 л кислорода при нормальных условиях равна 1,43 г, а 1 л воздуха 1,293г. Кислород растворяется в воде, хотя и в небольших количествах: 100 объемов воды при 0oС растворяют 4,9, а при 20oС – 3,1 объема кислорода.
Атомная и молекулярная масса кислорода
Относительная атомная масса атомарного кислорода равна 15,999 а.е.м.
Это безразмерная величина.Известно, что молекула кислорода двухатомна – О2. Относительная молекулярная масса молекулы кислорода будет равна:
Mr(О2) = 15,999 × 2 ≈32.
Аллотропия и аллотропные модификации кислорода
Кислород может существовать в виде двух аллотропных модификаций – кислорода О2 и озона О3 (физические свойства кислорода описаны выше).
При обычных условиях озон – газ. От кислорода его можно отделить сильным охлаждением; озон конденсируется в синюю жидкость, кипящую при (-111,9oС).
Растворимость озона в воде значительно больше, чем кислорода: 100 объемов воды при 0oС растворяют 49 объемов озона.
Образование озона из кислорода можно выразить уравнением:
3O2 = 2O3 – 285 кДж.
Изотопы кислорода
Известно, что в природе кислород может находиться в виде трех изотопов 16O (99,76%), 17O (0,04%) и 18O (0,2%). Их массовые числа равны 16, 17 и 18 соответственно. Ядро атома изотопа кислорода 16O содержит восемь протонов и восемь нейтронов, а изотопов 17O и 18O– такое же количество протонов,девять и десять нейтронов соответственно.
Существует двенадцать радиоактивных изотопов кислорода с массовыми числами от 12-ти до 24-х, из которых наиболее стабильным является изотоп 15О с периодом полураспада равным 120 с.
Ионы кислорода
На внешнем энергетическом уровне атома кислорода имеется шесть электронов, которые являются валентными:
1s22s22p4.
Схема строения атома кислорода представлена ниже:
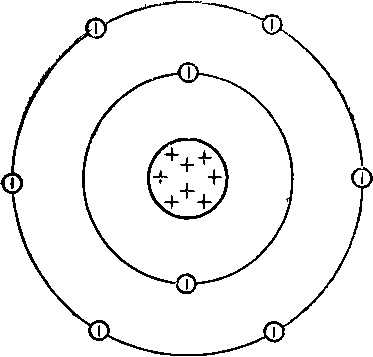
В результате химического взаимодействия кислород может терять свои валентные электроны, т.е. являться их донором, и превращаться в положительно заряженные ионы или принимать электроны другого атома, т.е. являться их акцептором, и превращаться в отрицательно заряженные ионы:
О0+2e → О2-;
О0-1e → О1+.
Молекула и атом кислорода
Молекула кислорода состоит из двух атомов – О2. Приведем некоторые свойства, характеризующие атом и молекулу кислорода:
|
Энергия ионизации атома, эВ |
13,41 |
|
Относительная электроотрицательность |
3,44 |
|
Радиус атома, нм |
0,060 |
|
Стандартная энтальпия диссоциации молекул при 25oС, кДж/моль |
498 |
Примеры решения задач
ru.solverbook.com
Кислород в природе (49,4% в Земной коре)
На Земле находится 49,4% кислорода, который встречается либо в свободном виде в воздухе, либо в связанном (вода, соединения и минералы).
Характеристика кислорода
На нашей планете газ кислород распространен больше всех других химических элементов. И это неудивительно, ведь он входит в состав:
- горных пород,
- воды,
- атмосферы,
- живых организмов,
- белков, углеводов и жиров.
Кислород активный газ и поддерживает горение.
Физические свойства
В атмосфере кислород содержится в бесцветном газообразном виде. Он не имеет запаха, малорастворим в воде и других растворителях. У кислорода прочные молекулярные связи, из-за которых он химически малоактивен.
Если кислород нагревать, он начинает окислять и реагировать с большинством неметаллов и металлов. Например, железо, этот газ медленно окисляет и вызывает его ржавление.
При снижении температуры (-182,9°С), и нормальном давлении газообразный кислород переходит в другое состояние (жидкое) и приобретает бледно-синий цвет. Если температуру еще снижать (до -218,7°С) газ затвердеет и изменится до состояния синих кристаллов.
В жидком и твердом состояниях кислород приобретает синий цвет и обладает магнитными свойствами.
Древесный уголь является активным поглотителем кислорода.
Химические свойства

Почти во время всех реакций кислорода с другими веществами образуется и выделяется энергия, сила которой может зависеть от температуры. Например, при обычных температурах этот газ медленно реагирует с водородом, а при температуре выше 550°С возникает реакция со взрывом.
Кислород – активный газ, который входит в реакцию с большинством металлов, кроме платиновых и золота. Сила и динамика взаимодействия, во время которого образуются оксиды, зависит от присутствия в металле примесей, состояния его поверхности и измельчения. Некоторые металлы, во время связи с кислородом, кроме основных оксидов образуют амфотерные и кислотные оксиды. Оксиды золота и платиновых металлов возникают во время их разложения.
Кислород кроме металлов, так же активно взаимодействует практически со всеми химическими элементами (кроме галогенов).
В молекулярном состоянии кислород более активен и эту особенность используют при отбеливании различных материалов.
Роль и значение кислорода в природе

Зеленые растения вырабатывают больше всего кислорода на Земле, причем основная масса производится водными растениями. Если кислорода в воде выработалась больше, то избыток уйдет в воздух. А если меньше, то наоборот, недостающее количество будет дополнено из воздуха.
Морская и пресная вода содержит 88,8 % кислорода (по массе), а в атмосфере его 20,95 % по объёму. В земной коре больше 1500 соединений имеют в составе кислород.
Из всех газов, входящих в состав атмосферы, больше всего важен для природы и человека кислород. Он есть в каждой живой клетке и необходим всем живым организмам для дыхания. Недостаток кислорода в воздухе сразу отражается на жизнедеятельности. Без кислорода невозможно дышать, а значит жить. Человек во время дыхания за 1 мин. в среднем его потребляет 0,5 дм3. Если в воздухе его станет меньше до 1/3 его части, то он потеряет сознание, до 1/4 части — он умрет.
Дрожжи и некоторые бактерии могут жить без кислорода, но теплокровные животные, умирают при его недостатке через несколько минут.
Круговорот кислорода в природе
Круговоротом кислорода в природе называется обмен им между атмосферой и океанами, между животными и растениями во время дыхания, а так же в процессе химического горения.
На нашей планете важный источник кислорода — растения, в которых проходит уникальный процесс фотосинтеза. Во время него происходит выделение кислорода.
В верхней части атмосферы тоже образуется кислород, вследствие разделения воды под действием Солнца.
Как происходит круговорот кислорода в природе?
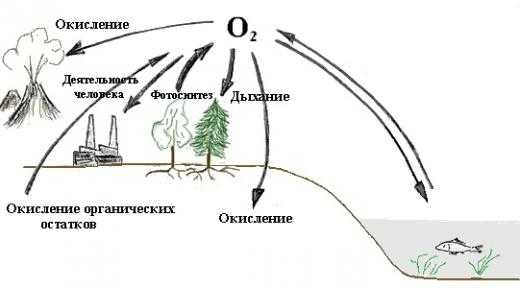
Во время дыхания животных, людей и растений, а так же горения любого топлива тратится кислород и образуется углекислый газ. Потом углекислым газом питаются растения, которые в процессе фотосинтеза снова вырабатывают кислород.
Таким образом, его содержание в воздухе атмосферы поддерживается и не заканчивается.
Области применения кислорода
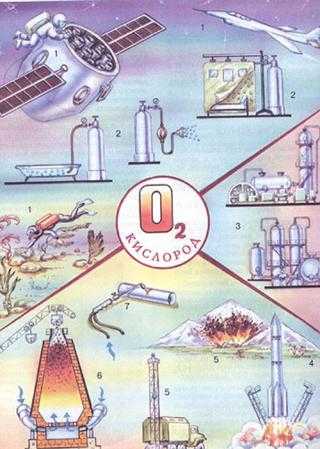
В медицине во время операций и опасных для жизни заболеваний больным дают дышать чистым кислородом, чтобы облегчить их состояние и ускорить выздоровление.
Без баллонов с кислородом альпинисты не поднимаются в горы, а аквалангисты не погружаются на глубину морей и океанов.
Кислород широко применяется в разных видах промышленности и производства:
- для обрезки и сварки различных металлов
- для получения очень высоких температур на заводах
- для получения разнообразных химических соединений • для ускорения плавления металлов.
Так же широко кислород применяется в космической индустрии и авиации.
xn—-8sbiecm6bhdx8i.xn--p1ai
