Конспект урока на тему «Белки» (10 класс)
10 класс. Биология (ПРОФ)
Тема урока: «Биологические полимеры – белки». (2 часа)
Тип урока: комбинированный
Цель урока: сформировать понятие о белках, как о органических полимерах, раскрыть состав, структуру, свойства и функции белков; развивать умение работать с учебником, анализировать. Сравнивать, делать выводы; воспитывать культуру труда.
Оборудование: мм презентация
Ход урока
организационный момент
Актуализация знаний
Что относят к неорганическим и органическим веществам клетки?
Каково строение и свойства воды и минеральных солей?
Каковы функции воды и минеральных солей?
Приложение 1
Изучение нового материала
БЕЛКИ — основная составная часть любой живой клетки. На их долю приходится половина сухого вещества клетки (после удаления из нее волы).
Состав белков.
В состав белков кроме С H O N могут входить S P Fe. Белки- полимеры, мономерами которых являются аминокислоты. В образовании огромного многообразия белков участвуют всего 20 аминокислот. Все аминокислоты содержат карбоксильную группу –COOH- с кислотными свойствамии аминную группу –NH2 с основными свойствами, что обеспечивает их высокую реактивность. Отличаются аминокислоты только углеводородным радикалом. Соединяясь молекулы аминокислоты образуют пептидные связи между углеродом кислотной и азотом основной групп.
Структуры белков.
Молекулы белков имеют различные пространственные конфигурации, ив их строении различаютчетыре уровня структурной организации:
первичная структура белка – последовательность аминокислот в составе полипептидной цепи;
вторичная структура имеет вид спирали в результате образования водородных связей между –СО и -NH- разных аминокислотных остатков полипептидной цепи;
третичная структура— трехмерная пространственная упаковка полипептидной цепи. В результате образуется глобула;
четвертичная структура возникает в результате соединения нескольких макромолекул с третичной стуктурой.
Свойства белков.
При изменении температуры, облучении рентгеновскими лучами, обезвоживании, резком изменении рН среды белковая молекула разрушается. Этот процесс называется денатурацией. Процесс денатурации обратим, если не разрушена первичная структура белка. Процесс восстановления естественной структуры белка называется
ФУНКЦИИ БЕЛКОВ
Какие функции белков вы проходили на уроках биологии?
Функции белков в клетке чрезвычайно многообразны.
Одна из важнейших — строительная (структурная) функция: белки участвуют в образовании всех клеточных мембран и органоидов клетки, а также внеклеточных структур. Белки, выполняющие структурные функции, занимают по количеству первое место среди других белков тела человека. Среди них важнейшую роль играет коллаген в соединительной ткани, кератин в волосах, ногтях, коже, эластин в сосудистой стенке и др. Большое значение имеют комплексы белков с углеводами в формировании ряда секретов — мукоидов, муцина и т. д. В комплексе с липидами (в частности фосфолипидами) белки участвуют в образовании биомембран клеток.
Исключительно важное значение имеет каталитическая (ферментативная) роль белков. Всеферменты — вещества белковой природы, они ускоряют химические реакции, протекающие в клетке, в десятки и сотни тысяч раз. Многочисленные биохимические реакции в живых организмах протекают в мягких условиях, при температурах, близких к 40°С, и значениях рН, близких к нейтральным. В этих условиях скорость протекания большинства реакций ничтожно мала, поэтому для их приемлемого осуществления необходимы специальные биологические катализаторы — ферменты. Как правило, ферменты — это либо белки, либо комплексы белков с каким-либо кофактором — ионом металла или специальной органической молекулой. Многие белки ускоряют химические реакции в сотни раз.
Двигательная функция живых организмов обеспечивается специальными сократительными белками. Эти белки участвуют во всех видах движения, к которым способны клетки и организмы: образование псевдоподий, мерцание ресничек и биение жгутиков у простейших, сокращение мышц у многоклеточных животных, движение листьев у растений и др.
В акте мышечного сокращения и расслабления участвует множество белковых веществ. Однако главную роль в этих жизненно важных процессах играют актин и миозин — специфические белки мышечной ткани. Сократительная функция присуща не только мышечным белкам, но и белкам цитоскелета, что обеспечивает тончайшие процессы жизнедеятельности клеток (расхождение хромосом в процессе митоза).
Транспортная функция белков заключается в присоединении химических элементов (например, кислорода) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела.
Дыхательная функция крови, в частности перенос кислорода, осуществляется молекулами гемоглобина — белка эритроцитов. В транспорте липидов принимают участие альбумины
сыворотки крови. Ряд других сывороточных белков образует комплексы с жирами, медью, железом, тироксином, витамином А и другими соединениями, обеспечивая их доставку в соответствующие органы-мишени.Защитная функция. При поступлении в организм чужеродных белков или микроорганизмов в белых кровяных тельцах — лейкоцитах — образуются особые белки — антитела. Они связывают и обезвреживают несвойственные организму вещества (антигены).
Высокая специфичность взаимодействия антител с антигенами (чужеродными веществами) по типу «белок — белок» способствует узнаванию и нейтрализации биологического действия антигенов. Защитная функция белков проявляется и в способности ряда белков крови к свертыванию. Свертывание белка плазмы кровифибриногена приводит к образованию сгустка крови, что предохраняет от потери крови при ранениях.
Гормональная функция. Обмен веществ в организме регулируется разнообразными механизмами. В этой регуляции важное место занимают гормоны, вырабатываемые в железах внутренней секреции. Ряд гормонов представлен белками или полипептидами, например гормоны гипофиза, поджелудочной железы и др.
Белки служат и одним из источников энергии в клетке, т. е. выполняют энергетическую функцию. При полном расщеплении 1 г белка выделяется 17,6 кДж энергии.
Закрепление
Что такое белки?
Перечислить виды пространственной конфигурации белков?
Какую роль играют водородные связи в строении белковых молекул?
Охарактеризуйте физические свойства белков.
Какие реакции характерны для белков?
Что такое денатурация белков?
Какие функции выполняют белки в организме?
Творческое задание (парная работа)
Составить синквейн по теме «Белки»
Белки.
2. Глобулярные, фибриллярные.
3. Защищают, регулируют, катализируют.
4. Мономерами являются аминокислоты.
5. Жизнь.
Приложение 2,3.
Рефлексия
Сегодня на уроке я…..
Домашнее задание
Пар. 3.2.1 Записи в тетр.
Приложение 1.
«Вода и минеральные вещества клетки»
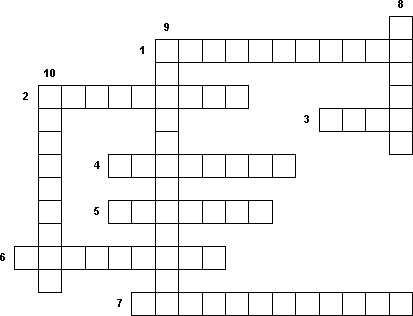
Вещества плохо, или совсем не растворяющиеся в воде.
2. Вода, находящаяся в межклетных пространствах, сосудах, вакуолях, полостях организма.
3. Одно из самых распространённых веществ на нашей планете.
4. Раствор, содержащий смесь какой-либо слабой кислоты и её растворимой соли.
5. Кислота, входящая в состав желудочного сока, способствующая перевариванию белковой пищи.
6. Поверхностное состояние воды, которое возникает благодаря образованию водородных связей между молекулами воды и молекулами других веществ.
7. Способность воды, поглощать тепловую энергию при минимальном повышении собственной температуры.
8. Остатки этой кислоты способствуют выведению из организма нерастворимых в воде веществ.
9. Вещества, хорошо растворимые в воде.
Приложение 2.
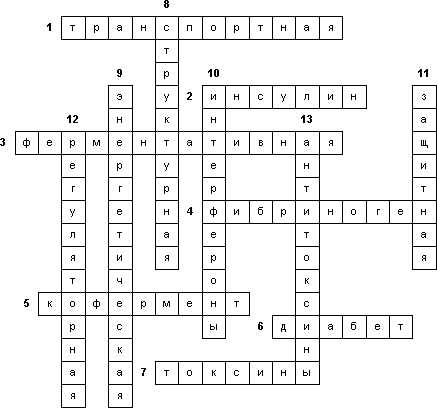
«Белки – органические полимеры. Строение белков».

1. Химическая связь, образующаяся в ходе реакции полимеризации.
2. Структура белковой молекулы, возникающая в результате соединения нескольких глобул в сложный комплекс.
3. Структура белка, имеющая вид клубка.
4. Структура белковой молекулы, представляющая линейную последовательность АК, в составе полипептидной цепи.
5. Белки, состоящие только из аминокислот (АК).
6. Структура белка, возникающая в результате образования водородных связей между СО– и NН–группами разных аминокислотных остатков полипептидной цепи.
7. Белки, содержащие небелковую часть.
8. Незаменимая аминокислота, которую человек получает с пищей в готовом виде.
9. Структура представляющая собой причудливую, но для каждого белка специфическую конфигурацию.
10. Утрата белковой молекулой природной структуры, под воздействием температуры, химических веществ, обезвоживания, облучения и других факторов.
11. Пространственные формы белковых молекул.
12. Белки, содержащие в себе углеводы, жиры, нуклеиновые кислоты … .
13. Белок, состоящий только из белковых молекул.
Приложение 3.
«Белки – органические полимеры. Функции белков».

1. Функция, при которой гемоглобин переносит кислород из лёгких к клеткам других тканей.
2. Гормон, регулирующий содержание глюкозы в крови.
3. Функция, при которой белковые молекулы ферментов способны ускорять течение биохимических реакций в клетке в сотни миллиардов раз.
4. Белок, предохраняющий организм от кровопотери.
5. Небелковое соединение в молекуле фермента.
6. Заболевание, возникающее при недостатке инсулина.
7. Белки, выделяемые организмом, являющиеся сильными ядами.
8. Функция, когда белок является основой всех биологических мембран органоидов клетки.
9. Функция белка, когда он может стать источником энергии в клетке.
10. Универсальные противовирусные белки.
11. Функция белка, предохраняющая организм от вторжения чужеродных организмов и от повреждений.
12. Функция белка, когда он регулирует различные физиологические процессы в организме.
13. Белки, способные подавлять действия ядов.


infourok.ru
Урок биологии по теме «Функции белков». 10-й класс
Разделы: Биология
Цель урока: используя знания о строении и свойствах белков расширить представления о функциях белков через творческую и исследовательскую деятельность (Приложение 1. Слайд №2).
Задачи (Слайд №3)
Образовательные:
Расширить знания о белках как природных полимерах, о многообразии их функций во взаимосвязи со строением и свойствами.
Развивающие:
1. Развивать мышление учащихся и умение
устанавливать причинно-следственные связи на
примере изучения свойств и функций белка.
2. Развивать практические умения постановки
цитологических опытов при установлении роли
белков ферментов.
3. Развивать умение делать выводы на основе
практических работ, развивать умение
самостоятельно получать информацию из
дополнительных информационных источников
(информационная компетентность).
4. Развивать умение структурировать материал.
5. Формировать способность анализировать свою
деятельность.
Воспитательные:
1. Воспитывать умение работать в группе
2. Воспитывать аккуратность учащихся при
выполнении и оформлении практических работ и
записей в тетради.
Тип урока: комбинированный с использованием исследовательской деятельности.
Технологии: тестовая, ИКТ, проблемного обучения.
Методы: частично-поисковый, словесный, наглядный, исследовательский.
Оборудование: презентация «Функции белков», компьютер с мультимедийным проектором, лабораторное оборудование к исследованию по теме «Ферментативная функция белка»: чашки петри, пероксид водорода, пипетка, кусочки вареного и сырого мяса, вареного и сырого картофеля, речной песок.
Методическое обеспечение:
- Раздаточный материал – текст «Белки» (Приложение 2), инструктивная карточка к лабораторной работе «Ферментативная функция белков» (Приложение 3), задание на установление соответствия между белками и их функциями (Приложение 4). Презентация Microsoft PowerPoint «Функции белков» (Приложение 1) – (POWER POINT).
- Актуальность использования средств ИКТ
- Возможность представления в мультимедийной форме уникальных информационных материалов (Приложение 5).
ХОД УРОКА
1. Организационное начало урока (приветствие, проверка готовности к работе, психологический настрой на урок) (Слайд № 4).
Притча
“Жил мудрец, который знал все. Один человек
захотел доказать, что мудрец знает не все. Зажав в
ладонях бабочку, он спросил: “Скажи, мудрец,
какая бабочка у меня в руках: мертвая или живая?”
А сам думает: “Скажет живая – я ее умерщвлю,
скажет мертвая – выпущу”. Мудрец, подумав,
ответил: “Все в твоих руках”.
В наших руках сегодня создать такую атмосферу на
уроке, при которой все будут чувствовать себя
комфортно.
Эпиграфом нашего урока будут слова А. Эйнштейна
«Радость видеть и понимать есть величайший дар
природы» (Слайд №5).
2. Мотивация
Задание: сделайте анализ круговой диаграммы (Слайд №6) и ответьте на вопросы:
1) Каков химический состав клетки?
2) Каких веществ органической природы в клетке
больше?
3) О чем свидетельствует сходство химического
состава клеток?
«Жизнь – это способ существования белковых
тел» (Ф. Энгельс) (Слайд №7).
Ни одно вещество химики не изучали так долго, как
белок прежде, чем удалось разгадать их
строение. От первых шагов на пути познания
состава белка до расшифровки структуры прошло
более двухсот лет.
Любой биологический объект, начиная от вирусов и
заканчивая человеком, состоит в основном из
белков (в пересчете на сухое вещество),
поэтому очень важно знать строение, свойства и
функции этих соединений.
3. Личностная значимость изучаемого материала
В сутки человек должен обязательно употреблять
100 г белка, иначе разовьется белковое голодание.
(Слайд №8) Недостаток белков в питании
вызывает у детей замедление роста и развития, а у
взрослых – глубокие изменения в печени,
нарушение деятельности желез внутренней
секреции, изменение гормонального фона,
ухудшение усвоения питательных веществ,
проблемы с сердечной мышцей, ухудшение памяти и
работоспособности.
В 70-х годах отмечались смертельные случаи у
людей, длительное время соблюдающих
низкокалорийные диеты с выраженным недостатком
белка. Происходило это из-за серьезных нарушений
в деятельности сердечной мышцы. Дефицит белка
уменьшает устойчивость организма к
инфекциям. Кроме того, белковая
недостаточность часто сопровождается
авитаминозом В12, А, Д, К и так далее, что также
влияет на состояние здоровья.
Вопрос к учащимся: «Какой личностный смысл для каждого из Вас имеют эти факты?»
4. Целеполагание
Задание: Установите соответствие между белками и их функциями (Приложение 4, Слайд №9).
Белки: Функции
А. Кератин 1. Строительная
Б. Гемоглобин 2. Запасающая
В. Актин 3. Защитная
Г. Антитела 4. Двигательная
Д. Миозин 5. Транспортная
Е. Фибриноген 6. Ферментативная
Ж. Коллаген 7. Регуляторная
З. Альбумин
И. Каталаза
К. Пепсин
Л. Инсулин
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
Почему Вы не можете выполнить данное задание? (ответ: не хватает знаний)
Постановка проблемного вопроса. В
состав клетки входят белки, жиры, углеводы,
нуклеиновые кислоты, вода, минеральные вещества,
но ни одно из веществ не выполняет столь
специфичных функций, как белки. Справедливо ли
это?
Учащиеся ставят цели и задачи работы на
данном уроке.
5. Актуализация знаний
Задания:
1. Работа со слайдами № 10-15 и беседа по вопросам:
1) Что такое полимеры?
2) Используя схему, ответьте доказательно, к каким
полимерам относятся белки?
3) Строение мономера белка.
4) Характеристика структурной организации белка.
2. Работа с текстом «Белки» (Слайд №16).
Вставьте в текст пропущенные термины и слова.
1) В состав белка входят следующие
элементы___,___,____,___,____. 2) Белки –
_______________,___________________ полимеры,
мономерами которых являются ____________________. 3) В
состав природных белков входят ______ аминокислот,
___ из них незаменимые, т.е. синтезируются в
организме и их поступление в организм не
обязательно вместе с пищей. 4) Мономеры белка
состоят из ___________,_________________.________________. 5) В состав
всех мономеров белка входят___________,________________, а
отличаются_______________. 6) Денатурация – процесс
изменения нативной структуры белка.
6. Изучение нового материала
Свойства и функции белка определяются его
структурой, строением и многообразием, поэтому
даже малые его дефекты структуры имеют серьезные
последствия.
Наследственное заболевание
серповидно-клеточная анемия связано с тем, что
при синтезе гемоглобина, состоящего
приблизительно из 600 аминокислотных остатков,
два из них меняются на другие. Это приводит к
нарушению функции гемоглобина: эритроциты
больных приобретают серповидную форму и
утрачивают способность к нормальному переносу
кислорода (Слайд №17).
Это пример связи структуры и функции
макромолекул.
Работа со слайдом № 18
Результатом данной работы будет таблица, которую по ходу работы будем заполнять.
Функции белков
Функция |
Сущность |
Пример |
| Структурная | Образование мембраны клеток и органоидов и др. структур | Коллаген, кератин |
| Регуляторная | Регулирование обмена веществ в организме | Некоторые гормоны – инсулин, глюкагон |
| Защитная | 1. При попадании в организм чужеродных
белков и микроорганизмов в лейкоцитах
образуются защитные белки. 2. Защита от потери крови при ранении в результате свертывания |
Антитела Фибриноген |
| Транспортная | Присоединение и перенос химических элементов по организму | Гемоглобин |
| Сократительная | Осуществление всех типов движения | Актин, миозин |
| Запасающая | Резерв для организма, плода | Яичный альбумин, казеин молока. |
| Токсическая | Змеиный яд, дифтерийный токсин | |
| Энергетическая | Не основной, но источник энергии в клетке | Расщепление 1 г белка – 17 кДж |
| Сигнальная | Узнавание молекул мембраной клетки | Гликопротеины |
| Ферментативная или каталитическая | Каталитическое ускорение биохимических реакций в клетке | Белки-ферменты (каталаза, пепсин, трипсин) |
Давайте вспомним: «О чем в ядре клетки хранится
наследственная информация» (представить
логическую цепь: признак – вещество – реакция –
белок – фермент). Павлов назвал ферменты
«возбудителями жизни и первым актом жизненной
деятельности».
Среди многочисленных функций белков особое
место занимает ферментативная.
Наука о ферментах называется энзимологией, а
ферменты – энзимами.
Выражение И.П. Павлова «Не все белки –
ферменты, но все ферменты белки» подчеркивают их
химическую организацию.
Далее учитель объясняет строение и механизм
действия фермента.
Чем же объясняется ускоряющее действие ферментов?
(Слайд 19) Каждый фермент имеет активный центр – определенная группа аминокислотных остатков. В активном центре происходит соединение фермента с субстратом (вещество, которое подлежит превращению) Форма активного центра и субстрата подходят друг другу как ключ к замку.
Процесс действия ферментов можно разделить на три стадии:
- Фермент распознает субстрат и связывается с ним.
- Образуется активный комплекс, состоящий из фермента и субстрата.
- Отделение продукта в результате ферментативной реакции.
Свойства ферментов (анализ графиков) (Слайды 20-23)
Далее учащимся предлагается выполнить исследование.
Исследовательское задание (Работа по группам):
Лабораторная работа «Ферментативное расщепление пероксида водорода в тканях организма» (Приложение 3)
Цель: сформировать знания о роли ферментов в клетках, закрепить умения проводить опыты и объяснять результаты работы.
Оборудование: свежий 3%-ный раствор пероксида водорода, штатив с пробирками, ткани растений (кусочки сырого и варёного картофеля) и животных (кусочки сырого и варёного мяса), пипетки, песок.
Ход работы:
1. Приготовьте четыре пробирки и поместите в первую пробирку — кусочек сырого картофеля, во вторую — кусочек варёного картофеля, в третью — кусочек сырого мяса, в четвёртую — кусочек варёного мяса. Капните в каждую из пробирок немного пероксида водорода. Пронаблюдайте, что будет происходить в каждой из пробирок.
2. Составьте таблицу, показывающую активность каждой ткани.
«Результаты исследования»
| № пробирки | Содержимое | Что делаю? | Что наблюдаю? |
| № 1 | |||
| № 2 | |||
| № 3 | |||
| № 4 |
Ответьте на вопросы (устно):
— В каких пробирках проявилась активность
фермента? Объясните почему?
— Как проявляется активность фермента в живых и
мёртвых тканях? Объясните наблюдаемое явление.
— Различается ли активность фермента в живых
тканях растений и животных?
— Как вы считаете, все ли живые организмы
содержат фермент каталазу, обеспечивающую
разложение пероксида водорода?
— Ответ обоснуйте.
— Сделайте вывод.
Группы учащихся отчитываются о выполнении
задания.
7. Рефлексия. Учащиеся выполняют задание, делают вывод (Слайд № 24).
8. Домашнее задание (Слайд № 25):
1. Задание для всех: глава 3.2.1., таблица «Функции
белков»,
2. Задание для проявляющих интерес к предмету:
найти классификацию ферментов в Интернете.
Интернет-ресурсы:
www.biology.asvu.ru — все о
биологии.
www.biodev.ru — все о биологии.
19.06.2014
xn--i1abbnckbmcl9fb.xn--p1ai
Конспект урока биологии для 10 класса «Строение и функции белков»
Метапредметный урок на тему: «Строение и функции белков».
«Белки: докажите тождество, что жизнь-белок»
Тип урока (рассчитано на 2 академических часа): урок обобщения и усвоения новых знаний.
Триединая дидактическая цель урока
Обучающая: полученные на уроках биологии, химии, физики знания о свойствах, нахождении в природе, значении белков интегрировать; развить знания о химических свойствах белков, о типах химической связи на примере водородной и ковалентной, раскрыть роль белковых молекул в зарождении, развитии, существовании живых организмов на Земле.
Развивающая: развитие речи, практических навыков работы с лабораторным оборудованием, схемами, опорными и обобщающими конспектами, умения работать с учебником; развитие мышления, памяти; развитие умения проводить анализ, синтез и на их основе обобщение и выводы.
Воспитывающая: формирование нравственных отношений, умения работать самостоятельно и вдвоем, выслушать мнение одноклассников, доказывать свое мнение; воспитание бережного отношения к природным объектам, воспитание здорового образа жизни.
Задачи урока
1. Учащиеся должны обобщить химические свойства белков, этапы синтеза белка клетке и роль белков в живом организме.
2. Уметь применять полученные знания при проведении качественных реакций на белок в лабораторных исследованиях, и выполнении упражнений по данной теме.
Оборудование урока: компьютер, медиапроектор, интерактивная доска; на доске – схема-конспект (блоки разных цветов), таблица “Важнейшие аминокислоты”; на партах – информационные учебные тексты в файлах, пробирки, химические стаканы, предметные стёкла, спиртовки, держатели пробирок, воронки, пипетки, спички.
Реактивы: растворы яичного белка, сульфата меди (II), гидроксида натрия, поваренной соли; концентрированный раствор азотной кислоты, кусочки шерстяной и синтетической ткани и мяса.
ХОД УРОКА
1. Организационный момент, приветствие
2. Актуализация знаний и целеполагание
Вступительное слово учителей химии и биологии (слова постепенно высвечиваются на презентации):
Меняя каждый миг свой образ прихотливой,
Капризна, как дитя и прозрачна, как дым,
Кипит повсюду жизнь в тревоге суетливой,
Великое смешав с ничтожным и смешным…
(Семен Надсон)
Жизнь существует на Земле миллиарды лет. Она заполняет все уголки нашей планеты. Озёра, реки, моря, океаны, горы, равнины, пустыни, даже воздух – населены живыми существами. Что же такое жизнь? Откуда она взялась на Земле? Эти вопросы волнуют людей всегда. В течении веков копились наблюдения, проводились исследования, создавались теории. Одни служили основой новых исследований, другие гибли в виду несостоятельности… Пожалуй, ни одно естественнонаучное явление не вызвало такой острой борьбы мировоззрений, какая всегда сопровождала проблемы живого. А причина этой борьбы – в самом объекте познания, его уникальности, неповторимости и сложности.
Не стоит забывать и слова русских поэтов:
“Не то, что мните вы, природа,
Не слепок, не бездушный лик.
В ней есть душа, в ней есть свобода,
В ней есть любовь, в ней есть язык”.
Ф. И. Тютчев
В одной из книг Библии сказано: “Вначале было слово”. Современная наука по аналогии начинается фразой: “Вначале был белок”.
Знаменитый путешественник и естествоиспытатель Александр Гумбольдт ещё на пороге XIX века вознамерился “распутать этот гордиев узел жизненных процессов”. Но наука XIX века ещё не могла видеть всей глубины изучаемого процесса. Постепенно было накоплено достаточное количество экспериментального материала, чтобы дать следующее определение жизни:
“Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, при чём с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка.” (Ф.Энгельс)
Вступительное слово учителя химии: Современная наука представляет жизнь как переплетение сложнейших химических процессов взаимодействия белков между собой и другими веществами. Следует подчеркнуть, что отдельные очищенные белки не имеют характерных признаков живого. Эту точку зрения можно подтвердить высказыванием члена Королевского общества Британской Академии наук ДжонаД.Бернала:
“Нельзя приписывать свойство жизни какому-либо одному соединению, оно лишь проявляется в результате многообразных реакций, в которых участвуют различные соединения”.
Какова цель нашего урока?
Учащиеся: Доказать или опровергнуть тождество: жизнь=белок. Изучив при этом состав, строение и функции белков.
Учитель биологии и химии: Давайте вернемся к домашнему заданию. Проверим, как Вы его выполнили (первоначальные сведения о белках были получены в 9 классе и на уроках биологии).
ТЕКСТ с ошибками (прием “Лови ошибку”)
Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.
После работы с текстом найденные ребятами ошибки записываются на доску, безкомментарий и без объяснения правильных ответов. Данная запись сохраняется в течение всего урока для проведения рефлексии.
3. Изучение нового материала
Учащиеся самостоятельно работают в составе трёх групп. На интерактивную доску высвечивается три блока схемы-конспекта, выделенных определённым цветом (1 блок – жёлтый, 2 блок – зелёный, 3 блок – синий), которые затем нужно заполнить.
Сразу нужно отметить, что желтый цвет концентрирует внимание, зеленый снимает усталость, синий вдохновляет на поиск новых идей (сдоровьесберегающие технологии).
Для самостоятельной работы группам выданы учебные тексты по блокам соответствующего цвета. После каждого учебного текста приведены разноуровневые вопросы и задания к нему. Вопросы первого уровня составлены по тексту, готовят учащихся к осмыслению и воспроизведению его. Вопросы второго уровня ставят перед учащимися познавательные задачи и требуют применения знаний. Рефлексия проводится в конце урока.
Алгоритм работы учащихся с учебными текстами:
прочитайте текст;
определите место полученной информации в этом блоке;
ответьте на вопросы, обсудите ответы в группе;
приготовьтесь к комментарию изученного материала по схеме-конспекту (выберете комментатора).
Блок №1 (желтого цвета). Состав и строение белков.
Консультант – учитель химии.
Вещества белковой природы известны давно. Начало их изучения положено в середине XVIII века итальянцем Я.Беккари, но только через 100 лет учёным удалось систематизировать свойства изученных белков, определить их состав и сделать вывод, что белки – это главный компонент живых организмов. Затем из белковых гидролизатов были получены продукты расщепления и возникли гипотезы о строении белков из аминокислот. Немецкий химик Эмиль Фишер первым выяснил как построены молекулы белков, и заложил основы их химического синтеза. В начале XX века Фишер доказал пептидную теорию строения белков, синтезировав полипептиды, состоящие из 3 – 18 аминокислотных остатков.
Химический состав
Белки – очень сложные органические соединения. Их молекулы содержат огромное число атомов – от нескольких тысяч до нескольких миллионов, в зависимости от вида белка. Поэтому белки называют высокомолекулярными органическими соединениями – биополимерами или макромолекулами. Каков же элементный состав белков?
Предположения учащихся: C, H, O, N, S, P и ионы металлов.
(демонстрируем молекулы гемоглобина, миоглобина и коллагена).
Учащиеся проводят опыты по определению качественного состава белков
Опыт №1
В трех пробирках – кусок мяса, сыра и яичный белок. Нагреем их на пламени спиртовки. Наблюдаем на стенках пробирок продукты горения.
Записывае вывод: в составе белков присутствуют C, H, O.
Опыт №2
Нагреваем яичный белок с раствором NaOH, поместим влажную универсальную индикаторную бумагу в горлышко пробирки.
Голубая окраска индикатора указывает на щелочную реакцию раствора, ощущается запах аммиака.
Записываем вывод: в состав белка входит азот.
Опыт №3
К раствору яичного белка добавить NaOH и несколько капель Pb(NO3)2. Нагреть содержимое пробирки.
Записываем вывод: в состав яичного белка входит сера.
Вопросы для вывода:
В чём причина многообразия белков?
К какому классу органических веществ можно отнести белки? Каков их состав?
Какой уровень организации белка определяет его биологическую активность?
Затем группы начинают работать с учебными текстами и учебником §27. Белки. Химия 10 класс. О.С. Габриелян и др.
После самостоятельного изучения текста §27 (О.С. Габриелян) стр. 226 – 230 учебника, учащиеся приступают к изучению дополнительных материалов, выданных учителем.
Можно выделить четыре уровня в строении полипептидной цепи.
Дополнительный материал для работы 1 группы (даны в приложении 1)
Разноуровневые вопросы и задания.
Первый уровень.
Как из аминокислот образуются молекулы белка?
Что такое первичная структура белка?
Что представляет собой вторичная структура белка?
За счёт чего молекула белка удерживается в данной структуре?
Что такое третичная структура белка?
За счёт чего молекулы некоторых белков могут закручиваться в клубок и удерживаться в этом виде?
Что такое четвертичная структура белка?
Второй уровень.
Напишите уравнение реакции получения трипептида из дипептида (изпользуйте формулу цистеина или серина), назовите полученныйтрипептид.
Сколько дипептидов может быть получено из двух аминокислот: аланина и лизина? Приведите структуры этих пептидов.
Могут ли измениться свойства белка при нарушении последовательности аминокислотных звеньев в линейной полимерной цепи?
Чем отличается вторичная структура белка от первичной?
Чем отличается третичная структура от вторичной и первичной?
Блок №2 (зеленого цвета). Свойства белков.
Консультант – учитель химии.
Алгоритм работы учащихся по блоку №2 несколько отличается от приведённого выше. Так, учащиеся первой и второй групп должны разделиться на две подгруппы для проведения опытов 1 и 2, 3 и 4. (Результаты каждого опыта обязательно обсуждаются в группе).
После самостоятельного изучения текста §27 стр. 231 – 234 учебника, учащиеся приступают к изучению дополнительных материалов, выданных учителем и проводят лабораторные опыты.
Белки – амфотерные электролиты. Глобулярные белки растворяются в воде и солевых растворах с образованием коллоидных систем, доказательством чего служит их способность рассеивать свет. Фибриллярные белки имеют волокнистое строение и нерастворимы в воде. Молекулы белков содержат свыше 50 аминокислотных остатков, поэтому их молекулярная масса велика.
Дополнительный материал для работы 1 группы (даны в приложении 2)
Разноуровненвые вопросы и задания.
Первый уровень
Задача.
В одном из белков содержится 0,32% серы. Определите относительную молекулярную массу данного белка, если предположить (упрощённо), что в молекуле содержится один атом серы.
Задача.
Известно, что для взрослого человека необходимо 1,5г белка на 1кг массы тела в день. Зная свою массу, определите суточную норму потребления белка для своего организма.
Задача.
Известно, что при продолжительности жизни 70 лет обновление белков в организме происходит в среднем 200 раз. Предположите, сколько раз произошло обновление белков в вашем организме.
Задача.
Закончите уравнение гидролиза трипептида:
Какая структура белка разрушается при гидролизе?
Обратима ли реакция гидролиза?
Каково значение качественных реакций на белки? Почему их называют цветными?
Второй уровень.
Определите по тексту значения понятий “высаливание”, “денатурация”, “коагуляция”; сравните результаты опытов, сделайте вывод о токсичности солей различных металлов.
Можно ли использовать белки как противоядие при отравлениях?
В каких случаях и с какой целью можно было бы применить качественные реакции в жизни?
В чём заключается сущность гидролиза?
Предположите, можно ли пищевые белки заменить другими компонентами рациона (например, углеводами и жирами), чтобы обеспечить важнейшие процессы в организме. Почему?
Блок №3 (жёлтого цвета). Функции белков.
Консультант – учитель биологии.
Биологическое значение белков очень велико.
В ходе эволюции появилось 1010 различных белков. Вы видите сколь огромно их количество. Сложность живого организма характеризуется количеством белков. Если в кишечной палочке их 3000, то в организме человека больше 5 млн.
1.Что происходит с белками в организме?
2. Какая из функций является ведущей?
3. На какую функцию будут потрачены белки только в крайнем случае, если нет жиров и углеводов?Дополнительный материал для работы 3 группы (даны в приложении 3)
Разноуровневые вопросы и задания.
Первый уровень.
Какова роль ферментов в организме?
Как образованы названия групп ферментов?
Что лежит в основе деятельности гормонов?
Где образуются гормоны в организме?
Какие ещё функции выполняют белки?
Какие белки определяют иммунные свойства организма?
Второй уровень
Предположите, каковы функции каждой группы ферментов.
Приведите примеры известных вам ферментов, назовите их функции.
Какую болезнь вызывает недостаток инсулина у человека?
Могут ли гормоны оказать негативное влияние на организм?
Расскажите о СПИДе и профилактике этого страшного заболевания.
Заключительное слово учителя.
Белки представляют собой природные вещества, построенные главным образом из аминокислот. Все ферменты, некоторые гормоны и антибиотики, некоторые токсины относятся к белкам. Белки являются важнейшей составной частью живых организмов и выполняют различные биологические функции. Важное свойство белков – денатурация, которая имеет физиологическое значение. Денатурация приводит к антигенной чувствительности белка, а иногда и полному блокированию ряда иммунологических реакций, к инактивации ферментов и нарушению обмена веществ. Учёные предполагают, что процессы старения связаны с медленно протекающей денатурацией. Может быть, именно в преодолении этого процесса – ключ продления жизни. Понятия “жизнь” и “белок” неразрывно связаны. Насколько многообразны белки, настолько сложна, загадочна и многолика сама жизнь. Подтверждением этого может стать высказывание Гёте: “Я всегда говорил и не устаю повторять, что мир бы не мог существовать, если бы был так просто устроен”.
Рефлексия (ошибки в тексте выделены)
Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислот в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке белок не меняет свой цвет.
5. Информация о домашнем задании
Творческое задание:
1. Почему жители крупных мегаполисов имеют проблему с кожей-дерматиты, полиносы?
2. Почему нельзя сушить кожаную обувь, прислонив ее непосредственно к батарее?
3. Собрав информацию об экологическом благополучии Благодарненского района, сделайте вывод о наиболее “комфортном” районе для счастливой жизни.
doc4web.ru
Урок биологии 10 класс «Строение и функции белков»
Метапредметный урок на тему: «Строение и функции белков».
«Белки: докажите тождество, что жизнь-белок»
Тип урока (рассчитано на 2 академических часа): урок обобщения и усвоения новых знаний.
Триединая дидактическая цель урока
Обучающая: полученные на уроках биологии, химии, физики знания о свойствах, нахождении в природе, значении белков интегрировать; развить знания о химических свойствах белков, о типах химической связи на примере водородной и ковалентной, раскрыть роль белковых молекул в зарождении, развитии, существовании живых организмов на Земле.
Развивающая: развитие речи, практических навыков работы с лабораторным оборудованием, схемами, опорными и обобщающими конспектами, умения работать с учебником; развитие мышления, памяти; развитие умения проводить анализ, синтез и на их основе обобщение и выводы.
Воспитывающая: формирование нравственных отношений, умения работать самостоятельно и вдвоем, выслушать мнение одноклассников, доказывать свое мнение; воспитание бережного отношения к природным объектам, воспитание здорового образа жизни.
Задачи урока
1. Учащиеся должны обобщить химические свойства белков, этапы синтеза белка клетке и роль белков в живом организме.
2. Уметь применять полученные знания при проведении качественных реакций на белок в лабораторных исследованиях, и выполнении упражнений по данной теме.
Оборудование урока: компьютер, медиапроектор, интерактивная доска; на доске – схема-конспект (блоки разных цветов), таблица “Важнейшие аминокислоты”; на партах – информационные учебные тексты в файлах, пробирки, химические стаканы, предметные стёкла, спиртовки, держатели пробирок, воронки, пипетки, спички.
Реактивы: растворы яичного белка, сульфата меди (II), гидроксида натрия, поваренной соли; концентрированный раствор азотной кислоты, кусочки шерстяной и синтетической ткани и мяса.
ХОД УРОКА
1. Организационный момент, приветствие
2. Актуализация знаний и целеполагание
Вступительное слово учителей химии и биологии (слова постепенно высвечиваются на презентации):
Меняя каждый миг свой образ прихотливой,
Капризна, как дитя и прозрачна, как дым,
Кипит повсюду жизнь в тревоге суетливой,
Великое смешав с ничтожным и смешным…
(Семен Надсон)
Жизнь существует на Земле миллиарды лет. Она заполняет все уголки нашей планеты. Озёра, реки, моря, океаны, горы, равнины, пустыни, даже воздух – населены живыми существами. Что же такое жизнь? Откуда она взялась на Земле? Эти вопросы волнуют людей всегда. В течении веков копились наблюдения, проводились исследования, создавались теории. Одни служили основой новых исследований, другие гибли в виду несостоятельности… Пожалуй, ни одно естественнонаучное явление не вызвало такой острой борьбы мировоззрений, какая всегда сопровождала проблемы живого. А причина этой борьбы – в самом объекте познания, его уникальности, неповторимости и сложности.
Не стоит забывать и слова русских поэтов:
“Не то, что мните вы, природа,
Не слепок, не бездушный лик.
В ней есть душа, в ней есть свобода,
В ней есть любовь, в ней есть язык”.
Ф. И. Тютчев
В одной из книг Библии сказано: “Вначале было слово”. Современная наука по аналогии начинается фразой: “Вначале был белок”.
Знаменитый путешественник и естествоиспытатель Александр Гумбольдт ещё на пороге XIX века вознамерился “распутать этот гордиев узел жизненных процессов”. Но наука XIX века ещё не могла видеть всей глубины изучаемого процесса. Постепенно было накоплено достаточное количество экспериментального материала, чтобы дать следующее определение жизни:
“Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, при чём с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка.” (Ф.Энгельс)
Вступительное слово учителя химии: Современная наука представляет жизнь как переплетение сложнейших химических процессов взаимодействия белков между собой и другими веществами. Следует подчеркнуть, что отдельные очищенные белки не имеют характерных признаков живого. Эту точку зрения можно подтвердить высказыванием члена Королевского общества Британской Академии наук ДжонаД.Бернала:
“Нельзя приписывать свойство жизни какому-либо одному соединению, оно лишь проявляется в результате многообразных реакций, в которых участвуют различные соединения”.
Какова цель нашего урока?
Учащиеся: Доказать или опровергнуть тождество: жизнь=белок. Изучив при этом состав, строение и функции белков.
Учитель биологии и химии: Давайте вернемся к домашнему заданию. Проверим, как Вы его выполнили (первоначальные сведения о белках были получены в 9 классе и на уроках биологии).
ТЕКСТ с ошибками (прием “Лови ошибку”)
Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.
После работы с текстом найденные ребятами ошибки записываются на доску, безкомментарий и без объяснения правильных ответов. Данная запись сохраняется в течение всего урока для проведения рефлексии.
3. Изучение нового материала
Учащиеся самостоятельно работают в составе трёх групп. На интерактивную доску высвечивается три блока схемы-конспекта, выделенных определённым цветом (1 блок – жёлтый, 2 блок – зелёный, 3 блок – синий), которые затем нужно заполнить.
Сразу нужно отметить, что желтый цвет концентрирует внимание, зеленый снимает усталость, синий вдохновляет на поиск новых идей (сдоровьесберегающие технологии).
Для самостоятельной работы группам выданы учебные тексты по блокам соответствующего цвета. После каждого учебного текста приведены разноуровневые вопросы и задания к нему. Вопросы первого уровня составлены по тексту, готовят учащихся к осмыслению и воспроизведению его. Вопросы второго уровня ставят перед учащимися познавательные задачи и требуют применения знаний. Рефлексия проводится в конце урока.
Алгоритм работы учащихся с учебными текстами:
прочитайте текст;
определите место полученной информации в этом блоке;
ответьте на вопросы, обсудите ответы в группе;
приготовьтесь к комментарию изученного материала по схеме-конспекту (выберете комментатора).
Блок №1 (желтого цвета). Состав и строение белков.
Консультант – учитель химии.
Вещества белковой природы известны давно. Начало их изучения положено в середине XVIII века итальянцем Я.Беккари, но только через 100 лет учёным удалось систематизировать свойства изученных белков, определить их состав и сделать вывод, что белки – это главный компонент живых организмов. Затем из белковых гидролизатов были получены продукты расщепления и возникли гипотезы о строении белков из аминокислот. Немецкий химик Эмиль Фишер первым выяснил как построены молекулы белков, и заложил основы их химического синтеза. В начале XX века Фишер доказал пептидную теорию строения белков, синтезировав полипептиды, состоящие из 3 – 18 аминокислотных остатков.
Химический состав
Белки – очень сложные органические соединения. Их молекулы содержат огромное число атомов – от нескольких тысяч до нескольких миллионов, в зависимости от вида белка. Поэтому белки называют высокомолекулярными органическими соединениями – биополимерами или макромолекулами. Каков же элементный состав белков?
Предположения учащихся: C, H, O, N, S, P и ионы металлов.
(демонстрируем молекулы гемоглобина, миоглобина и коллагена).
Учащиеся проводят опыты по определению качественного состава белков
Опыт №1
В трех пробирках – кусок мяса, сыра и яичный белок. Нагреем их на пламени спиртовки. Наблюдаем на стенках пробирок продукты горения.
Записывае вывод: в составе белков присутствуют C, H, O.
Опыт №2
Нагреваем яичный белок с раствором NaOH, поместим влажную универсальную индикаторную бумагу в горлышко пробирки.
Голубая окраска индикатора указывает на щелочную реакцию раствора, ощущается запах аммиака.
Записываем вывод: в состав белка входит азот.
Опыт №3
К раствору яичного белка добавить NaOH и несколько капель Pb(NO3)2. Нагреть содержимое пробирки.
Записываем вывод: в состав яичного белка входит сера.
Вопросы для вывода:
В чём причина многообразия белков?
К какому классу органических веществ можно отнести белки? Каков их состав?
Какой уровень организации белка определяет его биологическую активность?
Затем группы начинают работать с учебными текстами и учебником §27. Белки. Химия 10 класс. О.С. Габриелян и др.
После самостоятельного изучения текста §27 (О.С. Габриелян) стр. 226 – 230 учебника, учащиеся приступают к изучению дополнительных материалов, выданных учителем.
Можно выделить четыре уровня в строении полипептидной цепи.
Дополнительный материал для работы 1 группы (даны в приложении 1)
Разноуровневые вопросы и задания.
Первый уровень.
Как из аминокислот образуются молекулы белка?
Что такое первичная структура белка?
Что представляет собой вторичная структура белка?
За счёт чего молекула белка удерживается в данной структуре?
Что такое третичная структура белка?
За счёт чего молекулы некоторых белков могут закручиваться в клубок и удерживаться в этом виде?
Что такое четвертичная структура белка?
Второй уровень.
Напишите уравнение реакции получения трипептида из дипептида (изпользуйте формулу цистеина или серина), назовите полученныйтрипептид.
Сколько дипептидов может быть получено из двух аминокислот: аланина и лизина? Приведите структуры этих пептидов.
Могут ли измениться свойства белка при нарушении последовательности аминокислотных звеньев в линейной полимерной цепи?
Чем отличается вторичная структура белка от первичной?
Чем отличается третичная структура от вторичной и первичной?
Блок №2 (зеленого цвета). Свойства белков.
Консультант – учитель химии.
Алгоритм работы учащихся по блоку №2 несколько отличается от приведённого выше. Так, учащиеся первой и второй групп должны разделиться на две подгруппы для проведения опытов 1 и 2, 3 и 4. (Результаты каждого опыта обязательно обсуждаются в группе).
После самостоятельного изучения текста §27 стр. 231 – 234 учебника, учащиеся приступают к изучению дополнительных материалов, выданных учителем и проводят лабораторные опыты.
Белки – амфотерные электролиты. Глобулярные белки растворяются в воде и солевых растворах с образованием коллоидных систем, доказательством чего служит их способность рассеивать свет. Фибриллярные белки имеют волокнистое строение и нерастворимы в воде. Молекулы белков содержат свыше 50 аминокислотных остатков, поэтому их молекулярная масса велика.
Дополнительный материал для работы 1 группы (даны в приложении 2)
Разноуровненвые вопросы и задания.
Первый уровень
Задача.
В одном из белков содержится 0,32% серы. Определите относительную молекулярную массу данного белка, если предположить (упрощённо), что в молекуле содержится один атом серы.
Задача.
Известно, что для взрослого человека необходимо 1,5г белка на 1кг массы тела в день. Зная свою массу, определите суточную норму потребления белка для своего организма.
Задача.
Известно, что при продолжительности жизни 70 лет обновление белков в организме происходит в среднем 200 раз. Предположите, сколько раз произошло обновление белков в вашем организме.
Задача.
Закончите уравнение гидролиза трипептида:
Какая структура белка разрушается при гидролизе?
Обратима ли реакция гидролиза?
Каково значение качественных реакций на белки? Почему их называют цветными?
Второй уровень.
Определите по тексту значения понятий “высаливание”, “денатурация”, “коагуляция”; сравните результаты опытов, сделайте вывод о токсичности солей различных металлов.
Можно ли использовать белки как противоядие при отравлениях?
В каких случаях и с какой целью можно было бы применить качественные реакции в жизни?
В чём заключается сущность гидролиза?
Предположите, можно ли пищевые белки заменить другими компонентами рациона (например, углеводами и жирами), чтобы обеспечить важнейшие процессы в организме. Почему?
Блок №3 (жёлтого цвета). Функции белков.
Консультант – учитель биологии.
Биологическое значение белков очень велико.
В ходе эволюции появилось 1010 различных белков. Вы видите сколь огромно их количество. Сложность живого организма характеризуется количеством белков. Если в кишечной палочке их 3000, то в организме человека больше 5 млн.
1.Что происходит с белками в организме?
2. Какая из функций является ведущей?
3. На какую функцию будут потрачены белки только в крайнем случае, если нет жиров и углеводов?Дополнительный материал для работы 3 группы (даны в приложении 3)
Разноуровневые вопросы и задания.
Первый уровень.
Какова роль ферментов в организме?
Как образованы названия групп ферментов?
Что лежит в основе деятельности гормонов?
Где образуются гормоны в организме?
Какие ещё функции выполняют белки?
Какие белки определяют иммунные свойства организма?
Второй уровень
Предположите, каковы функции каждой группы ферментов.
Приведите примеры известных вам ферментов, назовите их функции.
Какую болезнь вызывает недостаток инсулина у человека?
Могут ли гормоны оказать негативное влияние на организм?
Расскажите о СПИДе и профилактике этого страшного заболевания.
Заключительное слово учителя.
Белки представляют собой природные вещества, построенные главным образом из аминокислот. Все ферменты, некоторые гормоны и антибиотики, некоторые токсины относятся к белкам. Белки являются важнейшей составной частью живых организмов и выполняют различные биологические функции. Важное свойство белков – денатурация, которая имеет физиологическое значение. Денатурация приводит к антигенной чувствительности белка, а иногда и полному блокированию ряда иммунологических реакций, к инактивации ферментов и нарушению обмена веществ. Учёные предполагают, что процессы старения связаны с медленно протекающей денатурацией. Может быть, именно в преодолении этого процесса – ключ продления жизни. Понятия “жизнь” и “белок” неразрывно связаны. Насколько многообразны белки, настолько сложна, загадочна и многолика сама жизнь. Подтверждением этого может стать высказывание Гёте: “Я всегда говорил и не устаю повторять, что мир бы не мог существовать, если бы был так просто устроен”.
Рефлексия (ошибки в тексте выделены)
Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислот в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке белок не меняет свой цвет.
5. Информация о домашнем задании
Творческое задание:
1. Почему жители крупных мегаполисов имеют проблему с кожей-дерматиты, полиносы?
2. Почему нельзя сушить кожаную обувь, прислонив ее непосредственно к батарее?
3. Собрав информацию об экологическом благополучии Благодарненского района, сделайте вывод о наиболее “комфортном” районе для счастливой жизни.
kopilkaurokov.ru
Открытый урок «Строение функции белков» 10 класс
Разработка урока по биологии
Макоевой Марьяны Мацуевны,
учителя биологии МКОУ «Лицей №1» г.п.Нарткала
Тема урока: «Строение и функции белков»
Слайд2
Цель: продолжить расширение и углубление знаний об органических веществах клетки на основе изучения строения и функций белков;
Задачи:
Познакомиться с ведущей ролью белков в строении и жизнедеятельности клетки.
Изучить строение макромолекул белка, имеющих характер информационных биополимеров.
Изучить свойства и функции белков.
Углубить знания о связи строения молекул веществ и их функции на примере белков
Ход урока
I. Организационный момент.
II. Изучение нового материала.
Слайд3
Жизнь – есть способ существования белковых, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка….
Ф.Энгельс
Изучая химический состав клетки, вы знаете, что все вещества входящие в ее состав делятся на две групп. Назовите эти группы. Сегодня на уроке мы продолжим изучать органические вещества – белки. Знания о белках имеют особенно важное значение для понимания всех процессов, происходящих в клетке. Белки лежат в основе всего живого. Поэтому эпиграфом нашего урока будет высказывание Энгельса: «Жизнь – есть способ существования белковых, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка…»
Вопрос. Какова роль белков в строении и жизнедеятельности клетки?
(В беседе учащиеся вспоминают известный из курса 8 – 9 классов материал о белках).
Среди органических компонентов клетки самыми важными являются белки. Они очень разнообразны и по строению, и по функциям. После удаления воды из клетки в сухом остатке на первом месте по содержанию стоят белки. Они составляют 10 – 20 % от сырой массы и от 50 до 80% от сухой массы клетки. Белки называют также протеинами (греч. hrоtos – первый, главный). Этим названием хотели подчеркнуть первостепенное значение белков для жизненного процесса.
Белки представляют собой высокомолекулярные (молекулярная масса до 1,5 млн углеродных единиц) органические соединения. Кроме С, О, Н, N. в состав белков могут входить S, Р, Fе. Белки построены из мономеров, которыми являются аминокислоты. Поскольку в состав молекул белков может входить большое число аминокислот, то их молекулярная масса бывает очень большой. Так, молекулярная масса инсулина – 5700, белка – фермента рибонуклеазы – 12 700, яичного альбумина – 36 00, гемоглобина – 65 000. Для сравнения: молекулярная масса спирта – 46, уксусной кислоты 60, бензола 78.
Белки являются нерегулярными полимерами.
Вопрос. Что является мономером белков?
В клетках разных живых организмов встречается свыше 170 различных аминокислот, но бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Из них может быть образовано ими 2∙ 1018 комбинаций, т. е. различных белков, которые будут обладать совершенно одинаковым составом, но различным строением. Но и это огромное число не предел — белок может состоять и из большего числа аминокислотных остатков, и, кроме того, каждая аминокислота может встречаться в белке несколько раз.
Слайд 4
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (— NН2 с основными свойствами, другая — карбоксильной группой (—СООН) с кислотными свойствами. Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение. В зависимости от количества аминокислот и карбоксильных групп, входящих в состав аминокислот, различают:
Нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу.
Кислые аминокислоты, имеющие более одной карбоксильной группы.
Основные аминокислоты, имеющие более одной карбоксильной группы.
Слайд 5
Наличие в одной молекуле аминокислоты и основной, и кислотной групп обусловливает их амфотерность и высокую реактивность. Через эти группы происходят соединения аминокислот при образовании белка. Связь образуется при взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой. Реакция, идущая с выделением воды, называется реакцией конденсации, а возникающая ковалентная азот – углеродная связь — пептидной — образуется пептид (греч. рерtos — сваренный). К свободным карбоксильной и аминогруппе могут присоединяться другие аминокислоты, удлиняя «цепь», называющуюся полипептидной. На одном конце такой цепи всегда будет группа NH2 (этот конец называется N-концом), а на другом конце — группа СООН (этот конец получил название С-конца)
Полипептидные цепи белков бывают очень длинными и включают самые различные комбинации аминокислот. В состав белка может входить не одна, а две полипептидные цепи и более. Так, в молекуле инсулина — две цепи, а иммуноглобулины состоят из четырех цепей.
Вопрос. На какие группы можно разделить аминокислоты в зависимости от того, могут ли они синтезироваться в организме?
Бактерии и растения могут синтезировать все необходимые им аминокислоты из более простых веществ. Многие животные, в том числе и человек, способны синтезировать не все аминокислоты, поэтому так называемые незаменимые аминокислоты (лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, тирозин, метионин) они должны получать с пищей в готовом виде. Заменимые аминокислоты – аминокислоты, которые в организме синтезируются.
В зависимости от аминокислотного состава белки бывают:
Слайд 6
Классификация белков. Сложность строения белковых молекул и чрезвычайное разнообразие их функций крайне затрудняют создание единой четкой классификации белков, на какой – либо одной основе.
Самостоятельная работа(1 минута)
Прочитайте статью «Классификация белков» на 42 стр. и ответе на вопросы:
Какие группы белков выделяют?
Какие характеристики лежат в основе данной классификация?
Среди белков различают протеины, состоящие только из белков, и протеиды — содержащие небелковую часть (например, гемоглобин).
Кроме простых белков, состоящих только из аминокислот, есть еще и сложные, в состав которых могут входить углеводы (гликопротеиды), жиры (липопротеиды), нуклеиновые кислоты (нуклеопротеиды) и др.
I. Классификация белков по их составу.
II. Классификация белков по их структуре.
Фибриллярные: наиболее важна вторичная структура (третичная почти или совсем не выражена). Нерастворимы в воде. Выполняют в клетке и в органах структурные функции, например в составе соединительной ткани (коллаген, миозин, кератин)
Глобулярные: наиболее важна третичная структура. Растворимы – легко образуют коллоидные суспензии. Выполняют функции ферментов, антител и др.
Промежуточные: фибриллярной природы, но растворимые. Примером может служить фибриноген, превращающийся в нерастворимый фибрин при свертывании крови.
Слайд7
III. Классификация белков по их функциям.
Уровни организации белковой молекулы. Молекулы белков могут принимать различные пространственные формы — конформации, которые представляют собой четыре уровня их организации.
Слайд 8
Под первичной структурой белка понимают число и последовательность аминокислот, соединенных друг с другом пептидными связями в полипептидной цепи. Первые исследования по выяснению аминокислотной последовательности белков были выполнены в Кембриджском университете Ф. Сэнгером, дважды удостоенным за свои работы Нобелевской премии. Сэнгер работал с гормоном инсулином. Это был первый белок, для которого удалось выяснить аминокислотную последовательность. Работа заняла ровно 10 лет (1944 – 1954гг.) В молекуле инсулина входит 51 аминокислота, а молекулярная масса этого белка равна 5733. Молекула состоит из двух полипептидных цепей. Удерживаемых вместе дисульфидными мостиками
Первичная структура уникальна для любого белка и определяет его форму, свойства и функции.
В организме человека свыше 10 000 различных белков, и все они построены из одних и тех же 20 станрдантных аминокислот. Аминокислотная последовательность белка определяет его биологическую функцию. В свою очередь эта аминокислотная последовательность однозначно определяется нуклеотидной последовательностью.
Слайд 9
Вторичная структура белков возникает в результате образования водородных связей между группами — СООН и — NН2 — разных аминокислотных остатков полипептидной цепи. Хотя водородные связи малопрочные, но благодаря их значительному количеству в комплексе они обеспечивают довольно прочную структуру. Белковая молекула напоминает растянутую пружину. Ренгено – структурный анализ показывает, что на один виток спирали приходится 3,6 аминокислотного остатка.
Слайд 10
Третичная структура представляет собой причудливую, но для каждого белка специфическую конфигурацию, имеющую вид клубка (глобулу). Прочность третичной структуры обеспечивается ионными, водородными и дисульфидными (—S—S—) связями между остатками цистеина, а также гидрофобным взаимодействием.
Слайд 11
Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких глобул в сложный комплекс. Полипептидные цепи удерживаются в молекуле вместе за счет гидрофобных взаимодействий, а также при помощи водородных и ионных связей Например, гемоглобин крови человека представляет комплекс из четырех таких субъединиц: из двух α — цепей и двух β-цепей. Две α — цепи содержат по 141 аминокислотному остатку, а две β-цепи – по 146 остатков. Полную структуру гемоглобина определили Кендрью и Перуц.
Некоторые вирусы, например вирус мозаики табака, имеют белковую оболочку, состоящую из многих полипептидных цепей, упакованных высокоупорядочным образом.
Слайд12
Свойства белков.
Белки обладают рядом физико – химических свойств, вытекающих из их структурной организации. Это во многом обуславливает функциональную активность каждой молекулы.
Во — первых, белки – преимущественно водорастворимые молекулы и, следовательно, могут проявлять свою функциональную активность только в водных растворах.
Во – вторых, белковые молекулы несут большой поверхностный заряд. Это определяет целый ряд электрохимических эффектов, например изменение проницаемости мембран каталитической активности и других функций.
В – третьих, белки термолабильны, т. е. проявляют свою активности в узких температурных рамках.
Утрата белковой молекулой своей природной структуры называется денатурацией. Она может возникать под воздействием температуры, химических веществ, обезвоживания, облучения и других факторов. Если при денатурации не нарушена первичная структура, то при восстановлении нормальных условий белок способен воссоздавать свою структуру. Этот процесс называется ренатурацией. Отсюда следует, что все особенности строения макромолекулы белка определяются его первичной структурой.
Слайд13
Функции белков. Белки выполняют целый ряд функций как в каждой клетке, так и в целом организме. Функции белков многообразны.
Белки являются основой всех биологических мембран, всех органоидов клетки, таким образом они выполняют структурную (строительную) функцию. Так, коллаген является важным составным компонентом соединительной ткани, кератин — компонент перьев, волос, рогов, ногтей, эластин — эластичный компонент связок, стенок кровеносных сосудов.
Слайд14
Очень важна ферментативная функция белков. Белковые молекулы ферментов способны ускорять течение биохимических реакций в клетке в сотни миллионов раз. К настоящему времени выделено и изучено более тысячи ферментов, каждый из которых способен влиять на скорость течения той или иной биохимической реакции.
Молекулы одних ферментов состоят только из белков, другие включают белок и небелковое соединение, или кофермент. В качестве коферментов выступают различные вещества, как правило, витамины и неорганические — ионы различных металлов.
Ферменты участвуют как в процессах синтеза, так и распада. При этом ферменты действуют в строго определенной последовательности, они специфичны для каждого вещества и ускоряют только определенные реакции. Встречаются ферменты, которые катализируют несколько реакций. Избирательность действия ферментов на разные химические вещества связана с их строением. Каталитическая активность фермента определяется не всей его молекулой, а определенным участком молекулы фермента, который называется его активным центром. Субстрат взаимодействует с ферментом, причем связывание субстрата осуществляется именно в активном центре. Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные молекулы в силу их пространственного соответствия, они подходят друг к другу, «как ключ к замку».
Рассмотрите рис. 16 «Схема образования комплекса «фермент—субстрат»
На заключительном этапе химической реакции комплекс «фермент—субстрат» распадается с образованием конечных продуктов и свободного фермента. Освободившийся при этом активный центр фермента может снова принимать новые молекулы вещества-субстрата.
Важное значение имеет транспортная функция белков. Так, гемоглобин переносит кислород из легких к клеткам других тканей. В мышцах эту функцию выполняет белок миоглобин. Сывороточный альбумин крови способствует переносу липидов и жирных кислот, различных биологически активных веществ. Белки-переносчики осуществляют перенос веществ через клеточные мембраны.
Слайд15
Специфические белки выполняют защитную функцию. Они предохраняют организм от вторжения чужеродных организмов и от повреждения. Так, антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки; интерфероны — универсальные противовирусные белки; фибриноген, тромбин и другие предохраняют организм от кровопотери, образуя тромб.
Многие живые существа для обеспечения защиты выделяют белки, называемые токсинами, которые в большинстве случаев являются сильными ядами. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
Регуляторная функция присуща белкам-гормонам (регуляторам). Они регулируют различные физиологические процессы. Например, наиболее известным гормоном является инсулин, регулирующий содержание глюкозы в крови. При недостатке инсулина в организме возникает заболевание, известное как сахарный диабет.
Белки могут выполнять энергетическую функцию, являясь одним из источников энергии в клетке. При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Но в качестве источника энергии белки используются крайне редко. Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Роль белка в жизни клетки огромна. Современная биология показала, что сходство и различие организмов определяются, в конечном счете набором белков. Чем ближе организмы друг к другу в систематическом положении, тем более сходны их белки.
Слайд16
Выводы:
Белки как макромолекулы – основа жизни.
Мономерами белков являются аминокислоты.
Первичная структура белка определяется генотипом.
Вторичная, третичная и четвертичная структурная организация зависят от первичной структуры.
Все биологические катализаторы – ферменты – имеют белковую природу.
Белковые молекулы обеспечивают иммунологическую защиту организма от чужеродных веществ.
Слайд17
Проверьте себя
Каким образом происходит соединение двух аминокислот, приводящих к образованию дипептида?
Каков характер связей в первичной, самой простой структуре молекулы белка?
Как называется структура молекулы белка, возникающая путем образования водородных связей между остатками карбоксильных и аминогрупп разных аминокислот одной молекулы белка?
Каким образом третичная структура превращается в четвертичную?
Что такое антитела?
Слайд18
Каждому термину, указанному в левой колонке. Подберите соответствующее ему определение, приведенное в правой колонке.
Первичная структура белка
Процесс утраты белковой молекулой своей структурной организации.
2. Денатурация
Б. Часть молекулы фермента, ответственная за присоединение и преобразование веществ.
3. Ренатурация
В. Последовательность аминокислотных остатков в полипептидной цепи, определенная генотипом.
4. Активный центр фермента
Г. Низкомолекулярные органические соединения различной природы, многие из которых являются предшественниками активных центров ферментов.
5. Витамины
Д. Процесс восстановления структурной организации белковой молекулы.
Слайд19
Домашнее задание: Изучить §11, ответить на вопросы на с. 46, заполнить таблицу, повторить § 9 -10. Подготовить сообщения или рефераты на темы: «Белки – биополимеры жизни», «Функции белков – основа жизнедеятельности каждого организма на Земле», «Многообразие ферментов, их роль в жизнедеятельности клеток и организмов».
infourok.ru
Урок биологии в 10 классе по теме «Строение и функции белков».
Данные об автореАвтор(ы):
Большова Тамара ГеннадиевнаМесто работы, должность:
МБОУ «Тюмеревская СОШ», учитель биологии
Регион:
Республика Чувашия Характеристики урока (занятия)Уровень образования:
среднее (полное) общее образованиеЦелевая аудитория:
Учитель (преподаватель)Класс(ы):
10 классПредмет(ы):
БиологияЦель урока:
Цель: углубить знания о строении молекулы белка, дать представление о структурах белка; развивать понимание взаимосвязи сложности строения белковой молекулы и выполняемыми ею функциями; воспитывать стремление к приобретению глубоких знаний в области молекулярной биологии.
Тип урока:
Урок изучения и первичного закрепления новых знанийУчащихся в классе (аудитории):
10Используемые учебники и учебные пособия:
1.В.Б.Сонин, С.Г.Мамонтов, Н.И.Сонин. Общая биология,10 класс, Дрофа.2013г
2.А.Ю.Ионцева, А.В.Торгалов. Биология в схемах и таблицах, Москва,2012г
Используемая методическая литература:
Л.А.Попова. Открытые уроки биологии.9-11 классы, Москва «Вако», 2013г
Используемое оборудование:
Оборудование: таблицы «Аминокислоты». «Модели первичной, вторичной, третичной и четвертичной структуры белка».
Предварительная подготовка: учащиеся подготовить дополнительный материал о значении белковых молекул в живой клетке
Используемые ЦОР:
Диск «Биология.Репетитор»
Краткое описание:
Урок биологии в 10 классе по теме «Строение и функции белков». Цель: углубить знания о строении молекулы белка, дать представление о структурах белка; развивать понимание взаимосвязи сложности строения белковой молекулы и выполняемыми ею функциями; воспитывать стремление к приобретению глубоких знаний в области молекулярной биологии.Урок биологии в 10 классе по теме «Строение и функции белков».
Цель: углубить знания о строении молекулы белка, дать представление о структурах белка; развивать понимание взаимосвязи сложности строения белковой молекулы и выполняемыми ею функциями; воспитывать стремление к приобретению глубоких знаний в области молекулярной биологии.
Оборудование: таблицы «Аминокислоты». «Модели первичной, вторичной, третичной и четвертичной структуры белка».
Предварительная подготовка: учащиеся подготовить дополнительный материал о значении белковых молекул в живой клетке.
Ход урока.
I. Повторение изученного материала.
1.Давайте на доске составим схему «Органические вещества»
Органические вещества
Белки Липиды Углеводы АТФ Нуклеиновые кислоты
2.Заполните таблицу «Функции углеводов»
Углеводы | Значение |
Моносахариды | |
Глюкоза | Источник энергии в клетке, содержится в крови, принимает участие в регуляции осмотического давления |
Галактоза | Входит в состав молочного сахара |
Фруктоза | Содержится в плодах и ягодах |
Полисахариды | |
Крахмал | Содержится в клубнях, плодах, семенах |
Гликоген | Накапливается в печени, мышцах, сердце, является поставщиком глюкозы в кровь |
Клетчатка (целлюлоза) | Источник глюкозы, входит в состав растительных оболочек клеток |
Хитин | Входит в состав клеточной стенки грибов и хитинового покрова, животных Типа Членистоногие |
3. Заполните таблицу «значение липидов»
Липиды | Значение |
1.Жиры. Животные (при комнатной температуре твердые) 2.Масла. Растительные (жидкие) | Источник энергии (1г -38,9кДж тепла), терморегулятор, источник воды, компонент витаминов, сохраняют запас энергии, выполняют строительную функцию |
Ответьте на вопросы: 1).В результате, каких процессов происходит образование моносахаридов? ( В результате фотосинтеза и расщепления полисахаридов)
2)Из каких веществ образуется глюкоза в процессе фотосинтеза? (Из углекислого газа и воды)
3) При расщеплении, какого органического вещества выделяется больше всего энергии (При расщеплении жиров выделяется больше всего энергии (38,9 кДж)
4)Что представляет собой молекула жира? (Молекула жира состоит из трехатомного спирта глицерина и жирных кислот).
II.Самостоятельное исследование. (Работа в группах)
На прошлом уроке мы изучили строение и значение углеводов и липидов. Тема сегодняшнего урока: «Строение и функции белков».
На сегодняшнем уроке вы должны провести исследование, работая в группах. Для этого класс делится на 4 группы. Каждой группе выдается задание, по которому вы должны провести свою работу и ответить на поставленные вопросы. Вы можете представить выполненное задание в форме таблиц, схем.
Задание для 1 группы. Строение белковой молекулы
1)Какое строение имеет молекула белка?
2) Что является мономером белка?
3) Благодаря какому свойству белковой молекулы в природе существует большое разнообразие белков?
(Примерный ответ. В 1871г. русский химик Н. Любавин (1845-1918) установил, что белки состоят из аминокислот. В настоящее время известно более 150 различных аминокислот, из них в построении молекул белков участвуют 20. Связь между молекулами аминокислот называется пептидной. В состав молекул белков входят 300-500 аминокислот, а иногда более 1000,поэтому такие молекулы называют полипептидами или полимерами.
Мономерами белка являются аминокислоты. Белки отличаются не только порядком чередования, количеством и составом своих мономеров. Результаты исследований показали, что число возможных вариантов белковых молекул и 100 аминокислотных остатков, в которых использовались все 20 аминокислот, равно 10130
Замена всего лишь одной аминокислоты на другую приводит к образованию новой белковой молекулы с совершенно иными свойствами. Если вместо заряженной глутаминовой кислоты в гемоглобине человека появляется остаток нейтрального валина, то возникает тяжелое заболевание – серповидноклеточная анемия, при котором гемоглобин кристаллизуется внутри эритроцитов и плохо взаимодействует с кислородом.
Итак, благодаря небольшому количеству аминокислот создается огромное количество белков.)
Задание для 2 группы. Структурные уровни организации белковой молекулы
1) Сколько уровней структур существует у белковых молекул?
2) Какими связями они поддерживаются?
3)Какая из структур самая прочная? Какая из структур самая слабая?
( При ответе учащиеся используют модели структур белковых молекул)
(Примерный ответ. Белковая молекула — очень сложная система. Соединенные между собой пептидными связями в длинную цепь, аминокислоты образуют первичную структуру. Она самая простая и прочная. Такая молекула была бы очень неудобна при выполнении своей функции.
Вторичная структура белка имеет вид спирали с большим количеством разветвлений, каждый из которых образован несколькими аминокислотами. Между группами СООН одной пептидной группы и NН2 другой пептидной группы образуется водородная связь. Водородная связь слабее пептидной связи между аминокислотами. Но так как водородных связей много, то образуется достаточно прочная структура.
Далее эта спираль скручивается в клубок – глобулу, причем это образование не хаотично, а строго определенно для каждого вида. Третичная структура белка образуется за счет S-S, солевых или сложноэфирных мостиков.
Каталитическая функция белковой молекулы может выполняться только на уровне третичной структуры. При соединении полипептидных цепей белков в единую структуру образуется четвертичная структура белка.
Гемоглобин содержит четыре полипептидные цепи, а гормон инсулин — две.
Под влиянием температуры, химических веществ, радиации происходит разрушение четвертичной, третичной, вторичной структур белка. Такое явление называется денатурацией белка. Если этот процесс не затрагивает первичной структуры, он может быть обратимым и белковая молекула восстанавливает свои свойства. Такой процесс называется ренатурацией.)
Задание для 3 группы. Размеры белковых молекул, их молекулярная масса и длина
1)Определите размеры белковых молекул.
2) Подсчитайте молекулярную массу белка.
3)Вычислите длину белковой молекулы.
(Примерный ответ. Белковые молекулы, по сравнению с углеводами и жирами, имеют значительно большие размеры. Молекула белка имеет формулу: C1861H3021O576N468 S21.
Молекулярная масса гемоглобина составляет 68000, лактогемоглобина-35200, рибонуклеазы – 12700. Для сравнения молекулярная масса глюкозы -180, поваренной соли -58.
Как подсчитать молекулярную массу белка? В среднем молекулярная масса аминокислоты равна 100. Для подсчета необходимо узнать количество аминокислот, входящих в состав данной молекулы:
Мб = Ма* па, где Мб – молекулярная масса белка, Ма –молекулярная масса аминокислоты, па –количество аминокислот.
Для подсчета длины белковой молекулы используется средняя величина длины аминокислоты, равная 0,38нм. Эту величину умножают на количество аминокислот, входящих в данный белок:
lб = lа* па).
Задание для 4 группы. Значение белков.
1.Определите функцию белков. (В организме каждого человека около 100 тыс. различных белков. Процесс сокращения и расслабления мышц, перенос гемоглобином О2 и СО2, составная часть клетки-все это функции белков.)
2. Составьте таблицу «Значение белков».
Функции белков | Пример |
Строительная | Входит в состав всех мембран клетки. |
Двигательная | Реснички, жгутики, веретено деления, актин и миозин участвуют в сокращении и расслаблении мышц |
Защитная | Образование тромба при ранах, антитела связывают инородные белки |
Каталитическая | Биологические катализаторы: белки — ферменты |
Регуляторная | Гормоны инсулин и глюкагон |
Транспортная | Транспорт веществ через мембрану, перенос О2 и СО2 гемоглобином |
Энергетическая | При окислении аминокислот высвобождается энергия:1г -17,6кДж |
III. Заслушиваем выступления, подводим итоги.
IV. Первичное закрепление изученного материала.
Какие утверждения верны?
1. Белки природные биополимеры.
2. Основная функция белка строительная.
3. Мономером белка является глюкоза.
4. Белок гемоглобин выполняет ферментативную функцию
5. При окислении 1г аминокислоты освобождается 17,6 кДж энергии
6. Белки выполняют защитную функцию.
7. Первичная структура белка имеет вид спирали.
8. Разрушение структуры белка называется денатурацией.
9. Биологические катализаторы это белки – ферменты
10. В среднем молекулярная масса аминокислоты равна 100.
Ключ (1, 2, 5,6, 8,9,10)
V. Рефлексия учебной деятельности
— Что нового вы узнали на уроке?
— Какие затруднения у вас возникли в процессе работы на уроке?
— Что было самым важным на уроке?
VI. Подведение итогов.
Оценивание учащихся во время урока, комментирую оценки
Задание на дом: 1. Прочитать параграф 3.2.1.
2.Решите задачу: Молекула гемоглобина имеет молекулярную массу 68000. Определите длину молекулы гемоглобина.
Решение: 1) Мб = Ма* па, па= Мб/ Ма =68000/100 = 680аминокислот содержится в данной молекуле;
2) lб = lа* па =0,38*680 =т258,4нм.
Литература:
1.В.Б.Сонин, С.Г.Мамонтов, Н.И.Сонин. Общая биология,10 класс, Дрофа.2013г
2.А.Ю.Ионцева, А.В.Торгалов. Биология в схемах и таблицах, Москва,2012г
Л.А.Попова. Открытые уроки биологии.9-11 классы, Москва «Вако», 2013г
www.openclass.ru
Урок биологии в 10 классе (модульный) «Состав и строение белков. Функции белков»
Тема урока: Состав и строение белков. Функции белков – 10 класс
Уроки 5—6 (модульные).
Комплексная дидактическая цель: способствовать формированию умений самостоятельной работы с учебной литературой, поиска необходимой информации для выполнения заданий и овладение знаниями о химическом составе, уровнях организации, свойствах и функциях белков; развитие навыков проведения биологических опытов, наблюдений и формирование выводов на основе полученных результатов опыта.
Оборудование: таблица по общей биологии «Строение и уровни организации белка»; учебники А.А. Каменского, Ю.И. Полянского «Общая биология 10 — 11»; клубни картофеля, 3% раствор перекиси водорода, терки для картофеля, пробирки, пробиркодержатели, спиртовки, спички, вода.
Ход урока
I. Организационный момент
II. Самостоятельная работа с учебно-тематическими картами
П. Рефлексия в группах, обсуждение выполнения заданий учебных элементов.
IV. Выполнение лабораторной работы
V. Подведение итогов модульного урока, определение индивидуального домашнего задания
Строение и функции белков.
Номер учеб-ного элемента
Учебный материал с указанием заданий
Руководство по усвоению учебного материала
УЭ-0
Интегрирующая цель: в ходе работы с учебно- тематической картой вы должны выяснить особенности строения белковых молекул, их свойства и биологические функции.
Внимательно прочитайте цель урока.
УЭ — 1
Цель: выяснить особенности строения белковой молекулы.
I. Выполните следующие задания:
1. Какое из перечисленных ниже органических соединений является мономером белка:
глюкоза, глицерин, жирные кислоты, аминокислоты, моносахариды.
Работайте самостоятельно в рабочей тетради.
См.: учебник А.А. Каменского 10 кл., § 11, с.40;
Правильный ответ за задание № 1 – 3 балла,
2. Выполните формулу аминокислоты в общем виде. Укажите, какие функциональные группы входят в ее состав, каково значение радикала R ?
Работайте с партнером по парте. См.: учебник А.А. Каменского 10 кл, § 11, с. 40—41, рис. 12, 13;
Максимальное число баллов за задание № 2 – 1 балл.
3. Почему молекулы белка получили название «макромолекулы»?
См. текст учебника А.А. Каменского 10 кл., §11, с. 40; Правильный ответ № 3 — 2 б.
4. В организации белковых молекул участвует всего около 20 аминокислот, однако многообразие белков огромно. Чем это объясняется?
См.: уч. А.А. Каменского 10 кл., § 11, с. 40, рис. 12 Правильный ответ— З балла.
5. Найдите в предложенном полипептиде пептидные (амидные) связи, запишите формулу в тетрадь и покажите их:
Nh3 — CH – C – N – CH – C – N – CH – COOH
H O H CH O H CH
Ch4 Ch4 H S
См.: уч. А.А. Каменского 10 кл., § 11, с. 40 – 41;
Правильный ответ— 3 балла.
6. Рассмотрите классификацию аминокислот (рис. 12). Ответьте на вопросы:
1) На какие группы делятся аминокислоты?
2) Чем отличаются группы аминокислоты друг от друга?
3) Сколько полипептидных цепей может входить в состав белка? Приведите пример.
Заполните таблицу:
№Название группы аминокислот
Что входит в состав
Общая формула
См.: уч. А.А. Каменского 10 кл., § 11, с. 41-42, рис. 12 Правильный ответ— 8 баллов.
II. Оцените работу своего партнера.
Работайте в паре. Максимальное количество баллов по УЭ-1 —20 балл.
УЭ — 2
Цель: выяснить природу классификации белков по их составу.
Выполните следующие задания:
1. Белки делятся по сложности образования на группы:
Протеины — …
Протеиды — …
2. Какие белки и почему относят к простым или сложным?
Дайте определение: гликопротеиды, липопротеиды, нуклеопротеиды.
Работайте индивидуально.
См.: учебник А.А. Каменскою 10 кл., § 11, с. 42;
Правильный ответ оценивается в 3 балла.
УЭ — 3
Цель: изучить структурную организацию белковой молекулы и ее свойства.
Цель: структурную организацию белковой молекулы и ее свойства.
I. Выполните следующие задания:
1. Вставьте пропущенные слова:
«Аминокислотную последовательность в составе полипептидной цепочки относят к … структуре белка. В результате образования водородных связей между —СО— и —NН— группами разных аминокислотных
Работайте с партнером по парте. См.: учебник А.А. Каменского 10 кл, § 11, с. 41—42, рис. 14, 15;
Максимальное число баллов за задание 8 баллов.
остатков большинство белков имеют вид спирали — это … структура белка. Более плотная, трехмерная пространственная «упаковка» полипептида — … структура белка. Следующий уровень организации белковой молекулы — …, который воз —
никает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс».
2. Заполните таблицу:
№Уровень организации белковой молекулы
Какую форму имеет
Какие связи образуют её
3. Что такое конформация?
4. Молекулы белков обладают свойством денатурации. Что это такое? Почему в результате денатурации белки теряют свои функции? Схематично зарисуйте в тетради структуру белковой молекулы в активном состоянии и после денатурации. От чего зависит денатурация? Обратима ли она?
5. Какая структура белка определяет все особенности строения макромолекулы белка?
II. Обсудите и оцените свою работу.
Работайте в паре.
III. Поменяйтесь тетрадями с партнером по парте и оцените работу друг друга.
Максимальное количество баллов по УЭ-3 — 8 баллов.
УЭ — 4
Цель: изучить биологические функции белков.
I. Выполните следующие задания:
1. Белки выполняют в клетке много жизненных
функций. Запишите функции белков, характерные
для различных типов белковых молекул, заполните таблицу:
Типы белковФункции
Примеры
1. Структурные.
2. Ферменты.
3. Гормоны.
4.Сократительные
5. Транспортные.
6. Защитные.
7. Запасные.
Работайте индивидуально
Прочитайте текст учебника
А.А. Каменского 10 кл., § 11,
с. 43-46; дополнительный материал: учебник Ю.И. Полян
ского, §39, с. 154—155.
Правильный ответ— I4 баллов.
2. В каждой клетке содержатся тысячи ферментов. Что они собой представляют? Какова их роль в клетке? Почему при разрушении структуры ферментов жизнедеятельность клетки прекращается?
Работайте индивидуально.
См. текст учебника А.А. Каменского, §11, с. 44, рис. 16, с. 45; дополнительный материал: учебник Ю.И. Полянского, §39, с. 154 — 155.
Правильный ответ—3 балла.
3. Используя рисунок, объясните механизм взаимодействия фермента и субстрата.
См.: учебн. А.А
infourok.ru
