Химическая формула озона. Структурная формула озона
Высоко над нашими головами, в стратосфере, на высоте 19-48 км планета окружена озоном. Это разновидность кислорода. Если молекула кислорода в воздухе состоит из двух атомов кислорода, соединенных вместе – O2, то молекула, которая имеет три атома, обозначена формулой озона – O3. Его создает солнечный свет. Когда ультрафиолетовые лучи от Солнца проходят сквозь атмосферу, они разрушают обычные двухатомные молекулы кислорода. Каждый освобожденный атом присоединяется к соседнему О2. Так образовывается химическая формула озона – O3.

Что собой представляет озон?
Открыли впервые этот газ французские физики Фабри и Бьюиссон. Ими в 1913 г. было определено, что солнечные лучи с длиной волны от 200 до 300 нм активно поглощаются атмосферой Земли. Термин «озон» в переводе с греческого значит «ароматный», «душистый». Все знают характерный запах этого газа, возникающего после грозы. Кислород присутствует в атмосфере в трех аллотропических формах: О2 – молекулярном, О – атомарном и О3 – формула озона, которая получается при химическом соединении первых двух.
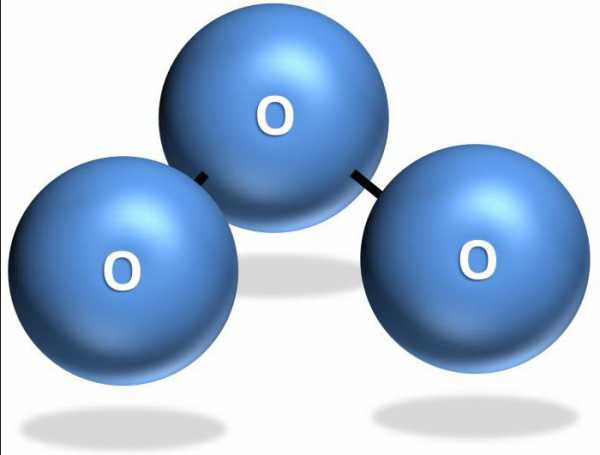
Свойства газа
Озоновый слой достаточно тонкий, практически незаметный. Если бы все молекулы этого газа, которые занимают 29 км космоса, объединились в единый твердый шар, его толщина занимала бы лишь третью часть сантиметра. Некоторое количество озона находится в воздухе над поверхностью Земли. Когда автомобильные выхлопные газы или смог выбрасываются в воздух, солнечный свет, вступая в реакцию с химическими элементами выбросов, образовывает озон. Особенно ощущается он в жаркий день, в наполненном смогом воздухе, ведь он достигает угрожающего здоровью уровня. Формула вещества озона физически непостоянна, и при концентрации его в воздухе более 9% газ взрывается, поэтому его хранение возможно лишь при низких температурах. При охлаждении до -111,90С газ превращается в жидкость.
Избыток озона
Человек не может жить в чистом кислороде, ему полезно малое количество озона в атмосфере, но чрезмерная концентрация его может быть смертельно опасной. Вдыхать его не нужно, потому что эта форма кислорода может повредить легкие. Спортсмены, которые вдыхают большое количество воздуха, насыщенного озоном, могут жаловаться на тяжесть и боль при вдохе. Деревья и растения, растущие вдоль шоссе, где воздух насыщен выхлопными газами, тоже страдают от избытка озона. Такая характеристика этого газа над самой поверхностью земли. Природное его содержание (одна часть его на десятки миллионов остальных частей воздуха) принимает участие в окислительных процессах, которые происходят на клеточном уровне в человеческом организме. В формуле озона выступает в качестве окислителя только один атом кислорода, а два оставшихся выделяются в виде свободного кислорода.
Полезные свойства
При применении полностью очищенного воздуха в помещениях, исследователи заметили рост количества заболеваний людей, находящихся в них. Причина оказалась простой – отсутствие озона в очищенном воздухе привело к расстройствам в организме. Регулярные незначительные дозы газа полезны и для профилактики болезней.
В чем заключается эффект газа? Учитывая результаты проведенных опытов, ученые пришли к выводу, что озон приводит к уничтожению почти всех имеющихся в природе вирусов, бактерий, простейших, а также плесени и дрожжевого грибка. За несколько минут малая порция (формула озона О3) в литре воздуха обезвреживает все опасные для человека вещества. Ведь озонирование – это природный процесс, обычный для организма. Даже в комнате озон освежает воздух, практически убирает риск заражения болезнями, которые переносятся воздушно-капельным путем, обезвреживает дым, пыль и аллергены, соединения тяжелых металлов и другие вредные для человека компоненты воздуха. Разлагаясь на воду, кислород и углекислый газ, эти соединения лишаются токсичности, убираются неприятные запахи. Учитывая формулу озона в химии, его высокая способность к окислению все шире применяется для обеззараживания воздуха и воды для питья.

Слой, находящийся на расстоянии 20 километров над поверхностью Земли, на самом деле защищает наше здоровье тем, что поглощает ультрафиолетовые лучи. Он действует как фильтр, охраняя Землю от вредного ультрафиолетового излучения. Без защитного слоя жизнь на планете была бы невозможна. Доказано, что растительный и животный мир появился на Земле лишь тогда, когда образовался мощный щит, ограждающий ее от солнечной радиации. Ультрафиолет помогает коже приобрести красивый загар, но, в то же время, он выступает главным виновником солнечных ожогов и причиной рака кожи.
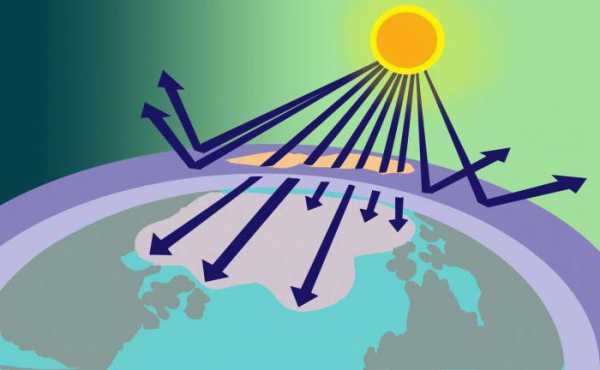
Озоновая дыра
В 70-х годах ученые, изучающие озоновый слой над планетой, выяснили, что химикаты, применяемые в холодильниках, кондиционерах и аэрозолях, могут уничтожать озон. Газы поступают в воздух при каждом случае ремонта этих приборов или при распылении различных аэрозолей. По мнению ученых, вредные газы, в конце концов, достигают молекул озона. При этом солнечная радиация освобождает из хлористо-фтористых углеводородов хлор, который разрушает структурную формулу озона, превращая его в обычный кислород. Таким образом, разрушается защитный слой. Еще через 15 лет британские ученые сделали потрясающее открытие: огромная дыра в озоновом слое разместилась над Антарктидой. Эта дыра появляется каждой весной и достигает размеров примерно территории США. Когда меняется направление ветра в связи со сменой времен года, дыра вновь наполняется озоновыми молекулами. При этом некоторое количество молекул заполняет дыру, а в других частях слой газа становится тоньше.
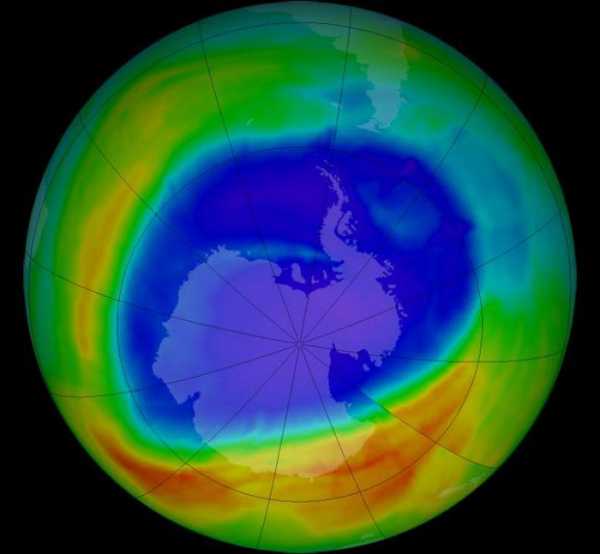
Чем грозит уменьшение защитного слоя?
Зимой 1992 года озоновый слой над Европой и Канадой стал тоньше на 20%. В тех местностях, где этот слой недостаточно плотный и не способен отфильтровать сильное излучение, очень заметно возрастает количество заболеваний раком кожи. Над самой Антарктидой ученые зафиксировали крайне высокий уровень одноокиси хлора, который образовывается в результате разрушения хлором озона. Исследователи подсчитали, что потеря всего 1% защитного слоя приводит к росту попадания на Землю ультрафиолетового излучения на 2%, а вместе с этим на 3-6% возрастает количество заболеваний раком кожи. Ультрафиолетовое излучение разрушает также иммунитет организма, делая человека более беззащитным перед инфекциями. Ультрафиолет может повреждать клетки всех растений, от злаков до деревьев.
Так как озоновый слой удерживает тепло, при его уменьшении воздух на этой широте охлаждается, меняя ветры и погоду в мире. Трудно предсказать, какое влияние окажет истощение слоя на климат в дальнейшем, ученые прогнозируют высушивание природных зон, утрату части растительности и недостаточное количество продуктов питания, если проблема уничтожения этого газа не будет решена. Даже при прекращении человеческой деятельности, влекущей за собой выбросы газов, которые разрушают защитный слой, ему бы понадобилось не менее 100 лет для возвращения к предыдущему уровню.
fb.ru
Сравните пожалуйста особенности озона и кислорода по данным критериям!
1. Химический элемент который образует вещество — кислород, хим. символ О, для обоих2. Молекулярная химическая формула: килсород О2, озон О3
3. Агрегатное состояние, цвет, запах, растворимость в воде
Кислород при нормальных условиях — газ без цвета, вкуса и запаха, слабо растворяется в воде (4,9 мл/100г при 0 °C, 2,09 мл/100г при 50 °C)
Озон при нормальных условиях — газ голубого цвета со специфическим запахом. Растворимость в воде при 0 °C — 0,394 кг/куб. м; (0,494 л/кг) , она в 10 раз выше по сравнению с кислородом.
4. Химическая активность
Обе модификации — окислители, но озон намного сильнее
Как правило, реакция окисления протекает с выделением тепла и ускоряется при повышении температуры. Озон — мощный окислитель, намного более реакционноспособный, чем двухатомный кислород. Окисляет почти все металлы (за исключением золота, платины и иридия) до их высших степеней окисления. Окисляет многие неметаллы.
5. Нахождение в природе
Кислород — самый распространенный на Земле элемент, на его долю (в составе различных соединений, главным образом силикатов) , приходится около 47,4 % массы твердой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 88,8 % (по массе) , в атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,12 % по массе. Более 1500 соединений земной коры в своем составе содержат кислород.
Озон образуется во многих процессах, сопровождающихся выделением атомарного кислорода, например при разложении перекисей, окислении фосфора и т. п.
При облучении воздуха жёстким ультрафиолетовым излучением образуется озон. Тот же процесс протекает в верхних слоях атмосферы, где под действием солнечного излучения образуется и поддерживается озоновый слой.
Атмосферный озон играет важную роль для всего живого на планете. Образуя озоновый слой в стратосфере он защищает растения и животных от жёсткого ультрафиолетового излучения. Поэтому проблема образования озоновых дыр имеет особое значение. Однако тропосферный озон является загрязнителем, который может угрожать здоровью людей и животных, а также повреждать растения.
6. Значение
Кислород – см. в Википедии
Применение озона обусловлено его свойствами:
•сильного окисляющего агента:
oдля стерилизации изделий медицинского назначения
oпри получении многих веществ в лабораторной и промышленной практике
oдля отбеливания бумаги
oдля очистки масел
•сильного дезинфицирующего средства:
oдля очистки воды и воздуха от микроорганизмов (озонирование)
oдля дезинфекции помещений и одежды
otvet.mail.ru
Озон (химический элемент): свойства, формула, обозначение
Крайне ценными для всего человечества свойствами обладает такой газ, как озон. Химический элемент, которым он образован, — это кислород О. На самом деле, озон О3 – одна из аллотропных модификаций оксигена, состоящая из трёх формульных единиц (О÷О÷О). Первое и более известное соединение – это сам кислород, точнее газ, который образован двумя его атомами (О=О) – О2.
Аллотропия – это способность одного химического элемента образовывать ряд различных по свойствам простых соединений. Благодаря ей человечество изучило и использует такие вещества, как алмаз и графит, моноклинная и ромбическая сера, кислород и озон. Химический элемент, имеющий такую способность, не обязательно ограничен только двумя модификациями, у некоторых их больше.
История открытия соединения
Составляющая единица многих органических и минеральных веществ, в том числе и такого как озон – химический элемент, обозначение которого О – оксиген, в переводе с греческого «oxys» — кислый, и «gignomai» — рождать.
Впервые новую аллотропную модификацию кислорода во время опытов с электрическими разрядами обнаружил в 1785 году голландец Мартин ван Марун, его внимание привлёк специфический запах. А веком позже француз Шенбейн отметил присутствие такого же после грозы, в результате чего газ был назван «пахнущий». Но учёные несколько обманулись, считая, что их обоняние учуяло сам озон. Запах, который они чувствовали, принадлежал органическим соединениям, окисленным при взаимодействии с О3, так как газ очень реакционноспособен.
Электронное строение
Один и тот же структурный фрагмент имеют О2 и О3 – химический элемент. Озон имеет более сложное строение. В кислороде же всё просто – два атома оксигена соединены двойной связью, состоящей из ϭ- и π-составляющей, согласно валентности элемента. О3 имеет несколько резонансных структур. 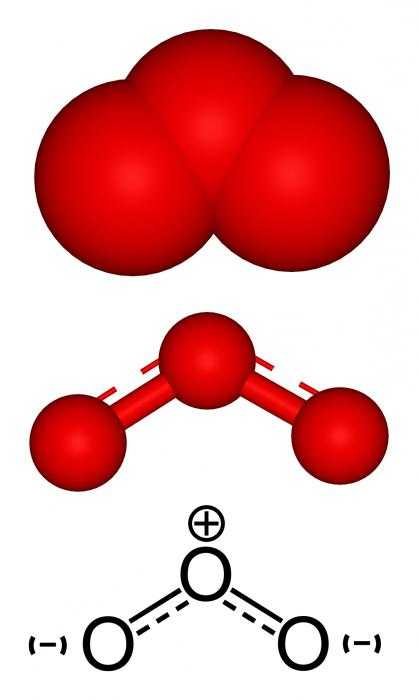 Кратная связь соединяет два кислорода, а третий имеет одинарную. Таким образом, вследствие миграции π-составляющей, в общей картине три атома имеют полуторное соединение. Эта связь короче, чем одинарная, но длиннее, чем двойная. Вероятность цикличности молекулы проведённые учёными эксперименты исключают.
Кратная связь соединяет два кислорода, а третий имеет одинарную. Таким образом, вследствие миграции π-составляющей, в общей картине три атома имеют полуторное соединение. Эта связь короче, чем одинарная, но длиннее, чем двойная. Вероятность цикличности молекулы проведённые учёными эксперименты исключают.
Методы синтеза
Для образования такого газа, как озон, химический элемент оксиген должен находиться в газообразной среде в виде отдельных атомов. Такие условия создаются при соударении молекул кислорода О2 с электронами во время электрических разрядов или другими частицами с большой энергией, а также при его облучении ультрафиолетом.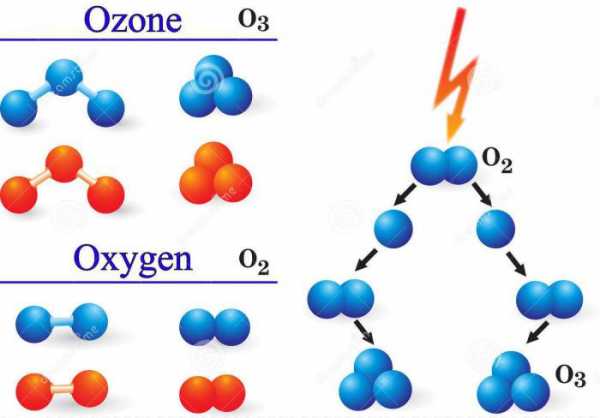
Львиная доля от общего количества озона в естественных условиях атмосферы образуется фотохимическим способом. Человек предпочитает в химической деятельности использовать другие методы, такие как, например, электролитический синтез. Он заключается в том, что в водную среду электролита помещают платиновые электроды и пускают ток. Схема реакции:
Н2О + О2 → О3 + Н2 + е—
Физические свойства
Кислород (О) – составная единица такого вещества как озон — химический элемент, формула которого, а также относительная молярная масса указаны в таблице Менделеева. Образуя О3, оксиген приобретает свойства, кардинально отличающиеся от свойств О2.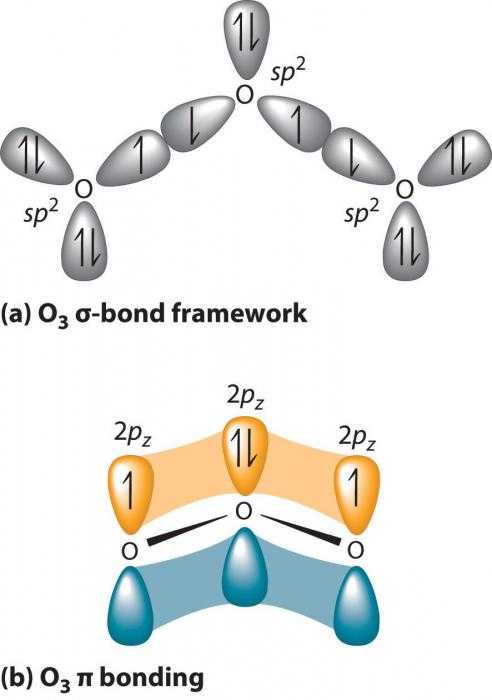
Газ голубого цвета – это обычное состояние такого соединения, как озон. Химический элемент, формула, количественные характеристики — все это определили при идентификации и изучении данного вещества. Температура кипения для него -111,9 °C, сжиженное состояние имеет темно-фиолетовый окрас, при дальнейшем понижении градуса до -197,2 °C начинается плавление. В твёрдом агрегатном состоянии озон приобретает чёрный цвет с фиолетовым отливом. Растворимость его в десять раз превышает это свойство кислорода О2. При самых незначительных концентрациях в воздухе чувствуется запах озона, он резок, специфичен и напоминает запах металла.
Химические свойства
Очень активным, с реакционной точки зрения, является газ озон. Химический элемент, который его образует – это кислород. Характеристики, определяющие поведение озона во взаимодействии с другими веществами, – это высокая окисляющая способность и неустойчивость самого газа. При повышенных температурах он разлагается с небывалой скоростью, процесс ускоряют и катализаторы, такие как оксиды металлов, хлор, диоксид азота и другие. Свойства окислителя присущи озону благодаря особенностям строения молекулы и подвижности одного из атомов оксигена, который отщепляясь, превращает газ в кислород: О3 → О2 + О·
Оксиген (кирпичик, из которого построены молекулы таких веществ, как кислород и озон) – химический элемент. Как пишется в уравнениях реакции — О·. Озон окисляет все металлы, за исключением золота, платины и его подгруппы. Он реагирует с газами, находящимися в атмосфере – оксидами серы, азота и прочими. Не остаются инертными и органические вещества, особенно быстро идут процессы разрывов кратных связей через образования промежуточных соединений. Крайне важно, что продукты реакций являются безвредными для окружающей среды и человека. Это вода, кислород, высшие оксиды различных элементов, окислы углерода. Во взаимодействие с озоном не вступают бинарные соединения кальция, титана и кремния с кислородом.
Применение
Основная область, где применяется «пахнущий» газ – это озонирование. Подобный метод стерилизации гораздо эффективнее и безопаснее для живых организмов, чем дезинфекция хлором. При очищении воды озоном не происходит образование токсичных производных метана, замещенных опасным галогеном.
Всё чаще такой экологический метод стерилизации находит применение в пищевой отрасли промышленности. Озоном обрабатывают холодильное оборудование, складские помещения для продуктов, с помощь него проводят устранение запахов.
Для медицины дезинфицирующие свойства озона также незаменимы. Им обеззараживают раны, физиологические растворы. Озонируют венозную кровь, а также «пахнущим» газом лечат ряд хронических заболеваний.
Нахождение в природе и значение
Простое вещество озон – элемент газового состава стратосферы, области околоземного пространства, расположенной на расстоянии порядка 20-30 км от поверхности планеты. Выделение этого соединения происходит во время процессов, связанных с электрическими разрядами, при сварке, работе аппаратов ксерокса. Но именно в стратосфере образуется и содержит 99% от общего количества озона, находящегося в атмосфере Земли.
Жизненно важным оказалось присутствие газа в околоземном пространстве. Он образует в нем так называемый озоновый слой, который защищает всё живое от смертельного ультрафиолетового излучения Солнца. Как ни странно, но наравне с огромной пользой, сам газ опасен для людей. Повышение концентрации озона в воздухе, которым дышит человек, вредно для организма, вследствие его крайней химической активности.
fb.ru
Химическая формула озона :: SYL.ru
Что собой представляет формула озона? Попробуем вместе выявить отличительные характеристики данного химического вещества.
Аллотропная модификация кислорода
Молекулярная формула озона в химии О3. Его относительная молекулярная масса составляет 48. В составе соединения есть три атома О. Так как формула кислорода и озона включает в себя один и тот же химический элемент, в химии их называют аллотропными модификациями.
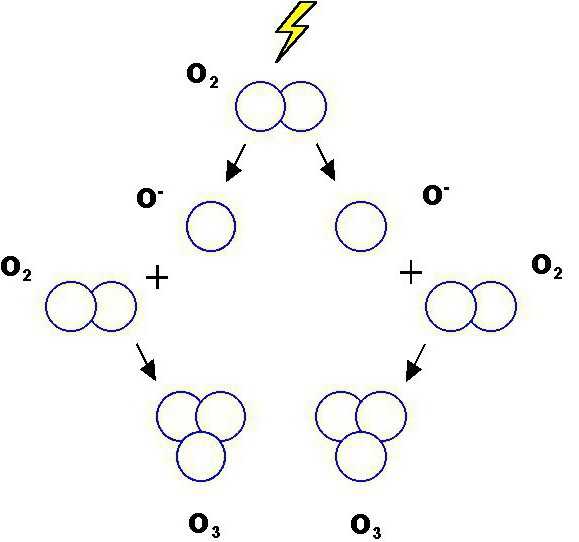
Физические свойства
При обычных условиях химическая формула озона – газообразное вещество, обладающее специфическим запахом, имеющим светло-голубой цвет. В природе данное химическое соединение можно ощутить во время прогулки после грозы по сосновому бору. Так как формула озона О3, он тяжелее кислорода в 1,5 раза. В сравнении с О2 растворимость озона значительно выше. При нулевой температуре 49 его объемов легко растворяется в 100 объемах воды. В незначительных концентрациях вещество не обладает свойством токсичности, ядом озон является только в значительных объемах. Предельной допустимой концентрацией считают 5% количества в воздухе О3. В случае сильного охлаждения он легко сжижается, а при понижении показателя температуры до -192 градусов становится твердым веществом.

В природе
Молекула озона, формула которого была представлена выше, в природе образуется при грозовом разряде из кислорода. Кроме того, О3 формируется при окислении смолы хвойных пород, он уничтожает вредные микроорганизмы, считается полезным для человека.
Получение в лаборатории
Как можно получить озон? Вещество, формула которого О3, образуется при пропускании через сухой кислород электрического разряда. Процесс осуществляется в специальном приборе – озонаторе. В его основе – две стеклянные трубки, которые вставлены одна в другую. Внутри располагается металлический стержень, снаружи есть спираль. После подключения к катушке высокого напряжения между внешней и внутренней трубкой возникает разряд, и кислород превращается в озон. Элемент, формула которого представлена в виде соединения с ковалентной полярной связью, подтверждает аллотропию кислорода.
Процесс превращения в озон кислорода является эндотермической реакцией, предполагающей существенные затраты энергии. В связи с обратимостью такого превращения наблюдается разложение озона, что сопровождается уменьшением энергии системы.
Химические свойства
Формула озона объясняет его окислительную способность. Он способен взаимодействовать с разными веществами, теряя при этом атом кислорода. Например, в реакции с иодидом калия в водной среде происходит выделение кислорода, образование свободного йода.
Молекулярная формула озона поясняет его способность вступать в реакцию практически со всеми металлами. Исключение составляют золото и платина. Например, после пропускания через озон металлического серебра наблюдается его почернение (образуется оксид). Под действием этого сильного окислителя наблюдается разрушение резины.
В стратосфере озон образуется благодаря действию УФ-облучения Солнца, формируя слой озона. Эта оболочка защищает поверхность планеты от негативного воздействия солнечной радиации.

Биологическое действие на организм
Повышенная окислительная способность данного газообразного вещества, образование свободных радикалов кислорода свидетельствуют о его опасности для организма человека. Какой вред способен нанести человеку озон? Он повреждает и раздражает ткани дыхательных органов.
Озон действует на холестерин, содержащийся в крови, вызывая атеросклероз. При продолжительном нахождении человека в среде, которая содержит повышенную концентрацию озона, развивается мужское бесплодие.
В нашей стране данный окислитель относят к первому (опасному) классу вредных веществ. Его среднесуточная ПДК не должна превышать 0,03 мг на кубический метр.
Токсичность озона, возможность его применения для уничтожения бактерий и плесени, активно применяют для дезинфекции. Стратосферный озон – прекрасный защитный экран земной жизни от ультрафиолетового излучения.

О пользе и вреде озона
Это вещество находится в двух слоях земной атмосферы. Тропосферный озон опасен для живых существ, негативно действует на сельскохозяйственные культуры, деревья, является компонентом городского смога. Стратосферный озон приносит человеку определенную пользу. Распад его в водном растворе зависит от рН, температуры, качества среды. В медицинской практике применяют озонированную воду различной концентрации. Озонотерапия предполагает прямой контакт данного вещества с организмом человека. Впервые подобная методика была применена в девятнадцатом веке. Американские исследователи проанализировали способность озона к окислению вредных микроорганизмов, рекомендовали медикам использовать это вещество при лечении простудных заболеваний.
В нашей стране озонотерапия начала применяться только в конце прошлого века. В терапевтических целях этот окислитель проявляет характеристики сильного биорегулятора, который способен увеличить результативность традиционных методик, а также проявить себя в качестве эффективного самостоятельного средства. После разработки технологии озонотерапии у медиков появилась возможность результативно бороться со многими заболеваниями. В неврологии, стоматологии, гинекологии, терапии, специалисты с помощью этого вещества борются с разнообразными инфекциями. Озонотерапия характеризуется простотой метода, его эффективностью, отличной переносимостью, отсутствием побочных эффектов, незначительными затратами.

Заключение
Озон является сильным окислителем, способным бороться с вредными микробами. Данное свойство широко применяют в современной медицине. В отечественной терапии озон используют в качестве противовоспалительного, иммуномодулирующего, противовирусного, бактерицидного, антистрессового, цитостатического средства. Благодаря его способности восстанавливать нарушения кислородного обмена, дает ему отличные возможности для лечебно-профилактической медицины.
Среди инновационных методик, основанных на окислительной способности данного соединения, выделим внутримышечное, внутривенное, подкожное введение данного вещества. Например, обработка пролежней, грибковых поражений кожи, ожогов, смесью кислорода и озона признана эффективной методикой.
В высоких концентрациях озон можно применять в качестве кровоостанавливающего средства. При низких концентрациях он способствует репарации, заживлению, эпителизации. Это вещество, растворенное в физиологическом растворе, является отличным средством для санации челюсти. В современной европейской медицине широкое распространение получила малая и большая аутогемотерапия. Оба метода связаны с введением в организм озона, использованием его окислительной способности.
В случае большой аутогемотерапии происходит введение озонового раствора заданной концентрацией в вену пациента. Малая аутогемотерапия характеризуется внутримышечным введением озонированной крови. Помимо медицины, этот сильный окислитель востребован в химическом производстве.
www.syl.ru
Формула озона в химии
Определение и формула озона
Может оставаться в состоянии переохлажденной жидкости до температуры (-250oC). плохо растворяется в воде, лучше в тетрахлориде углерода и различных фторхлоруглеродах. Очень сильный окислитель.
Химическая формула озона
Химическая формула озона – O3. Она показывает, что в составе молекулы этого вещества находится три атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу озона:
Mr(O3) = 3×Ar(O) = 3×16 = 48
Структурная (графическая) формула озона
Более наглядной является структурная (графическая) формула озона. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 1).
Рис. 1. Строение молекулы озона.
Электронная формула, показывающая распределение электронов в атоме по энергетическим подуровням показана ниже:
16O 1s22s22p6
Она также показывает, что кислород, из которого состоит озон, относится к элементам р-семейства, а также число валентных электронов — на внешнем энергетическом уровне находится 6 электронов (3s23p4).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Урок 16. Кислород и озон – HIMI4KA
В уроке 16 «Кислород и озон» из курса «Химия для чайников» мы рассмотрим кислород как химический элемент и как простое вещество; узнаем об истории его открытия; выясним, что такое озон и какими свойствами он обладает.

Исторически так сложилось, что химический элемент и одно из простых веществ, образованных атомами этого элемента, имеют общее название — кислород. Поскольку между этими понятиями существует принципиальная разница, следует четко различать, о чем идет речь — о кислороде как о химическом элементе или о простом веществе.
Кислород как химический элемент
Самым первым химическим элементом, к изучению которого мы приступаем, является кислород. Как вы уже знаете, химический знак кислорода — О. Относительная атомная масса кислорода равна 16:
Позднее вы узнаете, какое строение имеет атом кислорода и чем он отличается от атомов других химических элементов.
Когда говорят о кислороде как о химическом элементе, то подразумевают атомы кислорода. Например: «В состав многих сложных веществ входит кислород», «Массовая доля кислорода в глюкозе равна 53,3 %». В этих примерах речь идет об атомах кислорода (О), которые наряду с атомами других химических элементов входят в состав сложных веществ, следовательно, в данном случае речь идет о кислороде как о химическом элементе.
Кислород как простое вещество
Простое вещество кислород существует в виде молекул. Молекула кислорода состоит из двух атомов химического элемента кислорода (рис. 73), поэтому химическая формула кислорода как простого вещества — O2.
Поскольку относительная атомная масса кислорода равна 16, то относительная молекулярная масса простого вещества кислорода равна:
Следовательно, молярная масса кислорода равна:
Как у всех газов, молярный объем кислорода при нормальных условиях равен:
Когда говорят о кислороде как о простом веществе, то подразумевают вещество, имеющее формулу О2. Например: «Железные изделия быстро ржавеют в атмосфере влажного кислорода», «Для горения древесины необходим кислород». В этих примерах речь идет о веществе, имеющем формулу О2.
История открытия кислорода
История открытия самого важного для человека газа была долгой и запутанной. Впервые об открытии кислорода было сообщено в 1774 г. английским химиком Дж. Пристли. Он получил его при нагревании вещества HgO. Однако Дж. Пристли в то время не понял, что он получил новое газообразное вещество, и считал его разновидностью воздуха. Еще раньше в 1772 г. кислород был получен К. Шееле, но сообщение об этом он опубликовал только в 1777 г.
В 1774 г. Дж. Пристли сообщил о своих результатах великому французскому химику А. Лавуазье. Он тут же начал свои опыты и уже в 1775 г. сделал в Академии наук доклад «Мемуар о природе вещества, соединяющегося с металлами при прокаливании и увеличивающего их вес».
Происхождение названия «кислород» связано с образованием кислот в результате растворения в воде некоторых сложных веществ, содержащих атомы этого элемента. А. Лавуазье считал, что кислород — это обязательная составная часть всех кислот, что он «рождает» кислоты. Чтобы подчеркнуть это, А. Лавуазье в 1779 г. назвал этот газ «рождающим кислоты», или сокращенно — кислородом.
Озон
Кроме кислорода, существует еще одно простое вещество, молекулы которого состоят только из атомов кислорода. Это озон, молекула которого содержит три атома кислорода (рис. 74), его формула — О3.
При нормальных условиях озон представляет собой газ с резким раздражающим запахом. Он очень токсичен для всех живых организмов и поэтому используется вместо хлора для обеззараживания воды.
Небольшие количества озона образуются в воздухе во время грозы, а также в результате взаимодействия смолы хвойных деревьев с кислородом. Озон оказывает губительное действие на бактерии, поэтому лесной воздух (особенно в хвойных лесах) обладает целебным действием.
В небольших количествах озон образуется также при работе копировальных аппаратов и лазерных принтеров. Использовать такие приборы следует только в хорошо проветриваемых помещениях.
В верхних слоях атмосферы Земли (на высоте примерно 30—40 км) существует озоновый слой. Содержащийся в нем озон образуется из кислорода под воздействием солнечного излучения. Некоторые компоненты этого излучения губительны для живых организмов и растений на нашей планете, а озоновый слой поглощает их. Если бы не было озонового слоя, то жизнь на Земле постепенно бы прекратилась.
Многие ученые считают, что вещества, образующиеся в процессе производственной деятельности человека, разрушают озоновый слой. Это прежде всего фреоны — соединения, использующиеся в холодильных установках и дезодорантах, выбросы реактивных самолетов и ракет. Попадая в озоновый слой, эти вещества приводят к уменьшению его толщины или даже разрыву этого слоя — образованию так называемых озоновых дыр. В результате образования и увеличения размеров озоновых дыр могут наступить серьезные экологические катастрофы.
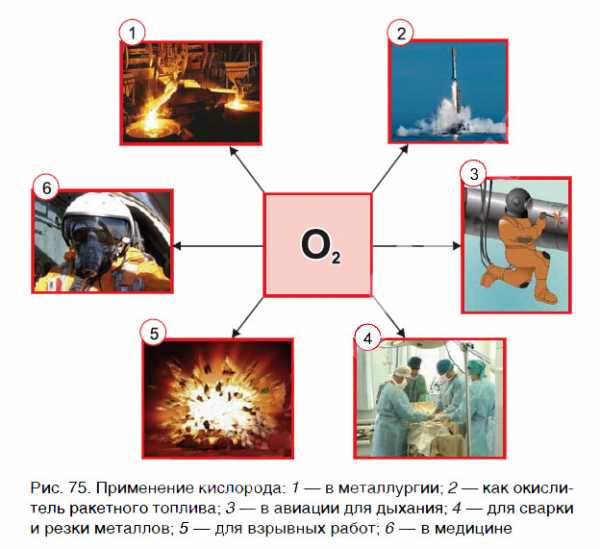
Применение кислорода
Кислород очень широко применяется в народном хозяйстве. На рисунке 75 приведены основные области применения кислорода. Главными потребителями кислорода являются металлургическая промышленность (выплавка стали), космическая техника (окислитель ракетного топлива), процессы обработки металлов (сварка и резка металлов).
Краткие выводы урока:
- Химический элемент кислород образует два простых вещества — кислород О2 и озон О3.
- Когда говорят о кислороде как о химическом элементе, подразумевают атомы кислорода О.
- Когда говорят о кислороде как о простом веществе, подразумевают вещество, состоящее из молекул и имеющее формулу О2.
Надеюсь урок 16 «Кислород и озон» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Ассоциация Российских Озонотерапевтов » Общие сведения о медицинском озоне
ОЗОН (О3) — аллотропная модификация кислорода, его молекула состоит из трех атомов кислорода и может существовать во всех трех агрегатных состояниях. Молекула озона имеет угловую структуру в форме равнобедренного треугольника с вершиной 127 o. Однако замкнутого треугольника не образуется, а молекула имеет строение цепи из 3-х атомов кислорода с расстоянием между ними 0,224 нм. В соответствии с этой молекулярной структурой дипольный момент составляет 0,55 дебай. В электронной структуре молекулы озона имеются 18 электронов, которые образуют мезомерностабильную систему, существующую в различных пограничных состояниях. Пограничные ионные структуры отражают дипольный характер молекулы озона и объясняют его специфическое реакционное поведение в сравнении с кислородом, который образует радикал с двумя неспаренными электронами. Молекула озона состоит из трех атомов кислорода. Химическая формула этого газа– O3 Реакция образования озона: 3O2 + 68 ккал/моль (285 кДж/моль) ⇄ 2O3 Молекулярная масса озона – 48 При комнатной температуре озон — это бесцветный газ с характерным запахом. Запах озона чувствуется при концентрации 10Химические свойства озона
Молекула озона неустойчива и при достаточных концентрациях в воздухе при нормальных условиях самопроизвольно превращается в двухатомный кислород с выделением тепла. Повышение температуры и понижение давления увеличивают скорость разложения озона. Контакт озона даже с малыми количествами органических веществ, некоторых металлов или их окислов резко ускоряет превращение. Химическая активность озона очень велика, это мощный окислитель. Он окисляет почти все металлы (за исключением золота, платины и иридия) и многие неметаллы. Продуктом реакции в основном является кислород. Озон растворяется в воде лучше, чем кислород, образуя нестойкие растворы, причём скорость его разложения в растворе в 5 -8 раз выше, чем в газовой фазе, чем в газовой фазе (Разумовский С.Д., 1990). Это обусловлено, по-видимому, не спецификой конденсированной фазы, а его реакциями с примесями и ионом гидроксила, поскольку скорость распада очень чувствительна к содержанию примесей и рН. Растворимость озона в растворах хлорида натрия подчиняется закону Генри. С увеличением концентрации NaCl в водном растворе растворимость озона уменьшается (Тарунина В.Н. и соавт.,1983). Озон имеет очень высокое сродство к электрону (1,9 эВ ), что и обуславливает его свойства сильного окислителя, превосходимого только фтором (Разумовский С.Д., 1990).Биологические свойства озона и его влияние на организм человека
Высокая окисляющая способность и то, что во многих химических реакциях, протекающих с участием озона, образуются свободные радикалы кислорода, делают этот газ крайне опасным для человека.- Раздражает и повреждает ткани органов дыхания;
- Воздействует на холестерин в крови человека, образуя нерастворимые формы, что приводит к атеросклерозу;
- Долгое нахождение в среде с повышенной концентрацией озона может стать причиной мужского бесплодия.
- Максимальная разовая предельно допустимая концентрация (ПДК м.р.) в атмосферном воздухе населённых мест 0,16 мг/м3
- Среднесуточная предельно допустимая концентрация (ПДК с.с.) – 0,03 мг/м3
- Предельно допустимая концентрация (ПДК) в воздухе рабочей зоны – 0,1 мг/м3 (при этом, порог человеческого обоняния приближённо равен 0,01 мг/м3).
Вредные и полезные свойства озона
Озон присутствует в двух слоях атмосферы. Тропосферный или приземный озон, находящийся в ближайшем к поверхности Земли слое атмосферы—в тропосфере – опасен. Он вреден и для человека, и для других живых организмов. Он губительно воздействует на деревья, посевы сельскохозяйственных культур. Кроме того, тропосферный озон—один из главных „ингредиентов“ городского смога. В тоже время стратосферный озон очень полезен. Разрушение образованного им озонового слоя (озонового экрана) приводит к тому, что поток ультрафиолетового излучения на земную поверхность увеличивается. Из-за этого возрастает количество заболеваний раком кожи (в том числе наиболее опасного его вида—меланомы), случаев катаракты. Воздействие жесткого ультрафиолета ослабляет иммунитет. Избыточное УФ-излучение может также стать проблемой для сельского хозяйства, так как посевы некоторых культур чрезвычайно чувствительны к ультрафиолету. В то же время следует помнить, что озон – ядовитый газ, и на уровне земной поверхности он является вредоносным загрязнителем. Летом из-за интенсивного солнечного излучения и жары в воздухе образуется особенно много вредоносного озона.Взаимодействие озона и кислорода друг с другом. Сходства и различия.
Озон – аллотропная форма кислорода. Аллотропия – существование одного и того же химического элемента в виде двух и более простых веществ. В данном случае и озон (O3) и кислород (OРастворимость озона и его стабильность в водных растворах
Скорость разложения озона в растворе в 5-8 раз выше, чем в газовой фазе. Растворимость озона в воде в 10 раз выше, чем кислорода. По данным разных авторов величина коэффициента растворимости озона в воде колеблется от 0,49 до 0,64 мл озона/ мл воды. В идеальных термодинамических условиях равновесие подчиняется закону Генри, т.е. концентрация насыщенного раствора газа пропорциональна его парциальному давлению. CРаспад озона и период полураспада (т 1/2)
В водной среде распад озона сильно зависит от качества воды, температуры и рН среды. Повышение рН среды ускоряет распад озона и снижает при этом концентрацию озона в воде. Аналогичные процессы происходят при повышении температуры. Период полураспада озона в бидистиллированной воде составляет 10 часов, в деминерализованной воде — 80 минут; в дистиллированной воде — 120 минут. Известно, что разложение озона в воде является сложным процессом реакций радикальных цепей: Максимальное количество озона в водном образце наблюдается в течение 8-15 минут. Через 1 час в растворе отмечаются только свободные радикалы кислорода. Среди них важнейшим является гидроксильный радикал (ОН’) (Staehelin G., 1985), и это необходимо принимать во внимание при использовании озонированной воды в терапевтических целях. Поскольку в клинической практике находят применение озонированная вода и озонированный физиологический раствор, нами проведена оценка этих озонированных жидкостей в зависимости от концентраций, используемых в отечественной медицине. Основными методами анализа явились йодометрическое титрование и интенсивность хемилюминесценции с использованием прибора биохемилюминометра БХЛ-06 (производство Нижний Новгород) (Конторщикова К. Н., Перетягин С. П., Иванова И. П. 1995). Явление хемилюминесценции связано с реакциями рекомбинации свободных радикалов, образующихся при разложении озона в воде. При обработке 500 мл би- или дистиллированной воды барботированием озоно-кислородной газовой смесью с концентрацией озона в пределах 1000-1500 мкг/л и скоростью потока газа 1 л/мин в течение 20 минут хемилюминесценция выявляется в течение 160 минут. Причем в бидистиллированной воде интенсивность свечения существенно выше, чем в дистиллированной, что объясняется наличием примесей, гасящих свечение. Растворимость озона в растворах NaCl подчиняется закону Генри, т.е. уменьшается с увеличением концентрации солей. Физиологический раствор обрабатывали озоном с концентрацией 400, 800 и 1000 мкг/л в течение 15 минут. Общая интенсивность свечения (в mv) увеличивалась с ростом концентрации озона. Продолжительность свечения составляет 20 минут. Это объясняется более быстрой рекомбинацией свободных радикалов и отсюда гашением свечения за счет наличия в физиологическом растворе примесей. Несмотря на высокий окислительный потенциал, озон обладает высокой селективностью, которая обусловлена полярным строением молекулы. Мгновенно реагируют с озоном соединения, содержащие свободные двойные связи (-С=С-). В результате чувствительными к действию озона являются ненасыщенные жирные кислоты, ароматические аминокислоты и пептиды, прежде всего содержащие SH- группы. Согласно данным Криге (1953) (цит. По Vieban R. 1994), первичным продуктом взаимодействия молекулы озона с биоорганическими субстратами является 1-3 диполярная молекула. Эта реакция является основной при взаимодействии озона с органическими субстратами при рН 0С и затем превращается в первичный озонид (молозонид) 1,2,3-триоксалан. Другое возможное направление реакции — образование эпоксидных соединений. Первичный озонид нестабилен и распадается с образованием карбоксильного соединения и карбонилоксида. В результате взаимодействия карбонилоксида с карбонильным соединением образуется биполярный ион , который затем превращается во вторичный озонид 1,2,3 — триоксалан. Последний при восстановлении распадается с образованием смеси 2-х карбонильных соединений, с дальнейшим образованием пероксида (I) и озонида (II). Озонирование ароматических соединений протекает с образованием полимерных озонидов. Присоединение озона нарушает ароматическое сопряжение в ядре и требует затрат энергии, поэтому скорость озонирования гомологов коррелирует с энергией сопряжения. Озонирование насушенных углеводородов связано с механизмом внедрения. Озонирование серо- и азотосодержащих органических соединений протекает следующим образом: Озониды обычно плохо растворимы в воде, но хорошо в органических растворителях. При нагревании, действии переходных металлов распадаются на радикалы. Количество озонидов в органическом соединении определяется йодным числом. Йодное число — масса йода в граммах, присоединяющееся к 100 г органического вещества. В норме для жирных кислот йодное число составляет 100-400, для твердых жиров 35-85, для жидких жиров — 150-200. Впервые озон, как антисептическое средство был опробован A. Wolff еще в 1915 во время первой мировой войны. Последующие годы постепенно накапливалась информация об успешном применении озона при лечении различных заболеваний. Однако длительное время использовались лишь методы озонотерапии, связанные с прямыми контактами озона с наружными поверхностями и различными полостями тела. Интерес к озонотерапии усиливался по мере накопления данных о биологическом действии озона на организм и появления сообщений из различных клиник мира об успешном использовании озона при лечении целого ряда заболеваний. История медицинского применения озона начинается с XIX века. Пионерами клинического применения озона были западные ученые Америки и Европы, в частности, C. J. Kenworthy, B. Lust, I. Aberhart, Е. Payer, E. A. Fisch, Н. Н. Wolff и другие. В России о лечебном применении озона было известно мало. Только в 60-70 годы в отечественной литературе появилось несколько работ по ингаляционной озонотерапии и по применению озона в лечении некоторых кожных заболеваний, а с 80-х годов в нашей стране этот метод стал интенсивно разрабатываться и получать более широкое распространение. Основы для фундаментальных разработок технологий озонотерапии были во многом определены работами Института химической физики АМН СССР. Книга «Озон и его реакции с органическими веществами» (С. Д. Разумовский, Г. Е. Зайков, Москва, 1974 г.) явилась отправной точкой для обоснования механизмов лечебного действия озона у многих разработчиков. В мире широко действует Международная озоновая ассоциация (IOA), которая провела 20 международных конгрессов, а с 1991 года в работе этих конгрессов принимают участие и наши врачи и ученые. Совершенно по-новому сегодня рассматриваются проблемы прикладного использования озона, а именно в медицине. В терапевтическом диапазоне концентраций и доз озон проявляет свойства мощного биорегулятора, средства, способного во многом усилить методы традиционной медицины, а зачастую выступать в качестве средства монотерапии. Применение медицинского озона представляет качественно новое решение актуальных проблем лечения многих заболеваний. Технологии озонотерапии используются в хирургии, акушерстве и гинекологии, стоматологии, неврологии, при терапевтической патологии, инфекционных болезнях, дерматологии и венерических болезнях и целом ряде других заболеваний. Для озонотерапии характерна простота исполнения, высокая эффективность, хорошая переносимость, практическое отсутствие побочных действий, она экономически выгодна. Лечебные свойства озона при заболеваниях различной этиологии основаны на его уникальной способности воздействовать на организм. Озон в терапевтических дозах действует как иммуномодулирующее, противовоспалительное, бактерицидное, противовирусное, фунгицидное, цитостатическое, антистрессовое и аналгезирующее средство. Его способность активно коррегировать нарушенный кислородный гомеостаз организма открывает большие перспективы для восстановительной медицины. Широкий спектр методических возможностей позволяет с большой эффективностью использовать лечебные свойства озона для местной и системной терапии. В последние десятилетия на передний план вышли методы, связанные с парентеральным (внутривенным, внутримышечным, внутрисуставным, подкожным) введением терапевтических доз озона, лечебный эффект которых связан, в основном, с активизацией различных систем жизнедеятельности организма. Кислородно-озоновая газовая смесь при высоких (4000 — 8000 мкг/л) концентрациях в ней озона в эффективна при обработке сильно инфицированных, плохо заживающих ран, гангрене, пролежней, ожогов, грибковых поражениях кожи и т.п. Озон в высоких концентрациях можно также использовать как кровоостанавливающее средство. Низкие концентрации озона стимулируют репарацию, способствуют эпителизации и заживлению. В лечении колитов, проктитов, свищей и ряда других заболеваний кишечника используют ректальное введение кислородно-озоновой газовой смеси. Озон, растворенный в физиологическом растворе, успешно применяют при перитоните для санации брюшной полости, а озонированную дистиллированную воду в челюстной хирургии и др. Для внутривенного введения используется озон, растворенный в физиологическом растворе или в крови больного. Пионерами Европейской школы было высказано постулирующее положение о том, что главной целью озонотерапии является: «Стимуляция и реактивация кислородного метаболизма без нарушения окислительно-восстановительных систем»,- это значит, что при расчете дозировок на сеанс или курс, озонотерапевтическое воздействие должно находиться в пределах, в которых ферментативно выравниваются радикальные кислородные метаболиты или избыточно полученный пероксид» (З. Риллинг, Р. Фибан 1996 в кн. Практика озонотерапии). В зарубежной медицинской практике для парентерального введения озона используются, в основном, большая и малая аутогемотерапии. При проведении большой аутогемотерапии, взятая у пациента кровь тщательно смешивается с определенным объемом кислородно-озоновой газовой смеси, и сразу же капельно вводится обратно в вену того же пациента. При малой аутогемотерапии озонированная кровь вводится внутримышечно. Терапевтическая доза озона в этом случае выдерживается за счет фиксированных объемов газа и концентрации озона в нем.Научные достижения отечественных учёных стали регулярно докладываться на международных конгрессах и симпозиумах
- 1991 г. – Куба, Гавана,
- 1993 г. – США Сан-Франциско,
- 1995 г. – ФранцияЛилль,
- 1997 г. – Япония, Киото,
- 1998 г. – Австрия, Зальцбург,
- 1999г . – Германия,Баден-Баден,
- 2001 г. – Англия, Лондон,
- 2005 г. – Франция,Страсбург,
- 2009 г. – Япония, Киото,
- 2010 г. — Испания, Мадрид
- 2011 г .Турция(Стамбул),Франция (Париж),Мексика(Канкун)
- 2012г. – Испания, Мадрид
Всероссийские научно-практические конференции с Международным участием по озонотерапии
I – «ОЗОН В БИОЛОГИИ И МЕДИЦИНЕ» – 1992 г., Н.Новгород II – «ОЗОН В БИОЛОГИИ И МЕДИЦИНЕ» – 1995 г., Н.Новгород III – «ОЗОН И МЕТОДЫ ЭФФЕРЕНТНОЙ ТЕРАПИИ» – 1998 г., Н.Новгород IV – «ОЗОН И МЕТОДЫ ЭФФЕРЕНТНОЙ ТЕРАПИИ» – 2000 г., Н.Новгород V – «ОЗОН В БИОЛОГИИ И МЕДИЦИНЕ» – 2003 г., Н.Новгород VI – «ОЗОН В БИОЛОГИИ И МЕДИЦИНЕ» – 2005 г., Н.Новгород «I Конференция по озонотерапии Азиатско-Европейского союза озонотерапевтов и производителей медоборудования»– 2006 г., Большое Болдино, Нижегородская область VII – «ОЗОН В БИОЛОГИИ И МЕДИЦИНЕ» – 2007 г., Н.Новгород У111 – «Озон, активные формы кислорода и методы интенсивной терапии в медицине» — 2009, г.Н.Новгород К 2000 г. Российская школа озонотерапии окончательно сформировала свой, отличающийся от Европейского, подход к применению озона как лечебного средства. Главные отличия — широкое использование физиологического раствора в качестве носителя озона, применение значительно более низких концентраций и доз озона, разработанные технологии экстракорпоральной обработки больших объёмов крови (озонированное искусственное кровообращение), индивидуальный выбор доз и концентраций озона при системной озонотерапии. В стремлении большинства российских врачей использовать наименьшие из эффективных концентраций озона нашел отражение основной принцип медицины — «не навреди». Безопасность и эффективность Российских методик озонотерапии многократно обоснована и доказана применительно к различным областям медицины. В результате многолетних фундаментально-клинических исследований нижегородскими учёными была «Установлена неизвестная закономерность формирования адаптационных механизмов организма млекопитающих при системном воздействии низкими терапевтическими дозами озона, заключающаяся в том, что пусковым механизмом является влияние озона на про- и антиоксидантный баланс организма и обусловленная умеренной интенсификацией свободно-радикальных реакций, что, в свою очередь, увеличивает активность ферментативного и неферментативного звеньев антиоксидантной системы защиты» (Конторщикова К. Н., Перетягин С. П.), на которую авторы получили открытие (Диплом № 309 от 16 мая 2006 г.). В работах отечественных учёных нашли развитие новые технологии и аспекты использования озона с лечебными целями:- Широкое использование в качестве носителя растворенного озона физиологического раствора (0,9% раствор NaCl)
- Применение сравнительно малых концентраций и доз озона при системном воздействии (внутрисосудистое и внутрикишечное введение)
- Внутрикостные вливания озонированных растворов
- Внутрикоронарное введение озонированных кардиоплегических растворов
- Тотальная экстракорпоральная обработка озоном больших объемов крови при искусственном кровообращении
- Низкопоточная озонокислородная терапия
- Внутрипортальное введение озонированных растворов
- Применение озона на театре военных действий
- Сопровождение системной озонотерапии методами биохимического контроля
- Озонотерапия — немедикаментозный метод лечебного воздействия, позволяющий получать положительные результаты при патологии различного генеза.
- Биологическое действие парентерально введенного озона проявляется на уровне низких концентраций и доз, что сопровождается клинически выраженными позитивными лечебными эффектами, имеющими четко выраженную дозозависимость.
- Опыт Российской и Европейской школ озонотерапии свидетельствует о том, что использование озона в качестве лечебного средства значительно повышает эффективность лекарственной терапии, позволяет в ряде случаев заменить или уменьшить фармакологическую нагрузку на пациента. На фоне озонотерапии восстанавливаются собственные кислородзависимые реакции и процессы больного организма.
- Технические возможности современных медицинских озонаторов, обладающих возможностями сверхточной дозировки, позволяют применять озон в диапазоне низких терапевтических концентраций аналогично общепринятым фармакологическим средствам.
www.ozonetherapy.ru
