Урок по биологии на тему «Белки и нуклеиновые кислоты» (9 класс)
Разработка урока по теме «Белки и нуклеиновые кислоты»
(с использованием технологии критического мышления)
Место урока в системе школьных уроков:
Данный урок является третьим уроком раздела «Основы учения о клетке».
Тип урока: Урок сообщения новых знаний.
Форма урока: урок-исследование.
Цель урока:
— продолжить углубление и расширение знаний о химическом составе клетки, раскрыв состав и функции белков и нуклеиновых кислот;
— сформировать понятие о белках и нуклеиновых кислотах.
Задачи урока:
Обучающие:
— сформировать знания о структуре и функциях белков.
— сформировать знания о структуре и видах нуклеиновых кислот.
Развивающие:
— формировать умения и навыки при решении задач на принцип комплементарности, осуществлять репликацию ДНК; сравнивать ДНК и РНК; объяснять их значение в хранении и передаче наследственной информации.
— развивать у учащихся умение самостоятельно выделять главное при работе с текстом в изучаемом материале;
— анализировать и обобщать изучаемые факты, логически излагать мысли;
Воспитательные:
— продолжить формирование системы нравственных отношений у учащихся: уважительное отношение к мнению других учеников; чувство ответственности за проделанную работу в группе;
— воспитывать критическую и объективную самооценку знаний.
Оборудование:
— Компьютер
— учебники
— опорные таблицы
— текст по теме «Функции белков»
Содержание урока.
Организационный момент. Проверка домашнего задания.
Актуализация знаний по теме «Химический состав клетки».
Сообщение темы урока.
Мотивация и сообщение цели урока.
Основная часть
Рефлексия.
Этап подведения итогов.
Домашнее задание.
На уроке использованы такие методы, как
-словесный (в беседах)
-объяснительно-иллюстративный (на этапе изучения нового материала)
— частично – поисковый метод (в творческом задании)
— контроля и самоконтроля
В урок включены такие формы работы, как самостоятельная, парная, групповая и индивидуальная работа.
Задействованы на уроке наглядные, дидактические средства обучения.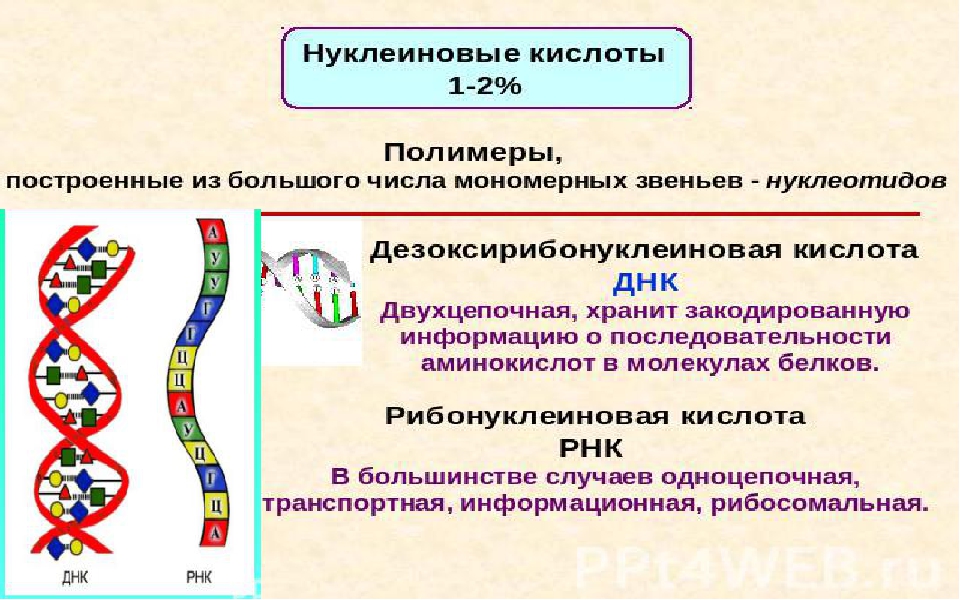
Содержание учебного материала и виды работы направлены на поддержание познавательной и мыслительной активности учащихся.
В результате работы на уроке была использована технология развития критического мышления. И применялись следующие приёмы:
«Кластер»
Таблица «Знаю – Хочу знать – Узнал»
«Сводная таблица»
«Фишбоун»
«Концептуальная таблица»
- «Незаконченное предложение»
«Синквейн»
Конечный или планируемый результат:
Результатом данного урока является изучение нового материала, актуализация знаний по теме «Химический состав клетки». Учащиеся должны усвоить основные особенности белков и нуклеиновых кислот.
Этап урока
Деятельность учителя
Деятельность учащихся
Психолого – педагогический комментарий
1. Организационный момент.
— Здравствуйте, ребята! Мы продолжаем изучать тему «Основы учения о клетке». На прошлом уроке мы говорили о химическом составе клетки. Узнали, какие вещества содержатся в клетке.
Слушают учителя. Психологически настраиваются на работу. На учебном столе у каждого ученика – учебник, тетрадь.
Создание доброжелательной психологической атмосферы в классе.
2. Актуализация знаний по теме «Химический состав клетки».
Стадия вызова.
— Прежде чем начать изучение нового материала, мы закрепим знания по изученной теме «Химический состав клетки». И наш урок я хочу начать с вопроса: «Какие вещества содержатся в клетке?» Давайте попробуем составить кластер по данной теме (Приложение 6) (Учитель на доске записывает ключевое слово «вещества клетки»)
— Проанализируем полученные вами кластеры.
(Учитель записывает на доске все идеи).
— Все молодцы, с заданием хорошо справились.
Дети записывают в тетради ключевое слово и вокруг него «накидывают» слова или предложения, выражающие идею по данной теме.
Зачитывают по одному свои варианты идей, и в ходе анализа каждый дополняет свой кластер.
Формирование мыслительной деятельности учащихся.
Создание ситуации заинтересованности.
Мотивация деятельности.
3.Сообщение темы урока.
Стадия вызова.
-Ребята, скажите, какие основные органические вещества содержатся в клетке?
-Молодцы! И сегодня мы исследуем клетку с точки зрения основных органических веществ. Тема нашего урока «Белки и нуклеиновые кислоты».
—Белки и нуклеиновые кислоты.
Записывают в тетрадь тему урока.
Создание ситуации заинтересованности, мотивации деятельности.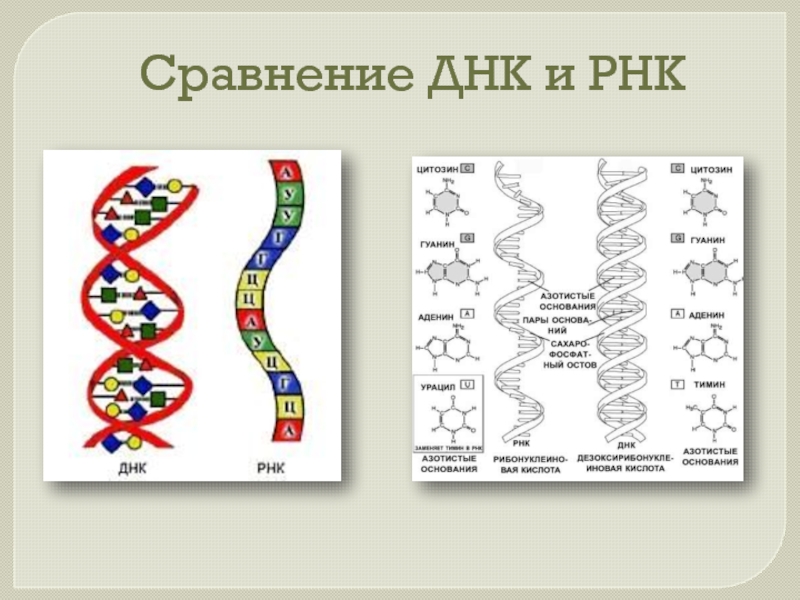
.
4.Мотивация.
— Перед тем, как начать изучать новую тему, мне хотелось бы узнать, что вы знаете об этом. И сейчас мы составим таблицу «Знаю – Хочу знать – Узнал» (приём «таблица «З-Х-У»)
(Приложение 7).
— Давайте попробуем сформулировать цель урока.
— Сформулируйте тезис, который мы будем доказывать?
Дети самостоятельно заполняют в таблице «З – Х – У» первый и второй столбец, то что знают про белки и нуклеиновые кислоты. И что хотят узнать.
-Изучить понятия «белки и нуклеиновые кислоты»
— Белки и нуклеиновые кислоты играют важную роль в клетке.
Создание ситуации заинтересованности, мотивации деятельности.
Формирование умения ставить цель, прогнозировать свою деятельность
5.Основная часть
— Начнём изучение нового материала с того, что дадим определение «белкам»?
Белки – это сложные высокомолекулярные органические соединения, играющие главную роль в процессе жизнедеятельности всех живых организмов.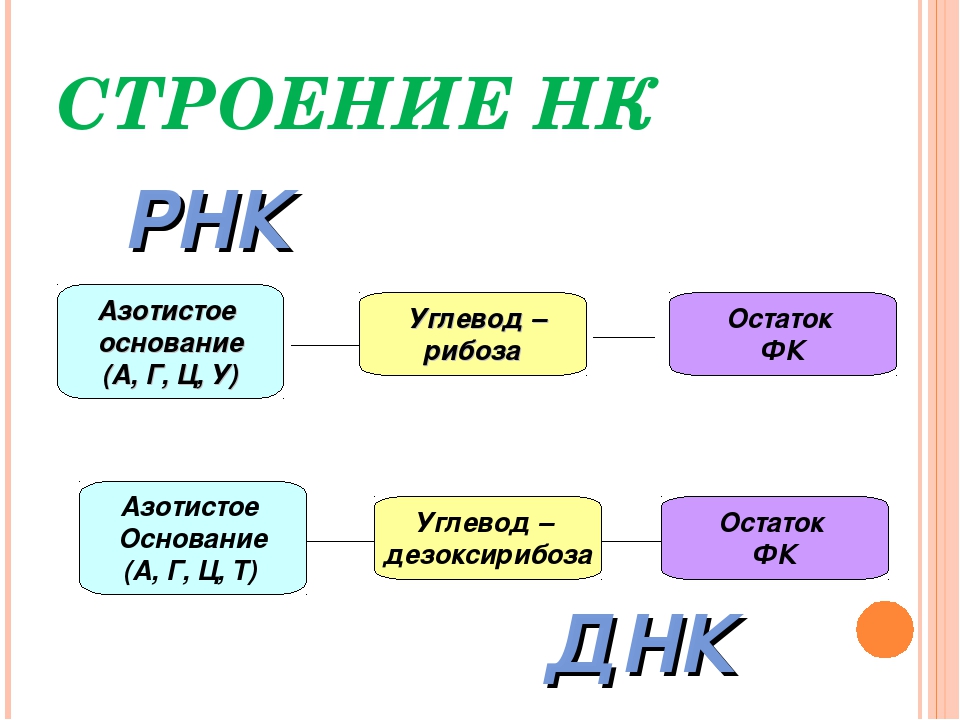
Белки — это полимеры, мономерами которых являются аминокислоты, т.е. белки состоят из аминокислот, которые соединяются друг с другом химической связью (пептидной), образуя структуры белков.
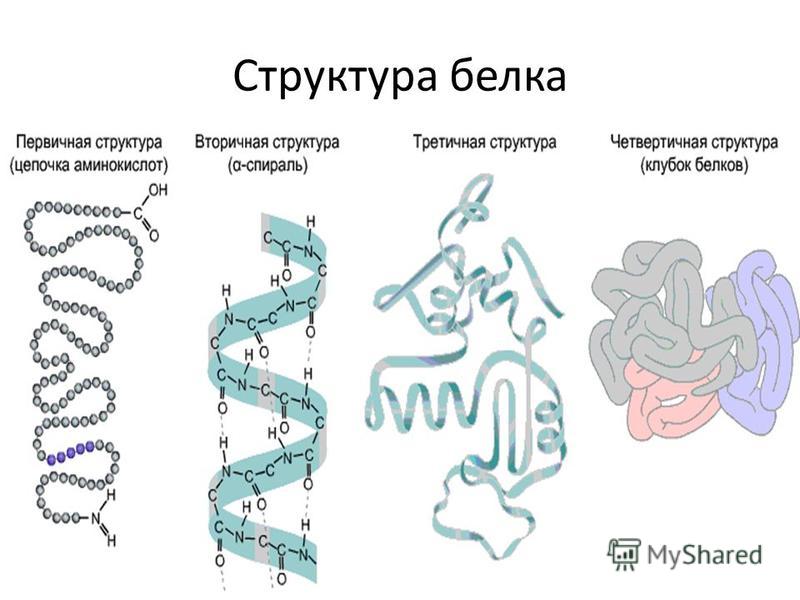
Существует четыре структуры белков.
— Попробуйте самостоятельно в парах разобраться по данному вопросу с помощью «Сводной таблицы» (Приложение 8), соотнесите рисунок с его характеристикой.
Учитель правильный вариант соотнесений выводит на экран (Приложение 9).
— Сейчас рассмотрим, какие функции выполняют белки в клетке. Для этого мы поработаем с текстом, с помощью которого вы должны заполнить «скелет рыбной кости». Голова — функции белков, «верхние косточки» — название функции, «нижние косточки» — ее суть, хвост – вывод (
— Давайте посмотрим, что у вас получилось!
— Теперь познакомимся с понятием «нуклеиновые кислоты». Запишем в тетрадь определение.
Нуклеиновые кислоты – это природные высокомолекулярные органические соединения, которые обеспечивают хранение и передачу наследственной информации в живых организмах.
Нуклеиновые кислоты – это полимер, мономерами которых являются нуклеотиды.
— В данном определении есть незнакомые слова?
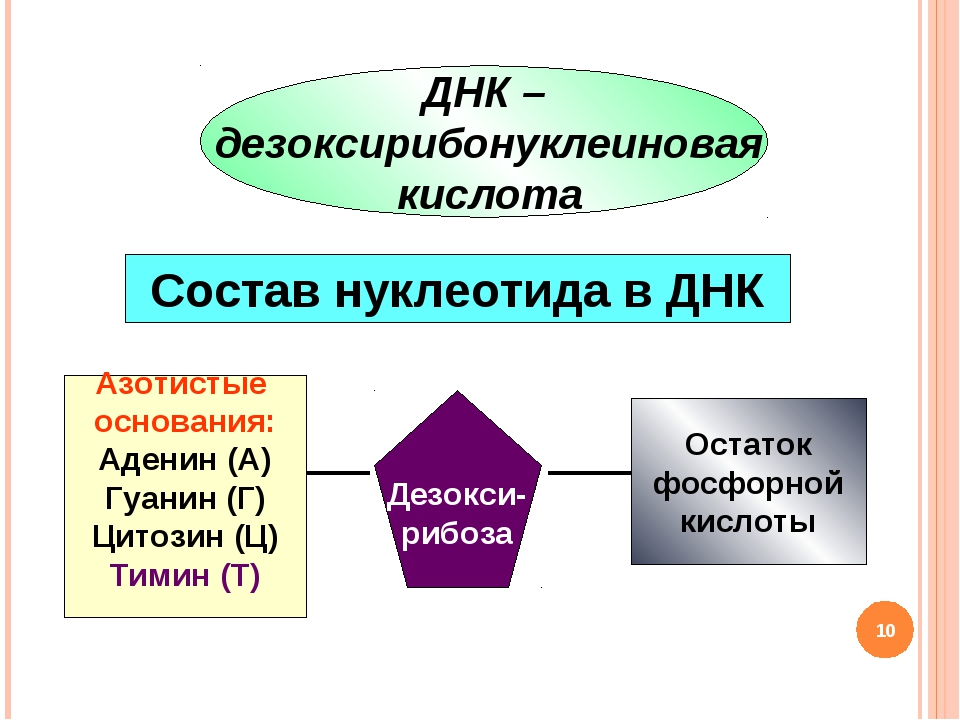
Нуклеотиды – это сложные соединения, которые состоят из 3-х компонентов: азотистого основания, углевода и остатка фосфорной кислоты.
Учитель объясняет строение нуклеотида с помощью таблицы.
Существует два вида нуклеиновых кислот: ДНК и РНК.
Что же такое ДНК?
ДНК – это полинуклеотид, который состоит из 4-х нуклеотидов: А, Г, Ц, Т.
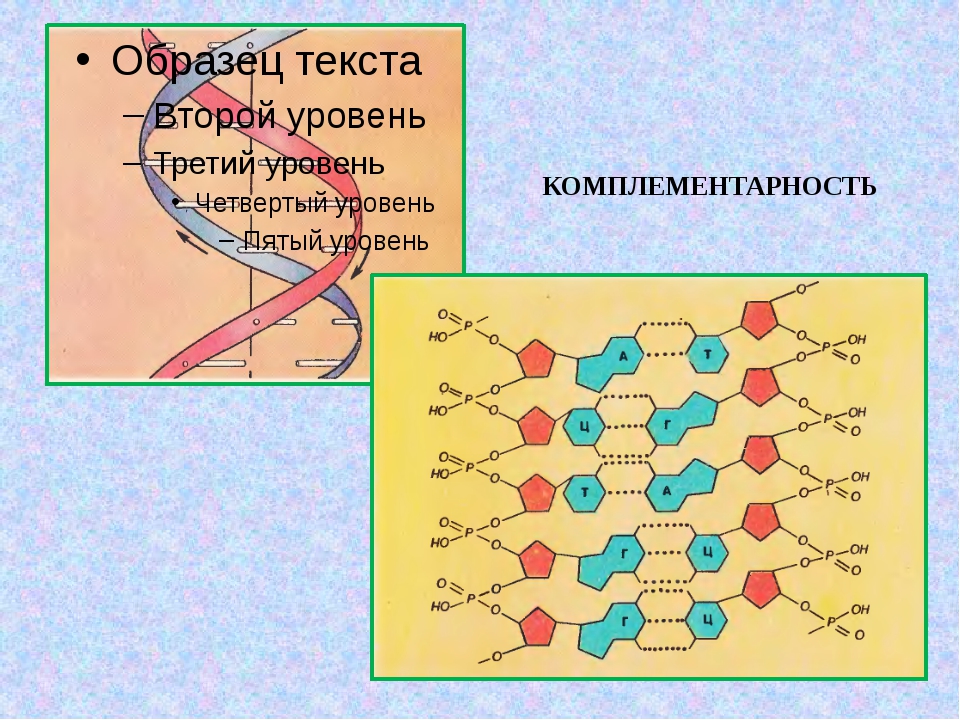
ДНК – двойная цепочка, соединенная по принципу комплементарности (А-Т, Г- Ц).
— Давайте потренируемся и решим задачу на данный принцип.
Условие: необходимо достроит вторую цепочку ДНК.
Каждый ряд – команда, получает лист с фрагментом одной цепи ДНК, который передается по цепочке.
1 команда: Т-Ц-Г-Т-А-Ц-А-Г-А-Г-Т-Ц
2 команда: А-Г-Ц-А-Т-Г-Т-Ц-Т-Ц-А-Г
— Проверим.
— Молодцы!
— А сейчас вы поработаете самостоятельно по заполнению «Концептуальной таблицы» на тему «Сравнение ДНК с РНК» с помощью текста учебника на стр.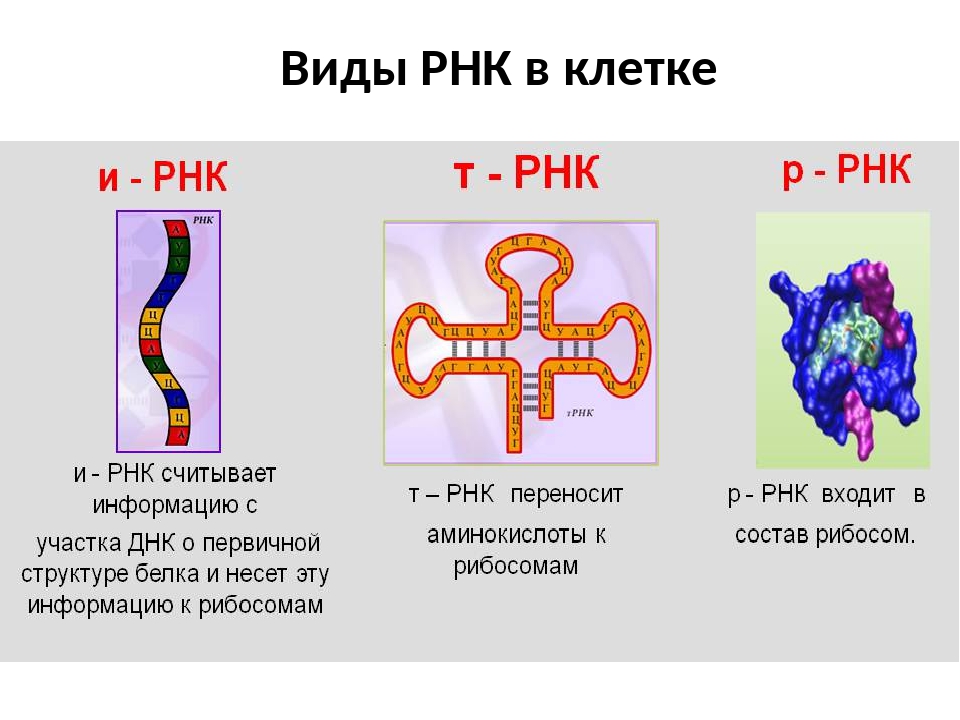 22-23. У вас на партах лежат таблицы с критериями сравнения. Вам нужно сравнить ДНК с РНК. (Приложение 12).
22-23. У вас на партах лежат таблицы с критериями сравнения. Вам нужно сравнить ДНК с РНК. (Приложение 12).
— Итак, таблица составлена, проверим.
— Молодцы! Хорошо поработали.
Дети записывают определение в тетрадь.
Рассматривают таблицу и соотносят соответствующий рисунок структуры белка с его характеристикой.
Учащиеся сравнивают и исправляют ошибки, если таковые есть.
Читают текст, заполняют «рыбку».
Дети отвечают.
Структурная – входит в состав клеточных структур;
Каталитическая – все процессы в клетке протекают при участии ферментов – катализаторов;
Транспортная – белки — переносчики;
Защитная – белки – антитела;
Двигательная – сократительные белки, участвующие во всех движениях;
Энергетическая – белки – источники – энергии.

Дети записывают определение в тетрадь.
— Да, нуклеотиды.
Дети слушают объяснения учителя и записывают определение в тетрадь.
Дети слушают объяснения учителя.
Дети каждой команды дописывают вторую цепочку ДНК.
В индивидуальном порядке дети заполняют таблицу с помощью текста учебника.
Проверяют правильный ответ.
Активация познавательной и мыслительной деятельности.
Умение прислушиваться к мнению других, развитие мышления.
Активация познавательной и мыслительной деятельности, умение работать с текстом, обобщать и выбирать главное.
Развитие коммуникативных способностей.
Активизация познавательной деятельности учащихся.
Активизация познавательной деятельности учащихся. Умение работать в группе.
Умение работать в группе.
Развитие логического мышления.
Умение работать с текстом, обобщать, делать выводы.
6.Рефлексия. Подведение итогов.
— Сегодня на уроке мы рассмотрели основные особенности важных органических веществ – это белков и нуклеиновых кислот.
— В начале урока вы заполнили в таблице «З-Х-У» первые два столбца, а сейчас самостоятельно заполните третий столбик «Узнал» (приложение 7).
Сейчас я предлагаю вам выполнить задание по пройденной теме «Незаконченное предложение» (Приложение 13).
— Данный урок мне хочется закончить фразой, которую вы должны продолжить («Сегодня на уроке мне удалось……»).
Дети заполняют таблицу.
Взаимопроверка (приводятся аргументы к тезису).
Дети индивидуально выполняют задание.
Самопроверка, выставление оценок.
Ученики активно продолжают фразу.
Использование аналитико-синтетического метода: умение сравнивать, обобщать, делать выводы.
Формирование навыков самоконтроля и самооценки.
7.Этап подведения итогов урока.
В ходе урока хочется отметить четкую и слаженную работу. Вы показали достаточно высокий уровень самостоятельной работы.
(Выставление оценок).
Выставление оценок в дневник учащихся
Создание ситуации успеха при подведении итогов урока.
8. Домашнее задание.
Домашнее задание:
— §6
— составить синквейн (приложение 14) по теме «Белки и нуклеиновые кислоты»
В дневники записывают домашнее задание.
Конспект урока «Белки и нуклеиновые кислоты» по биологии для 9 класса
Ученик: _____________________________________
Дата: «_____» _____________ 20 __ г.
Биология, 9 класс
Контрольная работа по теме
«Белки и нуклеиновые кислоты»
Часть 1.
Заполните пропуски в предложениях.
Потерю своих качеств и частичное изменение _________________ белковой молекулы называют _____________________
Этот процесс обратим в тех случаях, когда затронута только вторичная
____________________ или ___________________________________
В основе строения молекул ДНК лежит принцип комплементарности. Используя предложенный фрагмент одной цепи ДНК, постройте другую цепь: А–Т–Г–Г–Ц–Г–А–А: ___ – ___ – ___ – ___ – ___ – ___ – ___ – ___ –
Часть 2. Выберите, к каким структурам относятся данные высказывания.
1. Длинная нить последовательно соединенных аминокислот –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
2. В состав входят основания АУЦГ:
В состав входят основания АУЦГ:
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
3.Их мономерами являются аминокислоты:
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
4. Присуща не всем видам белков:
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
5. Имеет вид двойной спирали –
Имеет вид двойной спирали –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
6. Одна из их основных функций – каталитическая –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
7. В состав входит рибоза –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
8. В состав входят основания: АТГЦ
В состав входят основания: АТГЦ
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
9. Несут наследственную информацию –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
10. Их мономерами являются нуклеотиды
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
11. Подвергаются денатурации –
Подвергаются денатурации –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
12. Образует глобулу –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
13. Впервые были обнаружены в ядре –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
14. В состав входит дезоксирибоза –
В состав входит дезоксирибоза –
белки
нуклеиновые кислоты
первичная структура белка
вторичная структура белка
третичная структура белка
четвертичная структура белка
ДНК
РНК
Здесь представлен конспект к уроку на тему «Белки и нуклеиновые кислоты», который Вы можете бесплатно скачать на нашем сайте. Предмет конспекта: Биология (9 класс). Также здесь Вы можете найти дополнительные учебные материалы и презентации по данной теме, используя которые, Вы сможете еще больше заинтересовать аудиторию и преподнести еще больше полезной информации.
Нуклеиновые кислоты: строение и функции
Вы задумывались когда-либо о самом существе жизни? Может быть, приходилось отвечать на вопрос – что такое жизнь? А сами его когда-нибудь задавали?
Возможно,
это было на первых уроках биологии в девятом классе. А представьте – завтра или
уже сегодня после обеда вы встретите инопланетянина и возникнет необходимость
раскрыть перед ним саму суть существования жизни на Земле. Каким будет ваш
ответ?
А представьте – завтра или
уже сегодня после обеда вы встретите инопланетянина и возникнет необходимость
раскрыть перед ним саму суть существования жизни на Земле. Каким будет ваш
ответ?
Попробуем обратиться к истории.
Во второй половине XIX века Фридрих Энгельс, как вы знаете, отдавал предпочтение белкам. Как главным составляющим и непосредственным исполнителям, если так можно выразиться, жизни.
А в середине XX века американский физик Франк Типлер высказывал мнение, что жизнь является всего лишь информацией особого рода: «Я определяю жизнь как некую закодированную информацию, которая сохраняется естественным отбором». Трудно не согласиться с его попыткой выделить из всех критериев жизни в качестве главного способность живых организмов сохранять и передавать информацию.
Скорее всего, согласится с таким мнением и встретившийся вам инопланетянин. Но тогда у него непременно возникнет следующий вопрос – как вы это делаете?
Отвечаем прямо сейчас. На этом уроке.
На этом уроке.
Мы преодолели все предыдущие ступеньки лестницы органических веществ и полностью заслужили право узнать подробнее о самой таинственной и важной молекуле жизни на Земле – молекуле ДНК.
Точно так все ступеньки этой лестницы преодолевало и всё человечество. И именно наверху, в последнюю очередь, пытливому людскому разуму покорилась ДНК.
Это произошло в 1953 году стараниями всё тех же американцев: Джеймса Уотсона и Фрэнсиса Крика.
Джеймс Уотсон
Фрэнсис Крик
Кстати, в тесном сотрудничестве с известными Максом Перуцем и Джоном Кендрю, впервые открывшим структуры белка.
В 1962 году, пожалуй, наиважнейшее
открытие в истории биологии заслуженно было отмечено Нобелевской премией.
Которая была присуждена за открытие строения всего одной молекулы из многих
миллионов. Но именно той, которую природа на Земле назначила носителем наследственной информации всех живых организмов.
Если быть уж совсем справедливыми, то нуклеиновые кислоты были известны задолго до открытия строения ДНК.
В 1869 году они были открыты швейцарским биохимиком Фридрихом Мишером. Неизвестное в то время соединение было выделено из ядер лейкоцитов человека и сперматозоидов лосося и было названо нуклеин (от латинского nucleus – ядро). Но позднее были выявлены кислотные свойства нуклеина, и он получил своё современное название – нуклеиновая кислота.
Нуклеиновые кислоты оказались самыми огромными биологическими молекулами с молекулярной массой до нескольких миллионов. Можно с уверенностью утверждать, что такая огромная масса возможна только в том случае, если вещество является полимером. И это так на самом деле. Нуклеиновые кислоты (а это не только ДНК) – биополимеры. Мономерами нуклеиновых кислот являются нуклеотиды.
Если
ранее вы встречались с мономерами, представленными каким-либо одним веществом.
Помните? Глюкоза – мономер целлюлозы, аминокислоты (но они бывают 20 видов) –
мономеры белков. То мономеры нуклеиновых кислот состоят из остатков трёх
веществ: фосфорной кислоты, пятиуглеродного сахара (рибозы
или дезоксирибозы) и азотистого основания.
То мономеры нуклеиновых кислот состоят из остатков трёх
веществ: фосфорной кислоты, пятиуглеродного сахара (рибозы
или дезоксирибозы) и азотистого основания.
Но это ещё не всё. В состав нуклеотидов может входить пять различных азотистых оснований: аденин, гуанин, тимин, цитозин и урацил. По своему химическому строению они делятся на две группы: пуриновые и пиримидиновые. К пуриновым относятся аденин и гуанин, а к пиримидиновым – тимин, цитозин и урацил.
Таким образом, в зависимости от входящего в состав нуклеотидов азотистого основания, различают пять видов мономеров нуклеиновых кислот.
Адениловый, гуаниловый, тимидиловый, цитидиловый и урациловый нуклеотиды.
В
цепочки нуклеотиды соединяются через сахар. То есть пентоза одного нуклеотида –
остаток фосфорной кислоты другого – пентоза другого – остаток фосфорной кислоты
третьего и так далее.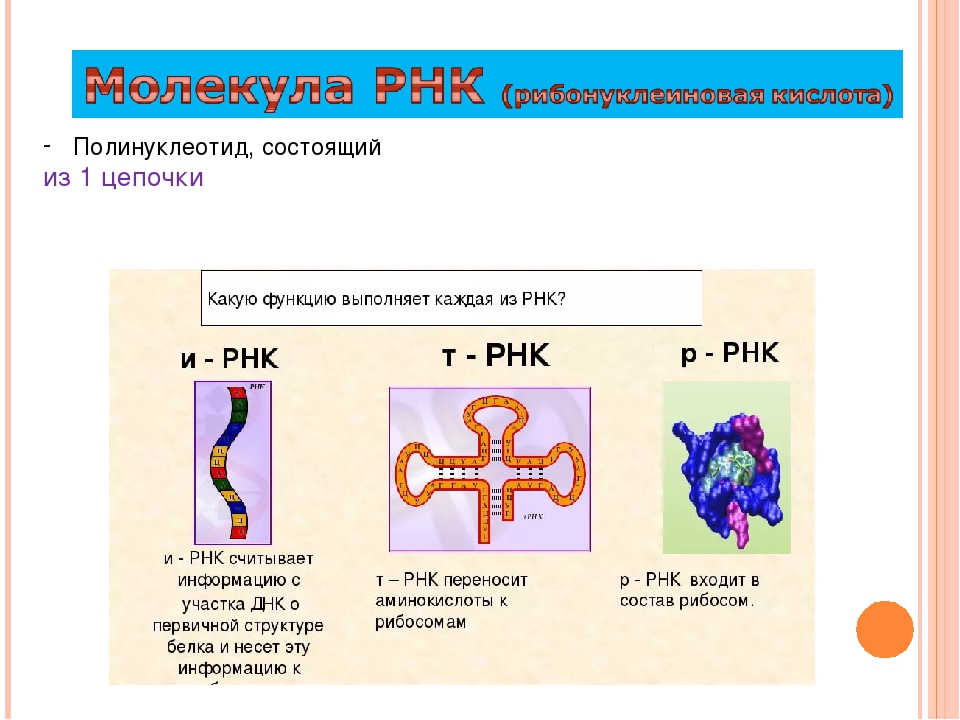
Идём дальше. Наверняка, вы уже встречались с названиями нуклеиновых кислот. Это может быть либо дезоксирибонуклеиновая кислота (ДНК), либо рибонуклеиновая кислота (РНК). Почему они так называются и как их различить? Несмотря на кажущуюся сложность, всё очень просто. Ключевая роль здесь отведена сахару, входящему в состав кислоты. Если это дезоксирибоза – кислота дезоксирибонуклеиновая. Если рибоза – рибонуклеиновая.
Обратимся к строению ДНК.
Следуя нашей схеме, ДНК – полимер. Мономером является нуклеотид. В состав нуклеотида входят остатки трёх веществ: фосфорной кислоты, дезоксирибозы и азотистого основания. Четыре из пяти азотистых оснований входит в состав ДНК: аденин, тимин, гуанин и цитозин.
Состав молекулы ДНК был известен задолго до открытия её структуры. В 1950 году американский учёный Эрвин Чаргафф установил важнейшие закономерности. Названные впоследствии правилами Чаргаффа. И которые вы обязательно должны запомнить:
1. Количество
адениловых нуклеотидов в молекуле ДНК равно количеству тимидиловых, а
количество гуаниловых – количеству цитидиловых.
Количество
адениловых нуклеотидов в молекуле ДНК равно количеству тимидиловых, а
количество гуаниловых – количеству цитидиловых.
2. Количество пуриновых азотистых оснований равно количеству пиримидиновых.
3. Суммарное количество адениловых и цитидиловых нуклеотидов равно суммарному количеству тимидиовых и гуаниловых нуклеотидов, что следует из первого правила.
На первый взгляд, это сложно, но решив уже пару задач на расчёт количества нуклеотидов, вы со всем разберётесь.
Знание состава дезоксирибонуклеиновой кислоты не проливало свет на её строение. Каково же пространственное расположение нуклеотидов в молекуле ДНК?
Оновываясь на исследованиях Чаргаффа, а также Розалинд Франклин
Джеймсу Уотсону и Фрэнсису Крику удалось найти ответ на этот вопрос.
Что
же было ими установлено? А ими была установлено, что ДНК – полинуклеотидная
цепочка, состоящая из двух цепей! В которой азотистые основания смотрят внутрь
этой цепочки. Этот ключевой момент и был самой главной загадкой для учёных.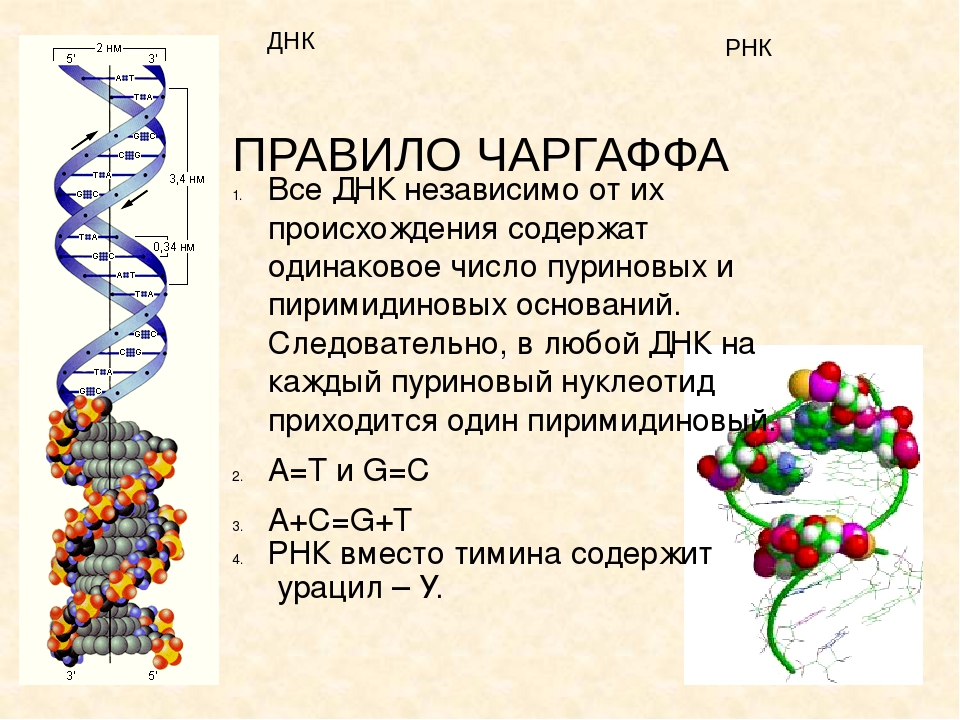 Кроме того, располагаются они не в произвольном порядке, а строго упорядоченно.
Это обусловлено тем, что между аденином и тимином в двойной спирали ДНК
возникает две водородные связи, а между гуанином и цитозином – три. Таким
образом, нуклеотиды образуют пары. А их соответствие друг другу называется комплементарностью.
Кроме того, располагаются они не в произвольном порядке, а строго упорядоченно.
Это обусловлено тем, что между аденином и тимином в двойной спирали ДНК
возникает две водородные связи, а между гуанином и цитозином – три. Таким
образом, нуклеотиды образуют пары. А их соответствие друг другу называется комплементарностью.
Комплементарность нуклеотидов обуславливает комплементарность и двух цепей ДНК. Они напоминают винтовую лестницу, так как закручены вокруг общей оси. Технические параметры этой лестницы таковы: диаметр около двух нанометров, один виток спирали включает в себя 10 пар нуклеотидов. Длина одного витка – 3,4 нанометра.
Таким
образом, со строением ДНК разобрались. Осталось назвать функции этого вещества
в организме. Они не будут разнообразными, как например, у белков. Но, как вы
понимаете, исключительно важными. Потому что в ДНК хранится вся наследственная
информация организма. Практически в каждой клетке живого существа содержится
информация о структуре всех его белков. И представлена она там в виде
последовательности нуклеотидов. То есть, в закодированном виде.
И представлена она там в виде
последовательности нуклеотидов. То есть, в закодированном виде.
Итак, ДНК отвечает за сохранность наследственной информации и передачу её потомкам в неизменном виде. Располагаются молекулы ДНК в эукариотической клетке, в основном, в ядре, а также в пластидах и митохондриях.
Что же, выдохнули, и давайте приниматься за РНК. Здесь попроще. Особенно после ДНК.
Вновь обратимся к нашей схеме. РНК – полимер. Мономером является нуклеотид. В состав нуклеотида входят остатки трёх веществ: фосфорной кислоты, рибозы и азотистого основания. Четыре из пяти азотистых оснований входит в состав РНК: аденин, урацил, гуанин и цитозин.
Молекулы РНК одноцепочечные и значительно короче молекул ДНК.
Но в отличие от ДНК, в клетке существует несколько видов РНК. Различаются они по размерам молекул, структуре и выполняемым функциям. Хотя все задействованы в одном важнейшем процессе – синтезе белка.
Рибосомные РНК (р-РНК) – самые многочисленные.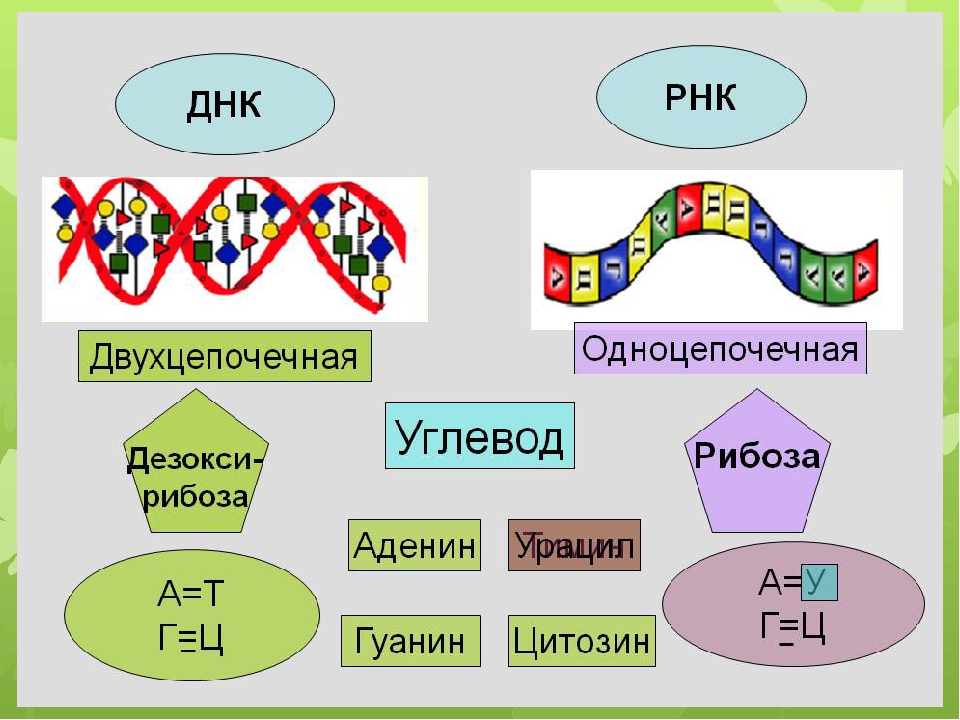 Они составляют до 80% всех РНК клетки. Р-РНК в
комплексе с белками являются основными структурными элементами рибосом, где
регулируют образование пептидных связей между аминокислотами.
Они составляют до 80% всех РНК клетки. Р-РНК в
комплексе с белками являются основными структурными элементами рибосом, где
регулируют образование пептидных связей между аминокислотами.
На долю транспортных РНК (т-РНК) приходится около 15% всех клеточных РНК. Молекулы т-РНК имеют сравнительно небольшие размеры – в среднем в их состав входит 80 нуклеотидов. А также достаточно изящную форму, которая напоминает листок клевера. От этого и пошло название структуры т-РНК – клеверный лист. Транспортные рибонуклеиновые кислоты переносят мономеры белков – аминокислоты – из цитоплазмы клетки к месту синтеза белка – в рибосомы.
И
третий вид рибонуклеиновых кислот клетки – информационные РНК (и-РНК),
либо их ещё называют матричными (м-РНК). Они являются самыми разнородными по
размерам и структуре. Так как они несут в себе информацию о строении самых
различных белков. Содержание и-РНК в клетке небольшое – 3-5% от всех РНК.
Чтобы представить себе функции информационных-РНК, забежим немножко вперёд и
одним глазком взглянем на процесс синтеза белка в клетке.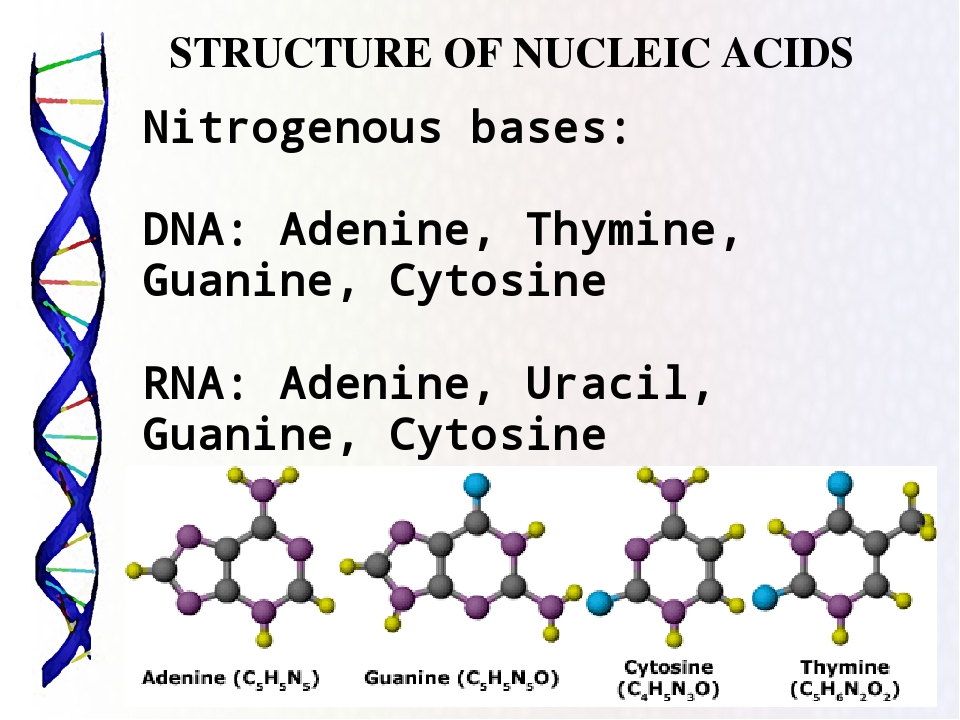
Мы уяснили, что информация о последовательности аминокислот, то есть о первичной структуре любого белка, находится в ядре клетки, в ДНК. А сборка самих белков из аминокислот происходит в других клеточных органеллах – в рибосомах. Значит, нужен какой-то механизм передачи информации из ядра в рибосомы. В качестве такого механизма и выступают информационные РНК. Они передают информацию о последовательности нуклеотидов ДНК в центры сборки белковых молекул.
ПРЕЗЕНТАЦИЯ ДЛЯ 9 КЛАССА ПО ТЕМЕ: НУКЛЕИНОВЫЕ КИСЛОТЫ. Учитель биологии ГБОУ СОШ 8. О.Ю. Ветренко
«Нуклеиновые кислоты»
Государственное бюджетное общеобразовательное учреждение Самарской области средняя общеобразовательная школа 8 пгт Алексеевка городского округа Кинель Самарской области Методическая разработка урока биологии
ПодробнееКонкурсный открытый урок
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РБ ГАОУ СПО Нефтекамский нефтяной колледж Посвящается году охраны окружающей среды Конкурсный открытый урок На тему: Нуклеиновые кислоты Тема урока: Нуклеиновые кислоты Цели урока:
ПодробнееБЛОК 2 Клетка как биологическая система.

1. К макроэлементам относятся: БЛОК 2 Клетка как биологическая система. 1) кислород, углерод, водород, азот 2) кислород, железо, золото 3) углерод, водород, бор 4) селен, азот, кислород 1) 2. Органоид,
ПодробнееОтложенные задания (30)
Отложенные задания (30) Вставьте в текст «ДНК» пропущенные термины из предложенного перечня, используя для этого цифровые обозначения. Запишите в текст цифры выбранных ответов, а затем получившуюся последовательность
ПодробнееОсновные генетические механизмы
Основные генетические механизмы Тренинг «Использование методики Xpert MTB/RIF», г.душанбе, 29 июля 2 августа 2013 г. Презентация подготовлена в рамках проекта USAID «Посилення контролю за туберкульозом
ПодробнееБелки, их строение и функции
2. 3.3. Белки, их строение и функции Белки это биологические гетерополимеры, мономерами которых являются аминокислоты. Белки синтезируются в живых организмах и выполняют в них определенные функции. В состав
3.3. Белки, их строение и функции Белки это биологические гетерополимеры, мономерами которых являются аминокислоты. Белки синтезируются в живых организмах и выполняют в них определенные функции. В состав
ОРГАНИЗАЦИЯ НАСЛЕДСТВЕННОГО МАТЕРИАЛА
Занятие 6. Тема: ОРНИЗИЯ НСЛЕДСТВЕННОО МТЕРИЛ (занятие I) » » 200 г ель занятия: изучить молекулярную природу гена, его свойства; научиться решать задачи, раскрывающие строение молекул ДНК и РНК, по репликации,
ПодробнееТема: «Нуклеиновые кислоты. ДНК»
Глава I. Основы цитологии На дом: 12 Тема: «Нуклеиновые кислоты. ДНК» Задачи: Дать характеристику нуклеиновым кислотам: видам НК, локализации их в клетке, строению, функциям. Изменено, дополнено Нуклеиновые
ПодробнееОБЩАЯ И МЕДИЦИНСКАЯ ГЕНЕТИКА
УЧЕБНОЕ ПОСОБИЕ ОБЩАЯ И МЕДИЦИНСКАЯ ГЕНЕТИКА ЗАДАЧИ Под редакцией профессора М. М. Азовой Министерство образования и науки Р Рекомендовано Координационным советом по области образования «Здравоохранение
М. Азовой Министерство образования и науки Р Рекомендовано Координационным советом по области образования «Здравоохранение
Решение задач. по молекулярной биологии.
Учитель биологии Зозуля Е.В.. Ноябрь 2014. Решение задач по молекулярной биологии. Молекулярная биология изучает механизмы хранения и передачи наследственной информации. Задачи по молекулярной биологии
ПодробнееID_2853 1/6 neznaika.pro
1 Клетка, её жизненный цикл (установление соответствия) Ответами к заданиям являются слово, словосочетание, число или последовательность слов, чисел. Запишите ответ без пробелов, запятых и других дополнительных
ПодробнееТема: Учение о клетке
Государственное бюджетное образовательное учреждение среднего профессионального образования «Кущевский медицинский колледж» министерства здравоохранения Краснодарского края Задания в тестовой форме по
ПодробнееРЕШЕНИЕ ЗАДАЧ ПО МОЛЕКУЛЯРНОЙ БИОЛОГИИ
РЕШЕНИЕ ЗАДАЧ ПО МОЛЕКУЛЯРНОЙ БИОЛОГИИ Шарлаева Елена Анатольевна, к. б.н., доцент каф. экологии, биохимии и биотехнологии АлтГУ, зам. председ. предм. комиссии ЕГЭ по биологии Для решения задач необходимо
б.н., доцент каф. экологии, биохимии и биотехнологии АлтГУ, зам. председ. предм. комиссии ЕГЭ по биологии Для решения задач необходимо
Репликация ДНК Биосинтез белка
Репликация ДНК Биосинтез белка Репликация удвоение молекулы ДНК Происходит в S (синтетический)период митотического цикла Образующиеся дочерние молекулы — точные копии материнской Принципы репликации Комплементарность
ПодробнееМолекулярная биология
Молекулярная биология Курс лекций для студентов IV курса факультета биологии РГПУ им. А.И. Герцена Профессор кафедры Зоологии, д.б.н., профессор Цымбаленко Надежда Васильевна СТРУКТУРА БЕЛКА ЛЕКЦИЯ 9 Структура
ПодробнееЗадание 4, (25 баллов)
Задание 4, вариант 1. Гены эукариотических клеток имеют «мозаичное» строение и состоят из кодирующих элементов (экзонов) и некодирующих участков (интронов). По завершении транскрипции образуется «незрелый»
По завершении транскрипции образуется «незрелый»
Терминологический диктант
Терминологический диктант Органы цветковых растений. 1 Часть тела организма выполняет определенную функцию… 2 В почве растение удерживает.. 3 Многочисленные разветвленные корни образуют. 4 В корневой
ПодробнееЗадания B6 по биологии
Задания B6 по биологии 1. Установите соответствие между особенностями строения и свойств вещества и веществом, имеющим эти особенности. ОСОБЕННОСТИ СТРОЕНИЯ И СВОЙСТВ ВЕЩЕСТВА А) неполярны, нерастворимы
ПодробнееO, H, C, N + S, P — макроэлементы. Na, K, Mg, Ca, Cl — микроэлементы Fe, Zn, Cu, Co, Mn, I, Se следовые элементы
O, H, C, N + S, P — макроэлементы Na, K, Mg, Ca, Cl — микроэлементы Fe, Zn, Cu, Co, Mn, I, Se следовые элементы Представленность макроэлементов в различных группах веществ Макромолекулы Сахара (углеводы)
ПодробнееДальтон единица измерения массы вещества, равная 1,661 x г, используемая для измерения массы вирусов, клеток, хромосом, митохондрий, рибосом, а
Д Дальтон единица измерения массы вещества, равная 1,661 x 10 24 г, используемая для измерения массы вирусов, клеток, хромосом, митохондрий, рибосом, а также молекул ДНК, РНК и белков.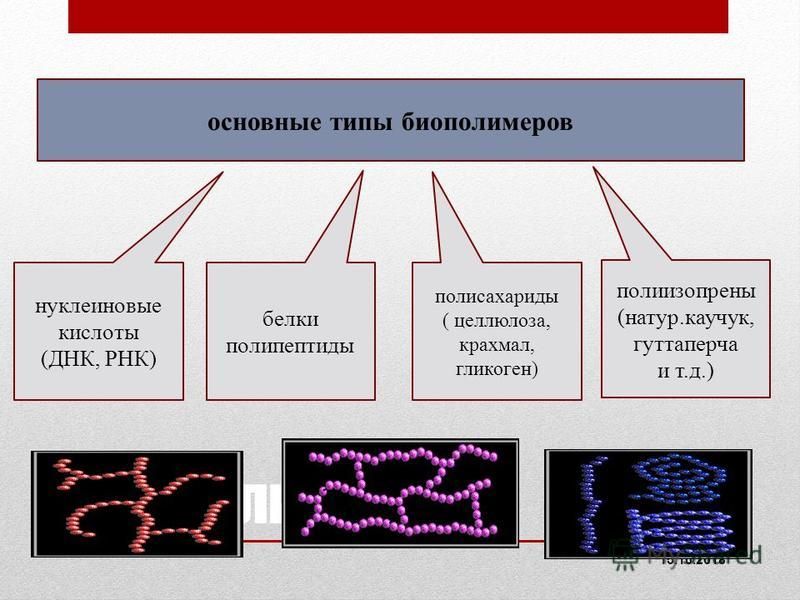 Дарвинизм теория,
Дарвинизм теория,
9 класс Биология П1 ПРОФИЛЬ.
9 класс Биология П1 ПРОФИЛЬ. Мономером ДНК является: Задание 1 нуклеозид нуклеотид глюкоза аминокислота Задание 2 Вторичная структура каждой т-рнк имеет не сколько петель благодаря тому, что соседние с
Подробнее10класс Биология погружение 3
10класс Биология погружение 3 Тема: Энергетический обмен. 1. Наибольшее количество энергии освобождается при расщеплении молекул 1) белков 2) жиров 3) углеводов 4) нуклеиновых кислот 2. В бескислородной
ПодробнееКонспект урока по биологии в 9 классе по теме «Нуклеиновые кислоты»
Руководство по усвоению
учебного материала
Внимательно прочитайте цель
урока.
Прочитайте параграф 1.6,
стр.29.
Работайте самостоятельно.
Правильный ответ – 3 балла.
Правильный ответ – 1 балл. См. параграф 1.6,
стр.2931, рис.9,10,11.
Работайте с партнером по парте.
Правильный ответ – 8 баллов
См. параграф 1.6, стр.2931,
Правильный ответ – 1 балл
См. параграф 1.6,
стр.30,31, рис.11.
Правильный ответ – 3 балла.
См. параграф 1.6, стр.30,31.
Правильный ответ – 2 балла.
Работайте самостоятельно.
Правильный ответ – 5 баллов
Тема: Нуклеиновые кислоты.
Номе
р УЭ
УЭ 0 Цель урока: познакомиться с различными видами нуклеиновых
Учебный материал с указанием заданий
кислот и их функциями.
УЭ 1 Строение молекулы ДНК.
Цель: выяснить особенности строения ДНК.
I. Выполните задания:
1.Вставьте пропущенные слова:
Сложные углеводы, белки и ________________________ относят к
группе биополимеров. Различают два типа нуклеиновых кислот
_________________ и ______________.
2. Между первым и вторым понятием существует определенная связь.
Аналогичная связь существует между третьим и одним из
приведенных ниже понятий. Найдите это понятие.
Белок:полипептид=нуклеиновые кислоты:
1.
См. параграф 1.6,
стр.2931, рис.9,10,11.
Работайте с партнером по парте.
Правильный ответ – 8 баллов
См. параграф 1.6, стр.2931,
Правильный ответ – 1 балл
См. параграф 1.6,
стр.30,31, рис.11.
Правильный ответ – 3 балла.
См. параграф 1.6, стр.30,31.
Правильный ответ – 2 балла.
Работайте самостоятельно.
Правильный ответ – 5 баллов
Тема: Нуклеиновые кислоты.
Номе
р УЭ
УЭ 0 Цель урока: познакомиться с различными видами нуклеиновых
Учебный материал с указанием заданий
кислот и их функциями.
УЭ 1 Строение молекулы ДНК.
Цель: выяснить особенности строения ДНК.
I. Выполните задания:
1.Вставьте пропущенные слова:
Сложные углеводы, белки и ________________________ относят к
группе биополимеров. Различают два типа нуклеиновых кислот
_________________ и ______________.
2. Между первым и вторым понятием существует определенная связь.
Аналогичная связь существует между третьим и одним из
приведенных ниже понятий. Найдите это понятие.
Белок:полипептид=нуклеиновые кислоты:
1. полисахарид; 2.полиамид; 3.полинуклеотид;
4.поливинилхлорид
3. Рассмотрите рисунок. Назовите вещества, входящие в состав
нуклеотидов ДНК и РНК (А, 13). Сколько типов нуклеотидов
встречается в молекулах ДНК и РНК? В тетради выпишите
соответствующие буквенные обозначения для ДНК и РНК (рис.Б, 1
4).
А Б
1 3
1
2
3
общая схема нуклеотида 2 4
типы нуклеотидов
4. Молекулы ДНК состоят из 4 типов нуклеотидов, однако
многообразие молекул ДНК бесконечно. Чем это объясняется?
5. В основе строения молекул ДНК лежит принцип
комплементарности. Используя этот принцип, на предложенной одной
цепи молекулы ДНК постройте вторую цепь:
А – А – Т – Г – Ц – Ц – Т – Г – А
6.
полисахарид; 2.полиамид; 3.полинуклеотид;
4.поливинилхлорид
3. Рассмотрите рисунок. Назовите вещества, входящие в состав
нуклеотидов ДНК и РНК (А, 13). Сколько типов нуклеотидов
встречается в молекулах ДНК и РНК? В тетради выпишите
соответствующие буквенные обозначения для ДНК и РНК (рис.Б, 1
4).
А Б
1 3
1
2
3
общая схема нуклеотида 2 4
типы нуклеотидов
4. Молекулы ДНК состоят из 4 типов нуклеотидов, однако
многообразие молекул ДНК бесконечно. Чем это объясняется?
5. В основе строения молекул ДНК лежит принцип
комплементарности. Используя этот принцип, на предложенной одной
цепи молекулы ДНК постройте вторую цепь:
А – А – Т – Г – Ц – Ц – Т – Г – А
6. Что представляет собой вторичная структура ДНК? Какие связи ее
поддерживают?
Выполните тестовое задание:
II.
1. В каком случае правильно указан состав нуклеотида ДНК?
А) рибоза, остаток фосфорной кислоты, тимин; Б)
фосфорная кислота, урацил, дезоксирибоза;
В) остаток фосфорной кислоты, дезоксирибоза, аденин.
2. Мономерами нуклеиновых кислот являются:
А)аминокислоты, Б)нуклеотиды, В)глюкоза, Г)глицерин и
жирные кислоты.
3. Вторичная структура ДНК поддерживается за счет
водородных связей между:
А)соседними нуклеотидами, Б)комплементарными
основаниями в двух цепях, В)остатками фосфорной кислоты
в остове цепей.
4. В клетке ДНК содержится в:
А)ядре и митохондриях, Б)только в ядре, В) ядре и
цитоплазме.
5. Функция ДНК в клетке:
А)хранение и передача наследственных свойств; Б) перенос аминокислот на рибосомы; В)каталитическая.
III.
Проверьте и оцените свою работу.
УЭ 2
Строение рибонуклеиновых кислот.
Цель: ознакомиться с особенностями строения рибонуклеиновых
кислот (РНК), их видами и функциями; уметь сравнивать
строение молекул ДНК и РНК.
Что представляет собой вторичная структура ДНК? Какие связи ее
поддерживают?
Выполните тестовое задание:
II.
1. В каком случае правильно указан состав нуклеотида ДНК?
А) рибоза, остаток фосфорной кислоты, тимин; Б)
фосфорная кислота, урацил, дезоксирибоза;
В) остаток фосфорной кислоты, дезоксирибоза, аденин.
2. Мономерами нуклеиновых кислот являются:
А)аминокислоты, Б)нуклеотиды, В)глюкоза, Г)глицерин и
жирные кислоты.
3. Вторичная структура ДНК поддерживается за счет
водородных связей между:
А)соседними нуклеотидами, Б)комплементарными
основаниями в двух цепях, В)остатками фосфорной кислоты
в остове цепей.
4. В клетке ДНК содержится в:
А)ядре и митохондриях, Б)только в ядре, В) ядре и
цитоплазме.
5. Функция ДНК в клетке:
А)хранение и передача наследственных свойств; Б) перенос аминокислот на рибосомы; В)каталитическая.
III.
Проверьте и оцените свою работу.
УЭ 2
Строение рибонуклеиновых кислот.
Цель: ознакомиться с особенностями строения рибонуклеиновых
кислот (РНК), их видами и функциями; уметь сравнивать
строение молекул ДНК и РНК.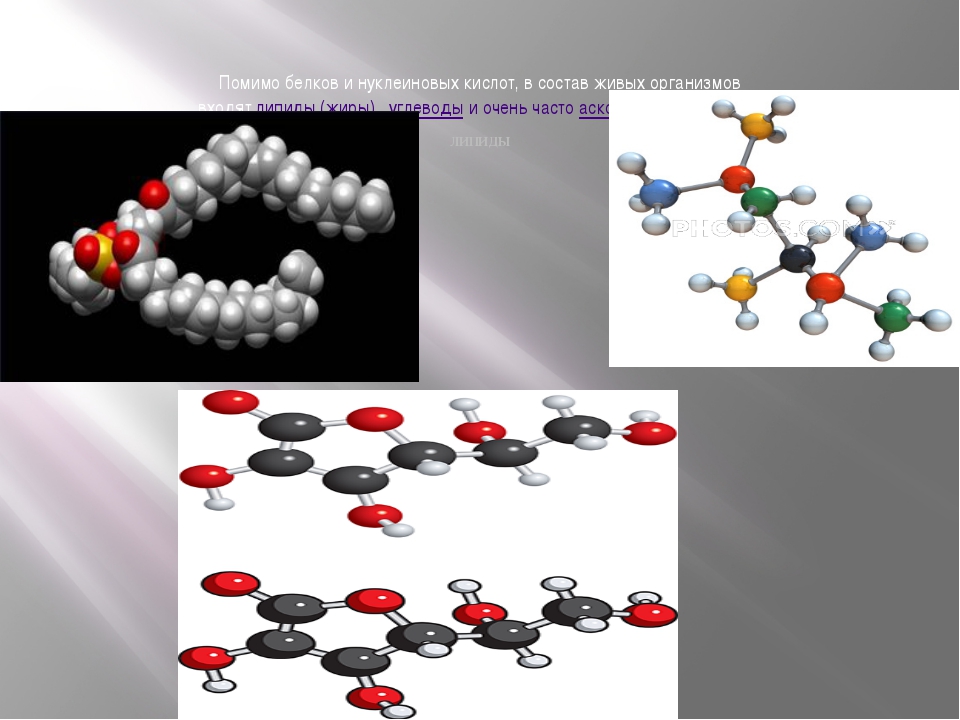 I.
Выполните задания:
1.Рассмотрите рисунок. Назовите вещества, входящие в состав
нуклеотидов РНК (А, 13). Какие типы нуклеотидов встречаются в
молекулах РНК? (рис.Б, 14).
А Б
1 3
1
2
3
общая схема нуклеотида 2 4
типы нуклеотидов
2. Заполните таблицу.
Основные виды РНК
Вид РНК
1.
2.
3.
3. Выявите сходства и различия в строении молекул ДНК и РНК,
заполнив таблицу.
Функции
Признаки сравнения
ДНК
РНК
1. Структура молекулы
2. Количество цепей
3. Моносахариды в нуклеотидах
4. Локализация в
клетке(размещение)
5. Функции
II.
Обсудите и оцените свою работу.
Максимальное количество баллов
за УЭ1 – 21 балл.
I.
Выполните задания:
1.Рассмотрите рисунок. Назовите вещества, входящие в состав
нуклеотидов РНК (А, 13). Какие типы нуклеотидов встречаются в
молекулах РНК? (рис.Б, 14).
А Б
1 3
1
2
3
общая схема нуклеотида 2 4
типы нуклеотидов
2. Заполните таблицу.
Основные виды РНК
Вид РНК
1.
2.
3.
3. Выявите сходства и различия в строении молекул ДНК и РНК,
заполнив таблицу.
Функции
Признаки сравнения
ДНК
РНК
1. Структура молекулы
2. Количество цепей
3. Моносахариды в нуклеотидах
4. Локализация в
клетке(размещение)
5. Функции
II.
Обсудите и оцените свою работу.
Максимальное количество баллов
за УЭ1 – 21 балл. См. параграф 1.6,
стр.3132.
Работайте индивидуально.
Правильный ответ – 7 баллов.
См. параграф 1.6,
стр.32.
Работайте с партнером по парте.
Правильный ответ – 6 баллов
См. параграф 1.6,
стр.2932.
Работайте в группе.
Правильный ответ – 10 баллов.
Максимальное количество баллов
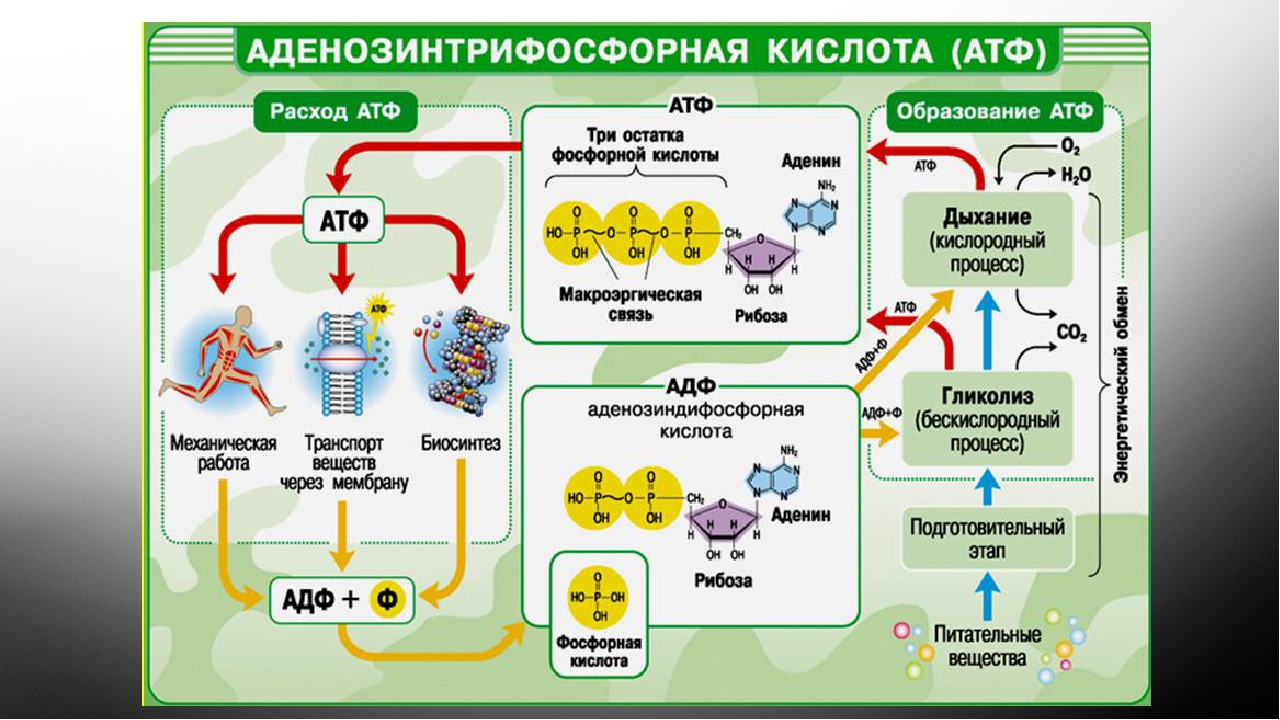
за УЭ2 – 23 балла. Тема: АТФ и другие органические соединения клетки.
Номе
р УЭ
УЭ 0
Учебный материал с указанием заданий
Цель урока: познакомиться с особенностями строения и
функциями АТФ и других органических соединений.
УЭ 1 Строение молекулы АТФ.
Цель: выделить особенности строения АТФ и ознакомиться с ее
функциями.
I. Выполните задания:
1. Обозначьте на рисунке составные части молекулы АТФ, подпишите
их.
О О О
О – Р – О – Р – О – Р – ОН
ОН ОН ОН
2
1 3
Руководство по усвоению
учебного материала
Внимательно прочитайте цель
урока.
См. параграф 1.6,
стр.3132.
Работайте индивидуально.
Правильный ответ – 7 баллов.
См. параграф 1.6,
стр.32.
Работайте с партнером по парте.
Правильный ответ – 6 баллов
См. параграф 1.6,
стр.2932.
Работайте в группе.
Правильный ответ – 10 баллов.
Максимальное количество баллов
за УЭ2 – 23 балла. Тема: АТФ и другие органические соединения клетки.
Номе
р УЭ
УЭ 0
Учебный материал с указанием заданий
Цель урока: познакомиться с особенностями строения и
функциями АТФ и других органических соединений.
УЭ 1 Строение молекулы АТФ.
Цель: выделить особенности строения АТФ и ознакомиться с ее
функциями.
I. Выполните задания:
1. Обозначьте на рисунке составные части молекулы АТФ, подпишите
их.
О О О
О – Р – О – Р – О – Р – ОН
ОН ОН ОН
2
1 3
Руководство по усвоению
учебного материала
Внимательно прочитайте цель
урока. Прочитайте параграф 1.7,
стр.3334,рис.12
Работайте самостоятельно.
Правильный ответ – 3 балла.
2. Чем отличается АТФ от обычных нуклеотидов?
Правильный ответ – 2 балла.
3. Молекула АТФ содержит богатые энергией связи. Как называются
эти связи? Какое количество энергии освобождается при разрыве
одной или двух таких связей в молекуле АТФ?
См. параграф 1.7,
Стр.3334 Работайте индивидуально
Правильный ответ – 3 балла
УЭ 2
УЭ3
4. Какую функцию выполняет АТФ в клетке?
II. Проверьте и оцените свою работу.
Органические соединения клетки.
Цель: ознакомиться с другими органическими соединениями
клетки.
I.
Заполните схему:
1.
Выполните задания:
См. параграф 1.7, стр.34,
Правильный ответ – 2 балла
Максимальное количество баллов
за УЭ1 – 10 баллов.
См. параграф 1.7,
стр.34.
Работайте индивидуально.
Правильный ответ – 2 балла.
Витамины
В С РР А Д Е К
2. Ответьте на вопросы.
Какова роль витаминов в организме? Почему некоторые
ферменты активны только в присутствии витаминов? В каком
центре фермента работают витамины?
См.
Прочитайте параграф 1.7,
стр.3334,рис.12
Работайте самостоятельно.
Правильный ответ – 3 балла.
2. Чем отличается АТФ от обычных нуклеотидов?
Правильный ответ – 2 балла.
3. Молекула АТФ содержит богатые энергией связи. Как называются
эти связи? Какое количество энергии освобождается при разрыве
одной или двух таких связей в молекуле АТФ?
См. параграф 1.7,
Стр.3334 Работайте индивидуально
Правильный ответ – 3 балла
УЭ 2
УЭ3
4. Какую функцию выполняет АТФ в клетке?
II. Проверьте и оцените свою работу.
Органические соединения клетки.
Цель: ознакомиться с другими органическими соединениями
клетки.
I.
Заполните схему:
1.
Выполните задания:
См. параграф 1.7, стр.34,
Правильный ответ – 2 балла
Максимальное количество баллов
за УЭ1 – 10 баллов.
См. параграф 1.7,
стр.34.
Работайте индивидуально.
Правильный ответ – 2 балла.
Витамины
В С РР А Д Е К
2. Ответьте на вопросы.
Какова роль витаминов в организме? Почему некоторые
ферменты активны только в присутствии витаминов? В каком
центре фермента работают витамины?
См. параграф 1.7,
стр.3435.
Работайте индивидуально.
Правильный ответ – 3 балла.
II.
Обсудите и оцените свою работу.
I.
Подведение итогов работы.
1. Прочитайте цели урока.
2. Достигли ли вы поставленной цели? В какой степени?
3. Оцените свою работу на уроке.
Если по итогам работы вы набрали:
От 58 до 66 баллов – оценка «5»;
От 50 до 57 баллов – оценка «4»;
От 36 до 49 баллов – оценка «3»;
Менее 35 баллов – оценка «2».
Максимальное количество баллов
за УЭ2 – 12 баллов.
Самостоятельно
Ваша оценка:________.
Сдайте тетради учителю ( в
индивидуальном порядке). УЭ4
II.
Домашнее задание:
Если вы получили оценку «5» получите творческое задание.
Темы для сообщений:
Нуклеиновые кислоты и возраст.
Нуклеиновые кислоты и наследственные заболевания.
Нуклеиновые кислоты и инфекционные болезни.
параграф 1.7,
стр.3435.
Работайте индивидуально.
Правильный ответ – 3 балла.
II.
Обсудите и оцените свою работу.
I.
Подведение итогов работы.
1. Прочитайте цели урока.
2. Достигли ли вы поставленной цели? В какой степени?
3. Оцените свою работу на уроке.
Если по итогам работы вы набрали:
От 58 до 66 баллов – оценка «5»;
От 50 до 57 баллов – оценка «4»;
От 36 до 49 баллов – оценка «3»;
Менее 35 баллов – оценка «2».
Максимальное количество баллов
за УЭ2 – 12 баллов.
Самостоятельно
Ваша оценка:________.
Сдайте тетради учителю ( в
индивидуальном порядке). УЭ4
II.
Домашнее задание:
Если вы получили оценку «5» получите творческое задание.
Темы для сообщений:
Нуклеиновые кислоты и возраст.
Нуклеиновые кислоты и наследственные заболевания.
Нуклеиновые кислоты и инфекционные болезни.
как работают «лекарства для генов»
Мало кто знает, что на основе ДНК и РНК можно сделать лекарства, способные противостоять инфекции и даже исправлять мутации у людей с генетическими заболеваниями. О том, как работают разнообразные методы этой отрасли и какие проблемы в ней только предстоит разрешить, школьникам «Сириуса» рассказал Валентин Власов – доктор биологических наук, академик РАН и научный руководитель Института химической биологии и фундаментальной медицины СО РАН.
О том, как работают разнообразные методы этой отрасли и какие проблемы в ней только предстоит разрешить, школьникам «Сириуса» рассказал Валентин Власов – доктор биологических наук, академик РАН и научный руководитель Института химической биологии и фундаментальной медицины СО РАН.
Как заставить гены молчать
Нуклеотиды – «буквы» ДНК (дезоксирибонуклеиновой кислоты) и РНК (рибонуклеиновой кислоты), молекул, в которых хранится и передается генетическая информация. Хотя «букв» в этом своеобразном алфавите всего четыре (А, У, Г и Ц в ДНК и А, Т, Г и Ц в РНК), с их помощью можно записать осмысленный «текст» – гены (инструкцию по сборке белков, о которой ученикам недавно рассказывал другой гость, Денис Ребриков). Эта инструкция переписывается с двуцепочечной молекулы ДНК, которая находится в ядрах наших клеток, на одноцепочечную молекулу РНК, и уже с нее синтезируется белок.
Но нуклеотиды не просто служат для записи инструкций по сборке – из их цепочек можно делать лекарства, которые будут разрушать систему синтеза белка у вирусов или бактерий, привязываться к определенным молекулам или даже «чинить» мутации в генах. Лекарства на основе нуклеотидов действуют по относительно легко объяснимому принципу и обычно очень специфичны: на каждую конкретную последовательность можно «натравить» свою цепочку нуклеотидов. Это работает потому, что каждый из четырех типов «букв» может образовать пару с другим. В ДНК две цепи держатся вместе, так как в каждой из них напротив стоят определенные буквы, тянущие друг к другу «руки» химических связей.
Лекарства на основе нуклеотидов действуют по относительно легко объяснимому принципу и обычно очень специфичны: на каждую конкретную последовательность можно «натравить» свою цепочку нуклеотидов. Это работает потому, что каждый из четырех типов «букв» может образовать пару с другим. В ДНК две цепи держатся вместе, так как в каждой из них напротив стоят определенные буквы, тянущие друг к другу «руки» химических связей.
Если сделать цепочку нуклеотидов, соответствующую последовательности РНК, которая будет создана с нужного (а точнее – ненужного) гена, то наше лекарство, используя все те же связи между парными буквами, сыграет роль «второй цепи», сделает молекулу похожей на ДНК и заблокирует эту последовательность. С нее не произведется белок, и вред «неправильного» гена будет нейтрализован. Такие цепочки называют антисенс-РНК (или антисмысловыми РНК), так как они лишают записанный в определенном гене «текст» его «смысла» . При этом по теории вероятности произвольно выбранная последовательность из всего 20 нуклеотидов у человека встретится лишь один раз на весь геном, так что риск ошибки очень невелик.
Множество разных лекарств на основе нуклеиновых кислот легко одновременно делать на заводе: из одних и тех же типов нуклеотидов строится огромное количество последовательностей. Работать такие лекарства могут по-разному: менять структуру гена, действовать на одну из стадий синтеза белка, на активирование РНК перед этим синтезом и так далее.
Ирония судьбы и нуклеиновый Уроборос
Первая научная публикация на эту тему появилась в 1967 году, а Валентин Власов стал одним из ее соавторов. Вскоре биологи получили письмо из США: некий студент по имени Джон Саммертон поздравлял коллег и сетовал, что самому ему также приходила эта идея, но вот финансирование получить не удалось. Три десятка лет спустя он откроет морфолино – одну из молекул, при помощи которой можно блокировать синтез определенных белков, – и станет главой крупнейшей компании по производству противовирусных лекарств на основе цепочек нуклеотидов (один из примеров – препарат от вируса Эбола).
Некоторые рибонуклеиновые кислоты не просто блокируют РНК, чтобы с нее не мог производиться белок, а разрезают ее – то есть выполняют работу, которую обычно делают ферменты (белки, которые катализируют реакции). Теоретически такие молекулы могли стать основой будущей жизни, катализируя воспроизводство самих себя во времена, когда еще не было ни белков, ни ДНК. Такие многофункциональные рибонуклеиновые кислоты назвали рибозимами – от «рибонуклеиновая кислота» (РНК), и «энзим» (фермент). За открытие рибозимов Сидни Олтмен и Томас Чек получили Нобелевскую премию по химии.
В 1998 году биологи открыли еще один интересный эффект, который назвали РНК-интерференцией. Наша клетка «привыкла» видеть РНК в виде одной цепи. Появление двуцепочечной часто означает вторжение геномных паразитов – вирусов, у которых можно встретить такую причудливую конструкцию. Поэтому такая РНК вызывает немало подозрений, и клетки научились заставлять «молчать» гены, которым она соответствует. Введя в клетку специально подобранную двуцепочечную РНК, можно добиться блокировки определенного гена.
«Генетические ножницы» и путеводные аптамеры
В начале 90-х годов ученые развили технологию, при помощи которой можно получать аптамеры – цепочки нуклеотидов, удивительно точно распознающие определенную «мишень». Такой мишенью может стать белок, который нужно блокировать или просто обнаружить. Чтобы создать аптамеры, достаточно насинтезировать много случайных последовательностей нуклеотидов, а потом предоставить этим цепочкам возможность связаться с мишенью – клюнуть на молекулярную «удочку». Затем молекулы, которые избежали этой участи, отмываются специальным раствором. Этот процесс можно повторить несколько раз. После такого искусственного отбора остаются только те молекулы, которые хорошо привязываются к нужной мишени. Это и есть аптамеры. Их можно размножить при помощи специальной реакции, которая называется ПЦР, и использовать в медицине. К примеру, уже сейчас существуют аптамеры, которые связываются с белками на поверхности клеток рака простаты. Ученые присоединили их к лекарственной молекуле, и теперь она сама может находить свою цель.
Еще один знаменитый многообещающий метод, CRISPR/Cas9, ученые подсмотрели у бактерий. У нас в организме есть множество разновидностей иммунных клеток, а бактериальные организмы одноклеточны. Несмотря на это, у них есть собственный иммунитет, позволяющий защищаться от вирусов. Бактерии вносят кусочки ДНК своих врагов в специальную «картотеку», которую хранят в своем геноме. Если тот же вирус появляется в клетке снова и хочет синтезировать белок за ее счет, специальные белки Cas будут узнать его РНК и разрезать ее. Если же в такую «картотеку» вставить нужную нам последовательность, систему CRISPR/Cas9 можно использовать для редактирования генов. Эту систему часто сравнивают с волшебными генетическими ножницами – место разреза можно выбрать довольно точно, так что ее перспективы в редактировании человеческого генома более чем заманчивы. Более того, метод уже применили для излечения генетических заболеваний у первых пациентов.
Бдительный иммунитет и светлое будущее
Однажды в экспериментах с мышами, больными энцефалитом, Валентин Власов и его коллеги обнаружили, что иммунный ответ возник не только у мышей, которым ввели специфические для вируса энцефалита последовательности, но и у группы контроля, которой просто вводили случайные цепочки нуклеотидов. Ученые решили, что эксперимент не удался, но позднее другие биологи оказались упорнее и сообразительнее и выяснили, чем вызван этот странный эффект.
«Природа тоже умная и широко использует этот принцип – олигонуклеотиды действуют слишком хорошо, а не просто прилипают. Мы ожидали, что наш олигонуклеотид свяжется и будет мешать синтезу белка. Оказалось, что в клетке есть фермент рибонуклеаза H, который атакует такие комплексы и разрезает их. То есть, можно не просто блокировать мишень, а уничтожить ее», – рассказал академик.
Так была открыта «нелюбовь» организма к чужим нуклеиновым кислотам. Ученые установили, что наш иммунитет умеет отличать их от «родных» по некоторым признакам. Например, в наших генах на последовательностях Г-Ц висит специальная метка – метильная группа. У бактерий ее нет, поэтому последовательность без метки наша клетка принимает за бактериальную и начинает «воевать» против нее.
Несмотря на такое разнообразие потенциальных лекарств на основе нуклеиновых кислот, до реального применения дошли лишь несколько. Активно внедрять эту группу лекарств в клиническую практику мешают ее недостатки: такие молекулы могут быть беззащитны перед ферментами организма, которые будут стремиться их разрезать, да и клеточная оболочка тоже очень привередливо относится ко всевозможным непрошеным гостям, тем более если они большого размера и тоже заряжены отрицательно, как и она сама (а значит, будут от нее отталкиваться). К тому же, организм большой, и во все клетки сразу лекарство не доставить. Напротив – чаще всего оно требуется только в клетках определенного типа. Поэтому ученые подбирают нуклеиновым кислотам носители (например, золотые наночастицы), химически модифицируют их, привязывают к ним молекулы, которые сыграют роль «системы самонаведения». Решить эти задачи предстоит сегодняшним школьникам – и, возможно, вскоре они увидят широкое применение этой отрасли в медицине.
Биологические молекулы • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Жизнь — таинственная, сложная, загадочная — не что иное как совокупность достаточно крупных молекул и довольно простых химических реакций. Если бы вам понадобилось конструировать крупные молекулы, вы пошли бы по одному из двух путей. Либо, как в кустарном ювелирном деле, вы стали строить каждую молекулу «с нуля», проделывая каждый раз уникальную работу. Либо — этот путь используется в современных строительных технологиях — вы бы изготовили набор простых молекул, из которых можно собирать самые разнообразные молекулы большего размера, сочетая модули тем или иным образом. Оказывается, именно такое модульное строение имеют биологические молекулы. Согласно теории эволюции, таким и должен был быть самой простой путь к крупным молекулам, поскольку в начале эволюционного процесса необходимость в конструировании очень сложных молекул отсутствовала. Со временем же могли добавляться новые модули, расширяя коллекцию крупных разнородных элементов, что вполне соответствует духу эволюции.
Белки
Основной структурной единицей белков являются молекулы аминокислот. Чтобы понять, что такое аминокислота, представьте себе совокупность атомов, у которых с одной стороны наружу выступает водород, с другой — соединенные между собой кислород и водород, а посередине расположены разнообразные другие компоненты. Подобно тому как бусины нанизываются на нить, из этих аминокислот собираются белки — ион водорода (Н+) одной аминокислоты объединяется с ионом гидроксила (ОН–) другой аминокислоты с образованием молекулы воды. (Представьте, как каждый раз при соединении двух аминокислотных молекул между ними пробегает капелька воды.) Среди белков самую важную роль играют белки-ферменты (см. Катализаторы и ферменты), регулирующие химические реакции в клетках; но белки также являются важными структурными компонентами живых организмов. Например, ваши волосы и ногти состоят из белков.
Углеводы
Углеводы содержат кислород, водород и углерод в соотношении 1:2:1. Во многих живых системах молекулы углеводов выполняют роль источников энергии. Одним из важнейших углеводов можно считать сахар глюкозу, содержащую шесть атомов углерода (С6Н12О6). Глюкоза — конечный продукт фотосинтеза и, следовательно, основа всей пищевой цепи в биосфере. Соединяя молекулы глюкозы, как основные строительные модули, можно получить сложные углеводы. Как и белки, углеводы играют вспомогательную роль в клетках, поскольку входят в клеточные структуры. Например, растительные волокна состоят из целлюлозы, которая представляет собой вереницу сцепленных особым образом молекул глюкозы.
Липиды
Липиды — это нерастворимые в воде органические молекулы. Вы получите правильное представление о липидах, если вообразите капельки жира, плавающие на поверхности бульона. В живых организмах липиды выполняют две важные функции. Один класс молекул — фосфолипиды — состоят из маленькой головки, содержащей фосфатную группу (атом фосфора, соединенный с четырьмя атомами кислорода), и длинного углеводородного хвоста. Углеводородный хвост этой молекулы гидрофобен, то есть энергетическое состояние молекулы минимально, когда этот хвост находится не в воде. Напротив, фосфатная головка гидрофильна, то есть энергетическое состояние молекулы минимально при контакте головки с водой . Если поместить молекулы фосфолипидов в воду, они будут стремиться достичь минимального энергетического состояния и выстроятся таким образом, что их хвосты окажутся вместе, а головки — врозь. Такая двухслойная структура очень стабильна, поскольку головки будут в контакте с водой, но вода будет вытеснена из области, окружающей хвосты молекул. Для перемещения липидным молекулам необходима энергия — либо чтобы удалить гидрофильные участки из воды, либо чтобы поместить в воду гидрофобные участки. Из таких липидных двухслойных структур состоят клеточные мембраны и мембраны, разделяющие компоненты клетки. Эти пластичные и прочные молекулы отделяют живое от неживого.
Кроме того, в липидах запасается энергия. Липиды могут накапливать примерно вдвое больше энергии на единицу массы, чем углеводы. Вот почему, когда вы переедаете и ваш организм хочет запасти энергию на случай непредвиденных обстоятельств в будущем, когда пищи не будет, он станет запасать ее в форме жира. На этом простом факте строится многомиллиардная индустрия диетических продуктов.
Нуклеиновые кислоты
Молекулы ДНК и РНК (см. Центральная догма молекулярной биологии) переносят информацию о химических процессах, идущих в клетке, и участвуют в передаче содержащейся в ДНК информации в цитоплазму клетки. В ДНК живого организма закодированы белки-ферменты, которые катализируют все химические реакции, происходящие в этом организме.
Молекулы-переносчики энергии
Жизнедеятельность требует затрат энергии. В частности, нужно, чтобы энергия, произведенная в одном месте, могла быть использована в другом. Эту функцию в клетке осуществляет целая армия специализированных молекул. Пожалуй, самые важные из них — аденозин трифосфат (АТФ) и аденозин дифосфат (АДФ). Обе молекулы устроены так: группа из атомов углерода, водорода и азота (она называется аденин) присоединена к молекуле рибозы (это сахар), и все это вместе крепится к хвосту из фосфатов. Из названий молекул понятно, что в хвосте АДФ содержится два фосфата, а в хвосте АТФ — три. Когда в клетке происходит химический процесс, например фотосинтез, образующаяся энергия идет на присоединение третьего фосфата к хвосту АДФ. Полученная молекула АТФ затем переносится в другие части клетки. Там запасенная энергия может быть использована в других химических процессах: она выделяется при отщеплении последнего фосфата от АТФ, в результате чего АТФ вновь превращается в АДФ.
Как мы уже упоминали, существуют и другие молекулы, которые переносят энергию в клетке. Набор таких молекул чем-то напоминает разные варианты оплаты счетов. Вы можете выбрать наличные, банковский перевод, кредитную карту и т. д. — в зависимости от того, какой способ вам удобнее. Так же и клетка для поддержания своей жизнедеятельности может использовать АТФ (эквивалент наличных денег) или любую другую из большого набора более сложных молекул.
См. также:
2.3: Биологические молекулы — Биология LibreTexts
Большие молекулы, необходимые для жизни, которые построены из более мелких органических молекул, называются биологическими макромолекулами. Существует четыре основных класса биологических макромолекул (углеводы, липиды, белки и нуклеиновые кислоты), каждый из которых является важным компонентом клетки и выполняет широкий спектр функций. Вместе эти молекулы составляют большую часть массы клетки. Биологические макромолекулы являются органическими, что означает, что они содержат углерод (за некоторыми исключениями, например, двуокись углерода).Кроме того, они могут содержать водород, кислород, азот, фосфор, серу и дополнительные второстепенные элементы.
Углерод
Часто говорят, что жизнь «основана на углероде». Это означает, что атомы углерода, связанные с другими атомами углерода или другими элементами, образуют фундаментальные компоненты многих, если не большинства, молекул, уникальных для живых существ. Другие элементы играют важную роль в биологических молекулах, но углерод определенно квалифицируется как элемент «фундамент» для молекул в живых существах.Это связывающие свойства атомов углерода, которые ответственны за его важную роль.
Углеродное соединение
Углерод содержит четыре электрона в своей внешней оболочке. Следовательно, он может образовывать четыре ковалентные связи с другими атомами или молекулами. Простейшей молекулой органического углерода является метан (CH 4 ), в котором четыре атома водорода связаны с атомом углерода (рис. 2.3.1).
Рисунок 2.3.1: Углерод может образовывать четыре ковалентные связи, образуя органическую молекулу. Самая простая молекула углерода — это метан (CH 4 ), изображенный здесь.Однако более сложные конструкции изготавливаются с использованием углерода. Любой из атомов водорода можно заменить другим атомом углерода, ковалентно связанным с первым атомом углерода. Таким образом могут быть образованы длинные и разветвленные цепи углеродных соединений (рис. 2.3.2 a ). Атомы углерода могут связываться с атомами других элементов, таких как азот, кислород и фосфор (рис. 2.3.2 b ). Молекулы также могут образовывать кольца, которые сами могут связываться с другими кольцами (рис.2.3.2 c ). Это разнообразие молекулярных форм объясняет разнообразие функций биологических макромолекул и в значительной степени основано на способности углерода образовывать множественные связи с самим собой и другими атомами.
Рис. 2.3.2: На этих примерах показаны три молекулы (обнаруженные в живых организмах), которые содержат атомы углерода, различным образом связанные с другими атомами углерода и атомами других элементов. (а) Эта молекула стеариновой кислоты имеет длинную цепочку атомов углерода. (б) Глицин, компонент белков, содержит атомы углерода, азота, кислорода и водорода.(c) Глюкоза, сахар, имеет кольцо из атомов углерода и один атом кислорода.Углеводы
Углеводы — это макромолекулы, с которыми большинство потребителей в некоторой степени знакомо. Чтобы похудеть, некоторые люди придерживаются «низкоуглеводной» диеты. Спортсмены, напротив, часто «нагружаются углеводами» перед важными соревнованиями, чтобы убедиться, что у них достаточно энергии для соревнований на высоком уровне. Фактически, углеводы являются неотъемлемой частью нашего рациона; злаки, фрукты и овощи — все это естественные источники углеводов.Углеводы обеспечивают организм энергией, особенно через глюкозу, простой сахар. Углеводы также выполняют другие важные функции у людей, животных и растений.
Углеводы можно представить формулой (CH 2 O) n , где n — количество атомов углерода в молекуле. Другими словами, соотношение углерода, водорода и кислорода в молекулах углеводов составляет 1: 2: 1. Углеводы подразделяются на три подтипа: моносахариды, дисахариды и полисахариды.
Моносахариды (моно- = «один»; sacchar- = «сладкий») представляют собой простые сахара, наиболее распространенным из которых является глюкоза. В моносахаридах количество атомов углерода обычно составляет от трех до шести. Большинство названий моносахаридов оканчиваются суффиксом -ose. В зависимости от количества атомов углерода в сахаре они могут быть известны как триозы (три атома углерода), пентозы (пять атомов углерода) и гексозы (шесть атомов углерода).
Моносахариды могут существовать в виде линейной цепи или кольцевых молекул; в водных растворах они обычно находятся в кольцевой форме.
Химическая формула глюкозы: C 6 H 12 O 6 . У большинства живых существ глюкоза является важным источником энергии. Во время клеточного дыхания из глюкозы выделяется энергия, которая используется для выработки аденозинтрифосфата (АТФ). Растения синтезируют глюкозу, используя углекислый газ и воду в процессе фотосинтеза, а глюкоза, в свою очередь, используется для удовлетворения потребностей растений в энергии. Избыток синтезированной глюкозы часто хранится в виде крахмала, который расщепляется другими организмами, которые питаются растениями.
Галактоза (входит в состав лактозы или молочного сахара) и фруктоза (содержится во фруктах) — другие распространенные моносахариды. Хотя глюкоза, галактоза и фруктоза имеют одинаковую химическую формулу (C 6 H 12 O 6 ), они отличаются структурно и химически (и известны как изомеры) из-за разного расположения атомов в углеродной цепи. (Рисунок 2.3.3).
Рис. 2.3.3. Глюкоза, галактоза и фруктоза — изомерные моносахариды, что означает, что они имеют одинаковую химическую формулу, но немного разные структуры.Дисахариды (ди- = «два») образуются, когда два моносахарида подвергаются реакции дегидратации (реакция, при которой происходит удаление молекулы воды). Во время этого процесса гидроксильная группа (–OH) одного моносахарида соединяется с атомом водорода другого моносахарида, высвобождая молекулу воды (H 2 O) и образуя ковалентную связь между атомами в двух молекулах сахара.
Обычные дисахариды включают лактозу, мальтозу и сахарозу. Лактоза — это дисахарид, состоящий из мономеров глюкозы и галактозы.Он содержится в молоке. Мальтоза, или солодовый сахар, представляет собой дисахарид, образующийся в результате реакции дегидратации между двумя молекулами глюкозы. Наиболее распространенным дисахаридом является сахароза или столовый сахар, который состоит из мономеров глюкозы и фруктозы.
Длинная цепь моносахаридов, связанных ковалентными связями, известна как полисахарид (поли- = «много»). Цепь может быть разветвленной или неразветвленной, и она может содержать разные типы моносахаридов. Полисахариды могут быть очень большими молекулами.Крахмал, гликоген, целлюлоза и хитин являются примерами полисахаридов.
Крахмал — это хранимая в растениях форма сахаров, состоящая из амилозы и амилопектина (оба полимера глюкозы). Растения способны синтезировать глюкозу, а избыток глюкозы откладывается в виде крахмала в различных частях растений, включая корни и семена. Крахмал, который потребляется животными, расщепляется на более мелкие молекулы, такие как глюкоза. Затем клетки могут поглощать глюкозу.
Гликоген — это форма хранения глюкозы у людей и других позвоночных, состоящая из мономеров глюкозы.Гликоген является животным эквивалентом крахмала и представляет собой сильно разветвленную молекулу, обычно хранящуюся в клетках печени и мышц. Когда уровень глюкозы снижается, гликоген расщепляется с высвобождением глюкозы.
Целлюлоза — один из самых распространенных природных биополимеров. Клеточные стенки растений в основном состоят из целлюлозы, которая обеспечивает структурную поддержку клетки. Дерево и бумага в основном целлюлозные по своей природе. Целлюлоза состоит из мономеров глюкозы, которые связаны связями между определенными атомами углерода в молекуле глюкозы.
Каждый второй мономер глюкозы в целлюлозе переворачивается и плотно упаковывается в виде удлиненных длинных цепей. Это придает целлюлозе жесткость и высокую прочность на разрыв, что так важно для растительных клеток. Целлюлоза, проходящая через нашу пищеварительную систему, называется пищевыми волокнами. Хотя связи глюкозы и глюкозы в целлюлозе не могут быть разрушены пищеварительными ферментами человека, травоядные животные, такие как коровы, буйволы и лошади, способны переваривать траву, богатую целлюлозой, и использовать ее в качестве источника пищи.У этих животных определенные виды бактерий обитают в рубце (часть пищеварительной системы травоядных) и секретируют фермент целлюлазу. В аппендиксе также содержатся бактерии, которые расщепляют целлюлозу, что придает ей важную роль в пищеварительной системе жвачных животных. Целлюлазы могут расщеплять целлюлозу на мономеры глюкозы, которые могут использоваться животным в качестве источника энергии.
Углеводы выполняют другие функции у разных животных. У членистоногих, таких как насекомые, пауки и крабы, есть внешний скелет, называемый экзоскелетом, который защищает их внутренние части тела.Этот экзоскелет состоит из биологической макромолекулы хитина, азотистого углевода. Он состоит из повторяющихся единиц модифицированного сахара, содержащего азот.
Таким образом, из-за различий в молекулярной структуре углеводы могут выполнять самые разные функции хранения энергии (крахмал и гликоген), а также структурной поддержки и защиты (целлюлоза и хитин) (рис. 2.3.4).
Рис. 2.3.4: Хотя их структура и функции различаются, все полисахаридные углеводы состоят из моносахаридов и имеют химическую формулу (CH 2 O) n.КАРЬЕРА В ДЕЙСТВИИ: диплом диетолог
Ожирение является проблемой здравоохранения во всем мире, и многие болезни, такие как диабет и болезни сердца, становятся все более распространенными из-за ожирения. Это одна из причин, почему к зарегистрированным диетологам все чаще обращаются за советом. Зарегистрированные диетологи помогают планировать пищевые продукты и программы питания для людей в различных условиях. Они часто работают с пациентами в медицинских учреждениях, разрабатывая планы питания для профилактики и лечения заболеваний.Например, диетологи могут научить пациента с диабетом, как контролировать уровень сахара в крови, употребляя в пищу правильные типы и количества углеводов. Диетологи также могут работать в домах престарелых, школах и частных клиниках.
Чтобы стать дипломированным диетологом, нужно получить как минимум степень бакалавра в области диетологии, питания, пищевых технологий или в смежных областях. Кроме того, дипломированные диетологи должны пройти программу стажировки под руководством и сдать национальный экзамен. Те, кто занимается диетологией, проходят курсы по питанию, химии, биохимии, биологии, микробиологии и физиологии человека.Диетологи должны стать экспертами в химии и функциях пищи (белков, углеводов и жиров).
Липиды
Липиды включают разнообразную группу соединений, объединенных общим признаком. Липиды являются гидрофобными («водобоязненными») или нерастворимыми в воде, поскольку они являются неполярными молекулами. Это потому, что они являются углеводородами, которые включают только неполярные углерод-углеродные или углерод-водородные связи. Липиды выполняют в клетке множество различных функций. Клетки хранят энергию для длительного использования в виде липидов, называемых жирами.Липиды также обеспечивают изоляцию растений и животных от окружающей среды (рис. 2.3.5). Например, они помогают водным птицам и млекопитающим оставаться сухими из-за их водоотталкивающих свойств. Липиды также являются строительными блоками многих гормонов и являются важной составляющей плазматической мембраны. Липиды включают жиры, масла, воски, фосфолипиды и стероиды.
Рисунок 2.3.5: Гидрофобные липиды в шерсти водных млекопитающих, таких как речная выдра, защищают их от непогоды. (кредит: Кен Босма)Молекула жира, такая как триглицерид, состоит из двух основных компонентов — глицерина и жирных кислот.Глицерин — это органическое соединение с тремя атомами углерода, пятью атомами водорода и тремя гидроксильными (–OH) группами. Жирные кислоты имеют длинную цепь углеводородов, к которой присоединена кислая карбоксильная группа, отсюда и название «жирная кислота». Количество атомов углерода в жирной кислоте может составлять от 4 до 36; наиболее распространены те, которые содержат 12–18 атомов углерода. В молекуле жира жирная кислота присоединена к каждому из трех атомов кислорода в -ОН-группах молекулы глицерина ковалентной связью (рис. 2.3.6).
Рисунок 2.3.6: Липиды включают жиры, такие как триглицериды, которые состоят из жирных кислот и глицерина, фосфолипидов и стероидов.Во время образования этой ковалентной связи высвобождаются три молекулы воды. Три жирные кислоты в жире могут быть похожими или разными. Эти жиры также называют триглицеридами, потому что они содержат три жирные кислоты. Некоторые жирные кислоты имеют общие названия, указывающие на их происхождение. Например, пальмитиновая кислота, насыщенная жирная кислота, получают из пальмы.Арахидовая кислота получена из Arachis hypogaea , научного названия арахиса.
Жирные кислоты могут быть насыщенными и ненасыщенными. В цепи жирной кислоты, если есть только одинарные связи между соседними атомами углерода в углеводородной цепи, жирная кислота является насыщенной. Насыщенные жирные кислоты насыщены водородом; другими словами, количество атомов водорода, прикрепленных к углеродному скелету, максимально.
Когда углеводородная цепь содержит двойную связь, жирная кислота является ненасыщенной жирной кислотой.
Большинство ненасыщенных жиров являются жидкими при комнатной температуре и называются маслами. Если в молекуле есть одна двойная связь, то он известен как мононенасыщенный жир (например, оливковое масло), а если имеется более одной двойной связи, то он известен как полиненасыщенный жир (например, масло канолы).
Насыщенные жиры плотно упаковываются и остаются твердыми при комнатной температуре. Животные жиры со стеариновой кислотой и пальмитиновой кислотой, содержащиеся в мясе, и жир с масляной кислотой, содержащиеся в масле, являются примерами насыщенных жиров.Млекопитающие хранят жиры в специализированных клетках, называемых адипоцитами, где жировые шарики занимают большую часть клетки. У растений жир или масло хранятся в семенах и используются в качестве источника энергии во время эмбрионального развития.
Ненасыщенные жиры или масла обычно растительного происхождения и содержат ненасыщенные жирные кислоты. Двойная связь вызывает изгиб или «перегиб», который препятствует плотной упаковке жирных кислот, сохраняя их в жидком состоянии при комнатной температуре. Оливковое масло, кукурузное масло, масло канолы и жир печени трески являются примерами ненасыщенных жиров.Ненасыщенные жиры помогают повысить уровень холестерина в крови, тогда как насыщенные жиры способствуют образованию бляшек в артериях, что увеличивает риск сердечного приступа.
В пищевой промышленности масла искусственно гидрогенизируются для придания им полутвердого состояния, что приводит к меньшей порче и увеличению срока хранения. Проще говоря, газообразный водород пропускают через масла, чтобы отвердить их. Во время этого процесса гидрирования двойные связи цис -конформации в углеводородной цепи могут быть преобразованы в двойные связи в транс -конформации.Это образует транс- -жир из цис- -жира. Ориентация двойных связей влияет на химические свойства жира (рис. 2.3.7).
Рисунок 2.3.7: В процессе гидрогенизации ориентация двойных связей изменяется, в результате чего из цис-жира образуется транс-жир. Это изменяет химические свойства молекулы.Маргарин, некоторые виды арахисового масла и шортенинг являются примерами искусственно гидрогенизированных трансжиров транс . Недавние исследования показали, что увеличение транс -жиров в рационе человека может привести к увеличению уровня липопротеинов низкой плотности (ЛПНП) или «плохого» холестерина, что, в свою очередь, может привести к отложению бляшек в организме человека. артерии, что приводит к болезни сердца.Многие рестораны быстрого питания недавно отказались от использования жиров транс и , а на этикетках пищевых продуктов в США теперь требуется указывать содержание жира транс .
Незаменимые жирные кислоты — это жирные кислоты, которые необходимы, но не синтезируются человеческим организмом. Следовательно, их необходимо дополнять с помощью диеты. Омега-3 жирные кислоты попадают в эту категорию и являются одной из двух известных незаменимых жирных кислот для человека (другая — омега-6 жирные кислоты). Они представляют собой тип полиненасыщенных жиров и называются омега-3 жирными кислотами, потому что третий углерод на конце жирной кислоты участвует в двойной связи.
Лосось, форель и тунец являются хорошими источниками жирных кислот омега-3. Жирные кислоты омега-3 важны для работы мозга, нормального роста и развития. Они также могут предотвратить сердечные заболевания и снизить риск рака.
Как и углеводы, жиры получили широкую огласку. Это правда, что чрезмерное употребление жареной и другой «жирной» пищи приводит к увеличению веса. Однако жиры выполняют важные функции. Жиры служат долгосрочным накопителем энергии. Они также обеспечивают изоляцию тела.Поэтому «здоровые» ненасыщенные жиры в умеренных количествах следует употреблять регулярно.
Фосфолипиды являются основным компонентом плазматической мембраны. Как и жиры, они состоят из цепей жирных кислот, прикрепленных к глицерину или подобной основной цепи. Однако вместо трех жирных кислот есть две жирные кислоты, а третий углерод глицериновой цепи связан с фосфатной группой. Фосфатная группа модифицируется добавлением спирта.
Фосфолипид имеет как гидрофобные, так и гидрофильные участки.Цепи жирных кислот гидрофобны и исключаются из воды, тогда как фосфат гидрофильный и взаимодействует с водой.
Клетки окружены мембраной, которая имеет бислой фосфолипидов. Жирные кислоты фосфолипидов обращены внутрь, вдали от воды, тогда как фосфатная группа может быть обращена либо к внешней среде, либо к внутренней части клетки, которые оба являются водными.
Стероиды и воски
В отличие от фосфолипидов и жиров, рассмотренных ранее, стероиды имеют кольцевую структуру.Хотя они не похожи на другие липиды, они сгруппированы с ними, потому что они также гидрофобны. Все стероиды имеют четыре связанных углеродных кольца, а некоторые из них, как и холестерин, имеют короткий хвост.
Холестерин — стероид. Холестерин в основном синтезируется в печени и является предшественником многих стероидных гормонов, таких как тестостерон и эстрадиол. Он также является предшественником витаминов Е и К. Холестерин является предшественником солей желчных кислот, которые помогают в расщеплении жиров и их последующем усвоении клетками.Хотя о холестерине часто говорят отрицательно, он необходим для правильного функционирования организма. Это ключевой компонент плазматических мембран клеток животных.
Воски состоят из углеводородной цепи со спиртовой (–OH) группой и жирной кислотой. Примеры восков животного происхождения включают пчелиный воск и ланолин. У растений также есть воск, например покрытие на листьях, которое помогает предотвратить их высыхание.
КОНЦЕПЦИЯ В ДЕЙСТВИИ
Чтобы получить дополнительную информацию о липидах, исследуйте «Биомолекулы: Липиды» с помощью этой интерактивной анимации.
Белки
Белки являются одними из наиболее распространенных органических молекул в живых системах и обладают самым разнообразным набором функций среди всех макромолекул. Белки могут быть структурными, регуляторными, сократительными или защитными; они могут служить для транспортировки, хранения или перепонки; или они могут быть токсинами или ферментами. Каждая клетка живой системы может содержать тысячи различных белков, каждый из которых выполняет уникальную функцию. Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры аминокислот, расположенных в линейной последовательности.
Функции белков очень разнообразны, потому что существует 20 различных химически различных аминокислот, которые образуют длинные цепи, и аминокислоты могут располагаться в любом порядке. Например, белки могут функционировать как ферменты или гормоны. Ферменты, которые вырабатываются живыми клетками, являются катализаторами биохимических реакций (например, пищеварения) и обычно являются белками. Каждый фермент специфичен для субстрата (реагента, который связывается с ферментом), на который он действует. Ферменты могут разрушать молекулярные связи, переупорядочивать связи или образовывать новые связи.Примером фермента является амилаза слюны, которая расщепляет амилозу, компонент крахмала.
Гормоны — это химические сигнальные молекулы, обычно белки или стероиды, секретируемые эндокринной железой или группой эндокринных клеток, которые контролируют или регулируют определенные физиологические процессы, включая рост, развитие, метаболизм и размножение. Например, инсулин — это белковый гормон, который поддерживает уровень глюкозы в крови.
Белки имеют разную форму и молекулярную массу; некоторые белки имеют глобулярную форму, тогда как другие имеют волокнистую природу.Например, гемоглобин — это глобулярный белок, а коллаген, обнаруженный в нашей коже, — это волокнистый белок. Форма белка имеет решающее значение для его функции. Изменения температуры, pH и воздействие химикатов могут привести к необратимым изменениям формы белка, что приведет к потере функции или денатурации (более подробно это будет обсуждаться позже). Все белки состоят из 20 одних и тех же аминокислот по-разному.
Аминокислоты — это мономеры, из которых состоят белки. Каждая аминокислота имеет одинаковую фундаментальную структуру, которая состоит из центрального атома углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группы (–COOH) и атома водорода.Каждая аминокислота также имеет другой вариабельный атом или группу атомов, связанных с центральным атомом углерода, известную как группа R. Группа R — единственное различие в структуре между 20 аминокислотами; в остальном аминокислоты идентичны (рис. 2.3.8).
Рисунок 2.3.8: Аминокислоты состоят из центрального углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группой (–COOH) и атомом водорода. Четвертая связь центрального углерода варьируется среди различных аминокислот, как видно из этих примеров аланина, валина, лизина и аспарагиновой кислоты.Химическая природа группы R определяет химическую природу аминокислоты в ее белке (то есть, является ли она кислотной, основной, полярной или неполярной).
Последовательность и количество аминокислот в конечном итоге определяют форму, размер и функцию белка. Каждая аминокислота присоединена к другой аминокислоте ковалентной связью, известной как пептидная связь, которая образуется в результате реакции дегидратации. Карбоксильная группа одной аминокислоты и аминогруппа второй аминокислоты объединяются, высвобождая молекулу воды.Полученная связь представляет собой пептидную связь.
Продукты, образованные такой связью, называются полипептидами. Хотя термины полипептид и белок иногда используются как взаимозаменяемые, полипептид технически представляет собой полимер аминокислот, тогда как термин белок используется для полипептида или полипептидов, которые объединились вместе, имеют различную форму и имеют уникальную функцию.
ЭВОЛЮЦИЯ В ДЕЙСТВИИ: Эволюционное значение цитохрома c
Цитохром c — важный компонент молекулярного механизма, который извлекает энергию из глюкозы.Поскольку роль этого белка в производстве клеточной энергии имеет решающее значение, за миллионы лет он очень мало изменился. Секвенирование белков показало, что существует значительное сходство последовательностей между молекулами цитохрома с разных видов; эволюционные отношения можно оценить путем измерения сходства или различий между белковыми последовательностями различных видов.
Например, ученые определили, что цитохром с человека содержит 104 аминокислоты. Для каждой молекулы цитохрома с, которая к настоящему времени была секвенирована у разных организмов, 37 из этих аминокислот находятся в одном и том же положении в каждом цитохроме с.Это указывает на то, что все эти организмы произошли от общего предка. При сравнении последовательностей белков человека и шимпанзе различий в последовательностях не обнаружено. При сравнении последовательностей человека и макаки-резуса было обнаружено единственное различие в одной аминокислоте. Напротив, сравнение человека с дрожжами показывает разницу в 44 аминокислотах, предполагая, что люди и шимпанзе имеют более недавнего общего предка, чем люди и макака-резус или люди и дрожжи.
Структура белка
Как обсуждалось ранее, форма белка имеет решающее значение для его функции.Чтобы понять, как белок приобретает свою окончательную форму или конформацию, нам необходимо понять четыре уровня структуры белка: первичный, вторичный, третичный и четвертичный (рис. 2.3.9).
Уникальная последовательность и количество аминокислот в полипептидной цепи — это ее первичная структура. Уникальная последовательность каждого белка в конечном итоге определяется геном, кодирующим этот белок. Любое изменение в последовательности гена может привести к добавлению другой аминокислоты к полипептидной цепи, вызывая изменение структуры и функции белка.При серповидно-клеточной анемии β-цепь гемоглобина имеет единственную аминокислотную замену, вызывающую изменение как структуры, так и функции белка. Что наиболее примечательно, так это то, что молекула гемоглобина состоит из двух альфа-цепей и двух бета-цепей, каждая из которых состоит примерно из 150 аминокислот. Таким образом, молекула содержит около 600 аминокислот. Структурная разница между нормальной молекулой гемоглобина и молекулой серповидных клеток, которая резко снижает продолжительность жизни у пораженных людей, состоит в одной из 600 аминокислот.
Из-за этого изменения одной аминокислоты в цепи обычно двояковогнутые или дискообразные эритроциты принимают форму полумесяца или «серпа», что закупоривает артерии. Это может привести к множеству серьезных проблем со здоровьем, таких как одышка, головокружение, головные боли и боли в животе у людей, страдающих этим заболеванием.
Паттерны сворачивания, возникающие в результате взаимодействий между частями аминокислот, не относящихся к R-группам, приводят к вторичной структуре белка. Наиболее распространены альфа (α) -спиральные и бета (β) -пластинчатые листовые структуры.Обе структуры удерживаются в форме водородными связями. В альфа-спирали связи образуются между каждой четвертой аминокислотой и вызывают поворот аминокислотной цепи.
В β-складчатом листе «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи. Группы R прикреплены к атомам углерода и проходят выше и ниже складок складки. Гофрированные сегменты выровнены параллельно друг другу, а водородные связи образуются между одинаковыми парами атомов на каждой из выровненных аминокислот.Структуры α-спирали и β-складчатых листов обнаруживаются во многих глобулярных и волокнистых белках.
Уникальная трехмерная структура полипептида известна как его третичная структура. Эта структура вызвана химическим взаимодействием между различными аминокислотами и участками полипептида. Прежде всего, взаимодействия между группами R создают сложную трехмерную третичную структуру белка. Могут быть ионные связи, образованные между группами R на разных аминокислотах, или водородные связи, помимо тех, которые участвуют во вторичной структуре.Когда происходит сворачивание белка, гидрофобные группы R неполярных аминокислот лежат внутри белка, тогда как гидрофильные группы R лежат снаружи. Первые типы взаимодействий также известны как гидрофобные взаимодействия.
В природе некоторые белки образованы из нескольких полипептидов, также известных как субъединицы, и взаимодействие этих субъединиц образует четвертичную структуру. Слабые взаимодействия между субъединицами помогают стабилизировать общую структуру.Например, гемоглобин представляет собой комбинацию четырех полипептидных субъединиц.
Рисунок 2.3.9: На этих иллюстрациях можно увидеть четыре уровня структуры белка. (кредит: модификация работы Национального института исследования генома человека)Каждый белок имеет свою уникальную последовательность и форму, которые удерживаются вместе за счет химических взаимодействий. Если белок подвержен изменениям температуры, pH или воздействию химикатов, структура белка может измениться, потеряв свою форму в результате так называемой денатурации, как обсуждалось ранее.Денатурация часто обратима, поскольку первичная структура сохраняется, если денатурирующий агент удаляется, позволяя белку возобновить свою функцию. Иногда денатурация необратима, что приводит к потере функции. Один из примеров денатурации белка можно увидеть, когда яйцо жарят или варят. Белок альбумина в жидком яичном белке денатурируется при помещении на горячую сковороду, превращаясь из прозрачного вещества в непрозрачное белое вещество. Не все белки денатурируются при высоких температурах; например, бактерии, которые выживают в горячих источниках, имеют белки, которые адаптированы для работы при этих температурах.
КОНЦЕПЦИЯ В ДЕЙСТВИИ
Чтобы получить дополнительную информацию о белках, исследуйте «Биомолекулы: Белки» с помощью этой интерактивной анимации.
нуклеиновые кислоты
Нуклеиновые кислоты являются ключевыми макромолекулами в непрерывности жизни. Они несут генетический план клетки и несут инструкции для функционирования клетки.
Двумя основными типами нуклеиновых кислот являются дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК). ДНК — это генетический материал, содержащийся во всех живых организмах, от одноклеточных бактерий до многоклеточных млекопитающих.
Другой тип нуклеиновой кислоты, РНК, в основном участвует в синтезе белка. Молекулы ДНК никогда не покидают ядро, а вместо этого используют посредника РНК для связи с остальной частью клетки. Другие типы РНК также участвуют в синтезе белка и его регуляции.
ДНК и РНК состоят из мономеров, известных как нуклеотиды. Нуклеотиды объединяются друг с другом с образованием полинуклеотида, ДНК или РНК. Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозного (пятиуглеродного) сахара и фосфатной группы (Рисунок 2.3.10). Каждое азотистое основание в нуклеотиде присоединено к молекуле сахара, которая присоединена к фосфатной группе.
Рисунок 2.3.10: Нуклеотид состоит из трех компонентов: азотистого основания, пентозного сахара и фосфатной группы.Двойная спиральная структура ДНК
ДНКимеет двойную спиральную структуру (рис. 2.3.11). Он состоит из двух цепей или полимеров нуклеотидов. Нити образованы связями между фосфатными и сахарными группами соседних нуклеотидов.Нити связаны друг с другом в своих основаниях водородными связями, и нити наматываются друг на друга по своей длине, отсюда и описание «двойной спирали», что означает двойную спираль.
Рисунок 2.3.11: Модель двойной спирали показывает ДНК как две параллельные нити переплетающихся молекул. (кредит: Джером Уокер, Деннис Митс)Чередующиеся сахарные и фосфатные группы лежат на внешней стороне каждой цепи, образуя основу ДНК. Азотистые основания сложены внутри, как ступени лестницы, и эти основания соединяются в пару; пары связаны друг с другом водородными связями.Основания спариваются таким образом, чтобы расстояние между скелетами двух цепей было одинаковым по всей длине молекулы.
Сводка
Живые существа основаны на углероде, потому что углерод играет такую важную роль в химии живых существ. Четыре позиции ковалентной связи атома углерода могут дать начало широкому разнообразию соединений с множеством функций, что объясняет важность углерода для живых существ. Углеводы — это группа макромолекул, которые являются жизненно важным источником энергии для клетки, обеспечивают структурную поддержку многих организмов и могут быть обнаружены на поверхности клетки в качестве рецепторов или для распознавания клеток.Углеводы классифицируются как моносахариды, дисахариды и полисахариды, в зависимости от количества мономеров в молекуле.
Липиды — это класс макромолекул, которые по своей природе неполярны и гидрофобны. Основные типы включают жиры и масла, воски, фосфолипиды и стероиды. Жиры и масла представляют собой запасенную форму энергии и могут включать триглицериды. Жиры и масла обычно состоят из жирных кислот и глицерина.
Белки — это класс макромолекул, которые могут выполнять широкий спектр функций для клетки.Они помогают метаболизму, обеспечивая структурную поддержку и действуя как ферменты, переносчики или гормоны. Строительными блоками белков являются аминокислоты. Белки организованы на четырех уровнях: первичный, вторичный, третичный и четвертичный. Форма и функция белка неразрывно связаны; любое изменение формы, вызванное изменениями температуры, pH или химического воздействия, может привести к денатурации белка и потере функции.
Нуклеиновые кислоты — это молекулы, состоящие из повторяющихся единиц нуклеотидов, которые направляют клеточную деятельность, такую как деление клеток и синтез белка.Каждый нуклеотид состоит из пентозного сахара, азотистого основания и фосфатной группы. Есть два типа нуклеиновых кислот: ДНК и РНК.
Глоссарий
- аминокислота
- мономер протеина
- углевод
- — биологическая макромолекула, в которой отношение углерода к водороду к кислороду составляет 1: 2: 1; углеводы служат источниками энергии и структурной поддержкой в клетках
- целлюлоза
- полисахарид, который составляет клеточные стенки растений и обеспечивает структурную поддержку клетки
- хитин
- вид углеводов, образующих внешний скелет членистоногих, таких как насекомые и ракообразные, и клеточные стенки грибов
- денатурация
- потеря формы белка в результате изменений температуры, pH или воздействия химических веществ
- дезоксирибонуклеиновая кислота (ДНК)
- двухцепочечный полимер нуклеотидов, несущий наследственную информацию клетки
- дисахарид
- два мономера сахара, которые связаны между собой пептидной связью
- фермент
- катализатор биохимической реакции, который обычно представляет собой сложный или конъюгированный белок
- жир
- молекула липида, состоящая из трех жирных кислот и глицерина (триглицерида), которая обычно существует в твердой форме при комнатной температуре
- гликоген
- запасной углевод у животных
- гормон
- химическая сигнальная молекула, обычно белок или стероид, секретируемая эндокринной железой или группой эндокринных клеток; действия по контролю или регулированию определенных физиологических процессов
- липиды
- — класс неполярных и нерастворимых в воде макромолекул
- макромолекула
- большая молекула, часто образованная полимеризацией более мелких мономеров
- моносахарид
- одно звено или мономер углеводов
- нуклеиновая кислота
- биологическая макромолекула, которая несет генетическую информацию клетки и несет инструкции для функционирования клетки
- нуклеотид
- мономер нуклеиновых кислот; содержит пентозный сахар, фосфатную группу и азотистое основание
- масло
- ненасыщенный жир, являющийся жидкостью при комнатной температуре
- фосфолипид
- основной компонент мембран клеток; состоит из двух жирных кислот и фосфатной группы, присоединенной к основной цепи глицерина
- полипептид
- длинная цепь аминокислот, связанных пептидными связями
- полисахарид
- длинная цепь моносахаридов; могут быть разветвленными и неразветвленными
- белок
- биологическая макромолекула, состоящая из одной или нескольких цепочек аминокислот
- рибонуклеиновая кислота (РНК)
- одноцепочечный полимер нуклеотидов, участвующий в синтезе белка
- насыщенная жирная кислота
- длинноцепочечный углеводород с одинарными ковалентными связями в углеродной цепи; количество атомов водорода, прикрепленных к углеродному скелету, максимально
- крахмал
- запасной углевод в растениях
- стероид
- Тип липида, состоящего из четырех конденсированных углеводородных колец
- транс жир
- форма ненасыщенного жира с атомами водорода, соседствующими с двойной связью, напротив друг друга, а не на одной стороне двойной связи
- триглицерид
- молекула жира; состоит из трех жирных кислот, связанных с молекулой глицерина
- ненасыщенная жирная кислота
- длинноцепочечный углеводород, который имеет одну или несколько двойных связей в углеводородной цепи
Авторы и авторство
ДНК: Рецепт человеческого тела — Урок
(0 оценок) Спасибо за оценку!Быстрый просмотр
Уровень оценки: 6 (5-7)
Требуемое время: 15 минут
Зависимость урока: Нет
Тематические области: Биология, науки о жизни, наука и технологии
Ожидаемые характеристики NGSS:
Резюме
В классе учащиеся работают над примером, показывающим, как ДНК обеспечивает «рецепт» создания белков человеческого тела.Они видят, как структура нуклеотидных оснований (аденин, тимин, гуанин, цитозин) образует двойную спиральную лестницу ДНК и служит кодом для шагов, необходимых для создания генов. Студенты расширяют свои знания, проводя соответствующие мероприятия, чтобы узнать, как инженеры и ученые применяют свое понимание ДНК в нашем мире. Данная инженерная программа соответствует научным стандартам нового поколения (NGSS).Инженерное соединение
Когда было обнаружено, что ДНК содержит инструкции по созданию клеток и белков, открылся путь для множества различных инженерных приложений.Генные инженеры находят способы модифицировать ДНК организмов, чтобы создать желаемый признак или белок, например, сделать урожай устойчивым к определенному гербициду или создать бактерии, которые создают человеческий инсулин. Судебные инженеры используют доказательства ДНК, чтобы помочь определить невиновность или виновность людей в совершении преступлений. Инженеры-агрономы создают генетически модифицированные культуры, позволяющие выращивать продукты питания в районах, плохо подходящих для ведения сельского хозяйства.
Цели обучения
После этого урока учащиеся должны уметь:
- Опишите ДНК (дезоксирибонуклеиновая кислота).
- Опишите способы взаимодействия инженеров с генетикой и человеческим телом.
Образовательные стандарты
Каждый урок или задание TeachEngineering соотносится с одним или несколькими научными дисциплинами K-12, образовательные стандарты в области технологий, инженерии или математики (STEM).
Все 100000+ стандартов K-12 STEM, охватываемых TeachEngineering , собираются, обслуживаются и упаковываются сетью стандартов достижений (ASN) , проект D2L (www.achievementstandards.org).
В ASN стандарты иерархически структурированы: сначала по источникам; например , по штатам; внутри источника по типу; например , естественные науки или математика; внутри типа по подтипу, затем по классу, и т. д. .
NGSS: научные стандарты нового поколения — наука| Ожидаемые характеристики NGSS | ||
|---|---|---|
МС-LS1-3.Используйте аргумент, подтвержденный доказательствами того, что тело представляет собой систему взаимодействующих подсистем, состоящих из групп клеток. (6-8 классы) Вы согласны с таким раскладом? Спасибо за ваш отзыв! | ||
| Нажмите, чтобы просмотреть другие учебные программы, соответствующие этим ожиданиям от результатов. | ||
| Этот урок посвящен следующим аспектам трехмерного обучения NGSS: | ||
| Наука и инженерная практика | Основные дисциплинарные идеи | Пересекающиеся концепции |
| Используйте устные и письменные аргументы, подкрепленные доказательствами, чтобы поддержать или опровергнуть объяснение или модель явления. Соглашение о выравнивании: Спасибо за ваш отзыв! | У многоклеточных организмов тело представляет собой систему множества взаимодействующих подсистем. Эти подсистемы представляют собой группы клеток, которые работают вместе, чтобы сформировать ткани и органы, которые специализируются на определенных функциях организма. Соглашение о выравнивании: Спасибо за ваш отзыв! | Системы могут взаимодействовать с другими системами; они могут иметь подсистемы и быть частью более крупных сложных систем. Соглашение о выравнивании: Спасибо за ваш отзыв! Ученые и инженеры руководствуются такими привычками ума, как интеллектуальная честность, терпимость к двусмысленности, скептицизм и открытость новым идеям.Соглашение о выравнивании: Спасибо за ваш отзыв! |
- Достижения и инновации в медицинских технологиях используются для улучшения здравоохранения.(Оценки
6 —
8) Подробнее
Посмотреть согласованную учебную программу
Вы согласны с таким раскладом? Спасибо за ваш отзыв!
- Генная инженерия включает изменение структуры ДНК для создания новых генетических моделей.(Оценки
6 —
8) Подробнее
Посмотреть согласованную учебную программу
Вы согласны с таким раскладом? Спасибо за ваш отзыв!
Какое альтернативное выравнивание вы предлагаете для этого контента?
Больше подобной программы
Все виды мутаций: изменения генетического кодаУчащиеся узнают о мутациях ДНК и хромосом, а также о неконтролируемых изменениях генетического кода.Они вводятся в мелкомасштабные мутации (замены, делеции и вставки) и крупномасштабные мутации (делеционные дупликации, инверсии, вставки, транслокации и нерасхождение …
ДНК, сборкаСтуденты укрепляют свои знания о том, что ДНК является генетическим материалом для всех живых существ, моделируя его с помощью зубочисток и мармеладных конфет, которые представляют четыре биохимических вещества (аденин, тиамин, гуанин и цитозин), которые соединяются друг с другом по определенному образцу, образуя двойную спираль. .Студенческие отряды …
Введение в генную инженерию и ее приложенияСтуденты узнают, как инженеры применяют свое понимание ДНК для манипулирования определенными генами для получения желаемых характеристик, и как инженеры использовали эту практику для решения текущих проблем, с которыми сталкивается человечество.Учащиеся заполняют блок-схему, в которой перечислены методы модификации генов для создания ГМО и пример …
Визуализация структуры ДНКСтуденты знакомятся с новейшими методами визуализации, используемыми для визуализации молекулярных структур, и методом электрофореза, который используется для идентификации и сравнения генетического кода (ДНК).
Введение / Мотивация
Что вам понадобится, если вы хотите испечь партию шоколадного печенья? Возможно, вам понадобится шоколадная стружка, мука, сахар, масло и яйца. И, может быть, орехи или овсяные хлопья, если хочешь. Но как вы знаете, как это сделать? По рецепту! Рецепт содержит инструкции, как соединить все ингредиенты, чтобы приготовить печенье.
Теперь предположим, что вместо печенья с шоколадной крошкой вы хотели сделать человека! Что вам нужно? (Напишите на доске «список ингредиентов», составленный учащимися; он может содержать: отец [сперма], мать [яйцо], матка, пища, белки, кости, мышцы, органы, воздух, вода, элементы, минералы. и т. д.) (После того, как список будет составлен, задайте учащимся следующий вопрос.) А где рецепт, который говорит нам, как объединить все ингредиенты, чтобы получился человек? (Примите предложения студентов.) Правильно, наша ДНК содержит рецепт создания клеток и белков в нашем организме.
Рис. 1. ДНК представляет собой двойную спираль, образованную парами оснований, прикрепленными к сахарно-фосфатному остову. Авторское право
Авторские права © Национальная медицинская библиотека США, Национальные институты здравоохранения http://ghr.nlm.nih.gov/handbook/illustrations / дна
ДНК означает дезоксирибонуклеиновую кислоту . ДНК — это пара молекул, обычно встречающихся в ядре каждой клетки, которая содержит коды (рецепт) белков, из которых состоят ткани нашего тела (покажите учащимся рис. 1 или аналогичное представление ДНК).
ДНК состоит из двух длинных молекул, связанных водородными связями между парами оснований. (Водородная связь — это межмолекулярная сила, вызванная отталкиванием электрона водорода одним основанием [придающим водороду положительный заряд] и отрицательным зарядом другого основания поблизости). Пары оснований — аденин (A), связанный с тимином (T), и цитозин (C), связанный с гуанином (G), — образуют код по всей длине ДНК.
Порядок нуклеотидных оснований формирует код, который определяет, какие белки производят наши клетки, и, следовательно, сообщает нашим клеткам, что им делать.Представьте себе, что ДНК раскручивается (см. Рис. 1) и раскладывается так, чтобы мы могли видеть порядок нуклеотидных оснований. Запишем для примера порядок нуклеотидных оснований. (Напишите на доске следующее.)
Обратите внимание, как нуклеотидные основания сопоставляются с образованием пар оснований. Эти пары — настоящий рецепт для приготовления белков. (Чтобы узнать больше о производстве белков или синтезе белков, см. Пример в разделе «Предпосылки урока».)
Теперь, когда вы понимаете, что ДНК содержит инструкции, давайте поговорим о генах.Ген — это сегмент ДНК, который транслируется в белок. Гены чаще рассматриваются как единицы наследственности, такие как ген карих глаз или гены, ответственные за высокий рост или высокое кровяное давление. ДНК и, следовательно, гены передаются от отца к его потомству через его сперму и от матери к ее потомству через ее яйцеклетку. У детей 50-50 ДНК родителей. У человека около 25 000 генов. Любым двум людям, хотя они выглядят по-разному и могут быть из разных концов света, исполнилось 99 лет.9% похожи по своим генам. Наш генетический состав на 98% такой же, как у шимпанзе, на 92% такой же, как у мышей, и на 18% такой же, как у сорняков. Ясно, что крошечные различия в наших генах могут вызвать огромные физические различия!
Наше растущее понимание генетики привело к появлению множества разнообразных инженерных приложений, включая способы улучшения сельскохозяйственных культур, поимки преступников, выявления болезней и определения отцовства и происхождения. Для множества различных приложений инженеры разрабатывают инструменты, оборудование и процессы для сбора и анализа ДНК.Биомедицинские инженеры, специализирующиеся в области генетики, находят способы модифицировать ДНК организмов для создания желаемого признака или белка (например, создания бактерий, которые создают человеческий инсулин).
Так же, как дети наследуют цвет волос или глаз от родителей, они также могут унаследовать генетические заболевания. Медицинский анализ ДНК дал возможность точно определить причину генетического заболевания человека и выявить людей, предрасположенных к наследственным заболеваниям (например, генетическим заболеваниям печени). Современная медицина не может предотвратить наследственные заболевания, но часто может улучшить здоровье и продолжительность жизни человека с помощью инженерных методов лечения.
Прорыв в ДНК позволил разработать методы и инструменты для быстрого обнаружения и выявления вспышек инфекционных заболеваний, таких как тяжелый острый респираторный синдром (вирус SARS). Биомедицинские инженеры помогают практикующим специалистам в области общественного здравоохранения отслеживать источник вспышек инфекционных заболеваний, будь то естественные или человеческие источники, что спасает множество жизней. См. Анализ ДНК и CODIS: Кто ограбил банк? задание, чтобы учащиеся использовали профили ДНК для раскрытия загадочных дел! Затем попросите учащихся расширить свои знания с помощью упражнения «Создание ДНК», построив модели ДНК для исследования кодов, относящихся к определенным физическим характеристикам, таким как цвет глаз и волос.
Предпосылки и концепции урока для учителей
Исследование генетики
Грегор Мендель (1822-84) был первым ученым, изучившим генетику путем изучения гороха. Он использовал растения гороха, потому что их легко перекрестно опылять, и они быстро заметили изменения в растениях. Он изучил некоторые характеристики растений гороха, такие как высота. Он заметил, что путем перекрестного опыления коротких и высоких растений он мог получить определенное количество высоких растений и определенное количество мелких растений, в зависимости от поколения.Сравнивая свое исследование гороха с людьми, он обнаружил, что каждая горошина получила свои черты от своих родительских растений. Мендель придумал принципы, которые верны и сегодня.
Наука генетики
Клетки есть во всех живых существах, и в каждой клетке содержится ядро. В ядре находится генетическая информация в виде хромосом, из которых состоят цепи ДНК. В среднем человеческая клетка состоит из 46 хромосом. Двадцать три хромосомы состоят из 23 пар. Эритроциты, сперма и яйцеклетки — единственные клетки в организме человека, которых нет 46.При репродукции человека сперматозоид соединяется с яйцеклеткой, образуя зиготу, в которой есть хромосомы, состоящие из генов, которые определяют, как будет выглядеть ребенок.
, авторское право
Авторское право © 1997 Программа по геному человека, Министерство энергетики США, Отчет программы по геному человека http://genomics.energy.gov
Белок — важный компонент в организме; это строительный блок всего в теле. Белок производится по «рецепту», содержащемуся в гене. Ген состоит из ДНК. ДНК организована по особому шаблону, в котором содержится рецепт создания генов.Каждая нить ДНК уникальна для человека, от которого она находится. Рецепт известен как код ДНК. Некоторые люди представляют нить ДНК как лестницу, каждая ступенька которой состоит из пары букв ДНК, представляющих нуклеотидные основания. Буквы — A, T, G и C, причем A связывается только с T, а G — только с C. Связывание этих букв образует связи пары оснований в форме двойной спирали.
Синтез белка
Синтез белка — это то, как фрагмент ДНК обеспечивает код для производства белков.В ядре клетки белок, называемый полимеразой РНК (рибонуклеиновой кислоты), прикрепляется к цепи ДНК, растягивает ее и разделяет ее часть:
Теперь РНК-полимераза перемещается по этой цепи и использует эти основания в качестве шаблона для создания мРНК (информационной РНК). Ее называют информационной РНК, потому что она передает сообщение, закодированное этими основаниями, рибосомам за пределами ядра клетки.
Обратите внимание, что мРНК является копией цепи 2 ДНК, за исключением того, что урацил (U), другое нуклеотидное основание, заменяет тимин (T) в мРНК.По мере образования мРНК РНК-полимераза повторно присоединяет цепь ДНК 1 и цепь ДНК 2.
мРНК перемещается за пределы ядра клетки в цитоплазму клетки, а затем прикрепляется к рибосомам, которые представляют собой белки, которые можно рассматривать как фабрики белков клетки. Рибосома считывает мРНК в наборах из трех оснований, называемых кодонами. Кодоны определяют, какие аминокислоты, строительные блоки белков, образуются. В нашем примере рибосома перемещается вниз по ДНК в несколько этапов, создавая белок, определяемый аминокислотами, которые требуются для каждого кодона:
Шаг 1 : Рибосома считывает кодон AUG , что означает Start Translation (начало производства белка).
Шаг 2 : Рибосома считывает кодон UGC , что означает превращение аминокислоты в цистеин .
Шаг 3 : Рибосома считывает кодон CUC , что означает превращение аминокислоты в лейцин .
Шаг 4 : Рибосома считывает кодон UAG , что означает Конечная трансляция .
(См. Полный список кодонов и аминокислот, которые они указывают, в таблице кодонов РНК Википедии по адресу http: // en.wikipedia.org/wiki/Codon.)
Белок, полученный в нашем примере, на самом деле не существует; он просто показывает, как ДНК содержит коды, необходимые для синтеза белка, и как осуществляется синтез белка. Примером настоящего белка, кодируемого ДНК, является гормон инсулин, который контролирует концентрацию глюкозы в нашей крови. Инсулин состоит из 51 аминокислоты.
Итак, ДНК содержит коды нуклеотидных оснований, которые транскрибируются РНК-полимеразой для образования мРНК, которая переносит код из ядра клетки в рибосомы в цитоплазме.Рибосомы переводят кодоны в мРНК, чтобы образовать аминокислотные цепи, которые становятся белками. Эти белки регулируют функции нашего тела и развитие.
Сопутствующие мероприятия
Закрытие урока
Расскажите, что вы знаете о ДНК. (Ожидаемые ответы: ДНК находится в ядре наших клеток. Это похоже на рецепт. Она имеет форму лестницы с двойной спиралью. Основа состоит из дезоксирибозы, фосфата сахара, а ступеньки лестницы являются нуклеотидными основаниями.Нуклеотидные основания — это коды белков, производимых нашими клетками. Ген — это сегмент ДНК, который транслируется в белок.)
Как ученые и инженеры используют свое понимание ДНК? (Возможные ответы: для выявления наследственных заболеваний у людей; для выявления инфекционных заболеваний и отслеживания их источников; для диагностики, лечения и [возможно] профилактики таких заболеваний человека, как рак, муковисцидоз и болезни сердца; для изменения организмов по желаемому признаку. или белка; для улучшения урожая; для поимки преступников; для исследования ДНК в рамках расследования преступлений, отцовства и происхождения.)
Словарь / Определения
биомедицинская инженерия: применение инженерных методов для понимания биологических систем и разработки терапевтических технологий и устройств. Диализ почек, кардиостимуляторы, синтетическая кожа, искусственные суставы и протезы — вот некоторые продукты биомедицинской инженерии. Также называется биоинженерией.
ДНК: дезоксирибонуклеиновая кислота содержит генетические инструкции, которые контролируют биологическое развитие наших клеток и белков, которые они производят.ДНК кодирует последовательность аминокислот в белках, используя генетический код, триплетный код нуклеотидных оснований.
инженер: человек, который применяет свое понимание науки и математики для создания вещей на благо человечества и нашего мира.
ген: сегменты ДНК, которые переводятся в белки.
нуклеотидное основание: часть РНК и ДНК, участвующая в спаривании; он включает цитозин, гуанин, аденин, тимин (ДНК) и урацил (РНК), сокращенно C, G, A, T и U.В генетике их обычно называют просто базами. Также называется парами оснований.
Синтез белка: процесс, в котором образуются белки. Коды нуклеотидных оснований ДНК транскрибируются РНК-полимеразой для образования мРНК, которая переносит код из ядра клетки в рибосомы в цитоплазме. Рибосомы переводят кодоны в мРНК, чтобы образовать аминокислотные цепи, которые становятся белками.
рибосома: крошечная круглая частица, состоящая из РНК и белка, которая находится в цитоплазме живых клеток и служит местом сборки полипептидов, кодируемых матричной РНК.
Оценка
Оценка перед уроком
Вопрос для обсуждения : Попросите студентов написать «рецепт» того, что нужно для создания человека. Сравните списки. Проведите обсуждение ДНК и того, как она содержит «рецепт» нашего тела.
Оценка после введения
Вопрос / ответ : Задайте студентам вопросы и попросите их поднять руки, чтобы ответить. Запишите их ответы на доске.
- Где хранится информация о том, как создавать наши клетки? (Ответ: В нашей ДНК это дезоксирибонуклеиновая кислота.)
- Что такое ген? (Ответ: Ген — это сегмент ДНК, который транслируется в белок.)
- Как ученые и инженеры используют наше понимание ДНК на благо общества? (Возможные ответы: для выявления наследственных заболеваний у людей; для выявления инфекционных заболеваний и отслеживания их источников; для диагностики, лечения и [возможно] профилактики таких заболеваний человека, как рак, муковисцидоз и болезни сердца; для изменения организмов по желаемому признаку. или белка; для улучшения урожая; для поимки преступников; для исследования ДНК в рамках расследования преступлений, отцовства и происхождения.)
Итоги урока Оценка
Инженерное воздействие : Мы узнали, что биомедицинские инженеры разрабатывают инструменты и процессы, позволяющие проводить анализ ДНК для изменения и улучшения сельскохозяйственных культур, поимки преступников, выявления болезней и определения отцовства и происхождения. Биомедицинские инженеры даже нашли способы модифицировать ДНК организмов, чтобы создать желаемый признак или белок (например, создать бактерии, которые создают человеческий инсулин). Предложите учащимся подумать о потенциальных абстрактных воздействиях ДНК-инженерии на общество и окружающую среду.Затем попросите учащихся выбрать одну возможную область воздействия (например, экологическую, этическую, экономическую, социальную [людей]) и написать убедительный аргумент, описывающий возможные воздействия (положительные и отрицательные) на эту область из-за инженерии ДНК.
Мероприятия по продлению урока
Исследование и отчет : Предложите студентам изучить «проект генома человека», чтобы выяснить, что это такое и почему он важен.Сообщите классу о пяти важных результатах этого исследовательского проекта. Начните свое исследование на веб-сайте проекта «О геноме человека» Национальной лаборатории Окриджа: http://www.ornl.gov/sci/techresources/Human_Genome/project/about.shtml
Предложите учащимся исследовать генетически модифицированные продукты питания, сообщая классу, представляют ли они опасность для здоровья и / или окружающей среды. В лаборатории продукты генетически модифицируются, отбирая их по желаемым характеристикам. Например, в 1992 году помидор FlavrSavr® был создан путем модификации его ДНК, чтобы помидор сопротивлялся гниению.А как насчет модифицированных фруктов в продуктовом магазине, рекламирующих, что в них нет семян? Каковы преимущества? Какие разногласия? Начните свое исследование на веб-сайте генетически модифицированных продуктов и организмов Национальной лаборатории Окриджа: http://www.ornl.gov/sci/techresources/Human_Genome/elsi/gmfood.shtml
Предложите учащимся узнать больше о синтезе белков. Попросите их описать, как образуется белок, исходя из его кода азотистых оснований в ДНК. (Ответ: коды нуклеотидных оснований транскрибируются РНК-полимеразой для образования мРНК, которая переносит код из ядра клетки в рибосомы в цитоплазме.Рибосомы транслируют кодоны мРНК, образуя аминокислотные цепи, которые становятся белками.)
Дополнительная поддержка мультимедиа
Используйте интерактивные мультимедийные мероприятия для изучения некоторых приложений ДНК-технологии на веб-сайте «Включение ДНК в работу» Кошлендского музея науки: https://koshland-science-museum.org/exhibitdna/inf02.jsp?PF=1#.T_tOjFJ6DqM
Превосходная графика ДНК и изображения, подходящие для презентаций PowerPoint или цветные прозрачные пленки, доступны на веб-сайте галереи изображений Программы генома человека Министерства энергетики США: http: // genomics.energy.gov/gallery/
Рекомендации
Блумберг, Роберт Б. (ред.) MendelWeb. Выпуск 97.1 (22 февраля 1997 г.). MendelWeb.
Gene. Последнее обновление 24 февраля 2009 г. Википедия, Бесплатная энциклопедия. По состоянию на 24 февраля 2009 г. http://en.wikipedia.org/wiki/Genes
Генетический код. Последнее обновление 21 февраля 2009 г. Википедия, Бесплатная энциклопедия. Фонд Викимедиа, Inc.По состоянию на 24 февраля 2009 г. (Включает полный список кодонов и аминокислот, которые они указывают в таблице кодонов РНК) http://en.wikipedia.org/wiki/Codons
Геномные программы Министерства энергетики США. Министерство энергетики США. (Хороший ресурс для информации и изображений)
Биосинтез белков. Последнее обновление 16 января 2009 г. Википедия, Бесплатная энциклопедия. По состоянию на 24 февраля 2009 г. http://en.wikipedia.org/wiki/Protein_biosynthesis
Авторские права
© 2007 Регенты Университета КолорадоАвторы
Фрэнк Буркхолдер; Джессика Тодд; Малинда Шефер Зарске; Дениз В.КарлсонПрограмма поддержки
Комплексная программа преподавания и обучения, Инженерный колледж, Университет Колорадо в БоулдереБлагодарности
Содержание этой учебной программы по цифровой библиотеке было разработано за счет грантов Фонда улучшения послесреднего образования (FIPSE), Министерства образования США и Национального научного фонда (грант GK-12 № 0338326).Однако это содержание не обязательно отражает политику DOE и NSF, и вы не должны рассчитывать на одобрение со стороны федерального правительства.
Последнее изменение: 30 апреля 2021 г.
ДНК против РНК — 5 ключевых отличий и сравнение
Listicle 18 декабря 2020 г. | Руайри Дж. Маккензи, редактор журнала Technology Networks
Дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК), пожалуй, самые важные молекулы в клеточной биологии, ответственные за хранение и считывание генетической информации, лежащей в основе всей жизни.Оба они представляют собой линейные полимеры, состоящие из сахаров, фосфатов и оснований, но есть некоторые ключевые различия, которые разделяют два 1 . Эти различия позволяют двум молекулам работать вместе и выполнять свои основные роли. Здесь мы рассмотрим 5 ключевых различий между ДНК и РНК. Прежде чем мы углубимся в различия, мы рассмотрим эти две нуклеиновые кислоты бок о бок.
A Сравнение спирали и основной структуры РНК и ДНК
ДНК vs.РНК — Сравнительная таблица
Сравнение | ДНК | РНК | |||||||||||
| Полное наименование | Дезоксирибонуклеиновая кислота | ДНК реплицирует и хранит генетическую информацию. Это план всей генетической информации, содержащейся в организме. | РНК преобразует генетическую информацию, содержащуюся в ДНК, в формат, используемый для создания белков, а затем перемещает ее на фабрики рибосомных белков. | ||||||||||
Структура | ДНК состоит из двух цепей, расположенных по двойной спирали. Эти нити состоят из субъединиц, называемых нуклеотидами. Каждый нуклеотид содержит фосфат, молекулу сахара с 5 атомами углерода и азотистое основание. | РНК имеет только одну цепь, но, как и ДНК, состоит из нуклеотидов. Нити РНК короче цепей ДНК. РНК иногда образует вторичную двойную спиральную структуру, но только периодически. | |||||||||||
Длина | ДНК — намного более длинный полимер, чем РНК. Хромосома, например, представляет собой одну длинную молекулу ДНК, длина которой в распакованном виде составляет несколько сантиметров. | Молекулы РНК разной длины, но намного короче, чем длинные полимеры ДНК. Большая молекула РНК может состоять всего из нескольких тысяч пар оснований. | |||||||||||
Сахар | Сахар в ДНК представляет собой дезоксирибозу, которая содержит на одну гидроксильную группу меньше, чем рибоза РНК. | РНК содержит молекулы сахара рибозы без гидроксильных модификаций дезоксирибозы. | |||||||||||
Основания | Основания в ДНК — это аденин («A»), тимин («T»), гуанин («G») и цитозин («C»). | РНК разделяет аденин («A»), гуанин («G») и цитозин («C») с ДНК, но содержит урацил («U»), а не тимин. | |||||||||||
Базовые пары | Пара аденина и тимина (AT)Пара цитозина и гуанина (CG) | Пара аденина и урацила0005 и пара цитозина (AU4) 9 (AU4) ) | |||||||||||
Местоположение | ДНК обнаружена в ядре, небольшое количество ДНК также присутствует в митохондриях. | РНК образуется в ядрышке, а затем перемещается в специализированные области цитоплазмы в зависимости от типа образованной РНК. | |||||||||||
| Реакционная способность | Из-за дезоксирибозного сахара, который содержит на одну кислородсодержащую гидроксильную группу меньше, ДНК является более стабильной молекулой, чем РНК, что полезно для молекулы, задачей которой является сохранение генетической информации в безопасности. | РНК, содержащая рибозный сахар, более реактивна, чем ДНК, и нестабильна в щелочных условиях.Более крупные спиральные канавки РНК означают, что она легче подвергается атаке ферментов. | |||||||||||
| Чувствительность к ультрафиолету (УФ) | ДНК уязвима для повреждения ультрафиолетом. | РНК более устойчива к повреждению УФ-светом, чем ДНК. |
Каковы основные различия между ДНК и РНК?
Функция
Какие три типа РНК?
- Информационная РНК ( мРНК ) копирует части генетического кода, процесс, называемый транскрипцией, и переносит эти копии в рибосомы, являющиеся клеточными фабриками, которые способствуют производству белков из этого кода.
- РНК переноса ( тРНК ) отвечает за доставку аминокислот, основных строительных блоков белка, на эти белковые фабрики в ответ на закодированные инструкции, вводимые мРНК. Этот процесс построения белка называется трансляцией.
- Наконец, рибосомная РНК ( рРНК ) является компонентом самой фабрики рибосом, без которой производство белка не могло бы происходить 3 .
Сахар
И ДНК, и РНК построены на основе сахара, но в то время как сахар в ДНК называется дезоксирибозой (слева на изображении), сахар в РНК называется просто рибозой (справа на изображении).Префикс «дезокси» означает, что, в то время как РНК имеет две гидроксильные (-ОН) группы, присоединенные к ее углеродной основной цепи, ДНК имеет только одну и вместо нее присоединен одинокий атом водорода. Дополнительная гидроксильная группа РНК оказывается полезной в процессе преобразования генетического кода в мРНК, которые могут быть превращены в белки, в то время как сахар дезоксирибозы придает ДНК большую стабильность 4 .
Химическая структура дезоксирибозы (слева) и рибозы (справа) Сахаров
Оснований
Азотистые основания в ДНК являются основными единицами генетического кода, и их правильное упорядочение и спаривание имеют важное значение для биологического функция.Четыре основания, составляющие этот код, — это аденин (A), тимин (T), гуанин (G) и цитозин (C). Основания соединяются вместе в структуру двойной спирали, эти пары представляют собой A и T, а также C и G. РНК не содержит тиминовых оснований, заменяя их основаниями урацила (U), которые соединяются с аденином 1 .
Структура
В то время как повсеместное распространение двойной спирали ДНК Фрэнсиса Крика и Джеймса Уотсона (или Розалинд Франклин?) Означает, что двухцепочечная структура структуры ДНК общеизвестна, одноцепочечный формат РНК не так хорошо известен.РНК может образовывать двухцепочечные структуры, например, во время трансляции, когда молекулы мРНК и тРНК образуют пару. Полимеры ДНК также намного длиннее полимеров РНК; Геном человека длиной 2,3 м состоит из 46 хромосом, каждая из которых представляет собой одну длинную молекулу ДНК. Для сравнения, молекулы РНК намного короче 4 .Расположение
Эукариотические клетки, включая все клетки животных и растений, содержат большую часть своей ДНК в ядре, где она существует в сильно сжатой форме, называемой хромосомой 5 .Этот сжатый формат означает, что ДНК можно легко хранить и переносить. Помимо ядерной ДНК, часть ДНК присутствует в митохондриях, производящих энергию, небольших органеллах, свободно плавающих в цитоплазме, области клетки за пределами ядра.
Три типа РНК находятся в разных местах. мРНК образуется в ядре, причем каждый фрагмент мРНК копируется из соответствующего участка ДНК перед тем, как покинуть ядро и попасть в цитоплазму. Затем фрагменты перемещаются по клетке по мере необходимости, перемещаясь с помощью внутренней транспортной системы клетки, цитоскелета.тРНК, как и мРНК, представляет собой свободно перемещающуюся молекулу, которая перемещается по цитоплазме. Если он получает правильный сигнал от рибосомы, он затем будет выслеживать аминокислотные субъединицы в цитоплазме и переносить их на рибосому для встраивания в белки 5 . рРНК, как упоминалось ранее, находится в составе рибосом. Рибосомы образуются в области ядра, называемой ядрышком, перед тем, как экспортироваться в цитоплазму, где некоторые рибосомы свободно плавают. Другие цитоплазматические рибосомы связаны с эндоплазматическим ретикулумом, мембранной структурой, которая помогает обрабатывать белки и экспортировать их из клетки 6 .
Ссылки
- https://www.ncbi.nlm.nih.gov/books/NBK21154/
- https://ghr.nlm.nih.gov/primer/basics/dna
- https: // www.rnasociety.org/about/what-is-rna/
- https://www.nature.com/scitable/topicpage/chemical-structure-of-rna-348
- https://www.genome.gov / 25520880 / deoxyribonucleic acid-dna-fact-sheet / # al-2
- http://jcs.biologies.org/content/126/21/4815
Чтобы персонализировать контент, который вы видите на домашней странице Technology Networks, войдите в систему или подпишитесь бесплатно
АВТОРИЗОВАТЬСЯ ПОДПИСАТЬСЯ БЕСПЛАТНОФерменты нуклеиновой кислоты: игра с более полной колодой
Плохая РНК.Состоит всего из четырех субъединиц и химически подобных субъединиц, удивительно, что РНК может иметь эффективные ферментативная активность. Тем не менее, начиная с открытия РНК ферменты в природе (1, 2), и продолжается разработка новых Ферменты РНК через in vitro эволюция (3, 4), сейчас Совершенно очевидно, что РНК может быть эффективным и универсальным катализатором. Репертуар химических реакций, которые могут катализироваться РНК, составляет широкая (таблица 1) и расширяющаяся стабильно.Каталитические скорости более 1 секунды -1 и каталитические Сообщалось об увеличении скорости до 10 13 раз (последние обзоры см. в ссылках 5 и 6).
Таблица 1Реакции, катализируемые РНК и ДНК ферменты
Пытаясь объяснить каталитическую активность ферментов РНК, несколько авторы указали на решающую роль, которую играет металл кофакторы, чаще всего Mg 2+ (7–9). До недавнего времени это было считал, что все ферменты РНК — металлоферменты.Двухвалентный металл катионы помогают сложить РНК в четко определенную структуру и помогают в катализ, действуя либо как кислота Льюиса, либо, при координации с водой, обычным кислотным основанием. Однако за последний год он Стало ясно, что двухвалентные металлы не являются существенными для РНК-катализа. Рибозим шпильки, например, так же активен в присутствии Mg 2+ в присутствии обменно-инертного металла комплексный гексамин кобальта (10–12). Это убедительно свидетельствует о том, что функциональные группы самой РНК несут ответственность за катализ.
Нуклеотидным компонентам РНК не хватает химического разнообразия, конечно по сравнению с аминокислотными компонентами белков. Просто подумайте, что могла бы сделать РНК, если бы у нее была боковая цепь имидазола, например гистидин, карбоксильная группа, такая как глутаминовая кислота, или сульфгидрильная группа как цистеин. Но РНК также должна функционировать как генетическая макромолекула, и в этом контексте его химическая однородность может быть выгодной, потому что это упрощает задачи репликации и транскрипции. Относительно для каталитической функции, в РНК отсутствует общее кислотное основание с pK — в нейтральном диапазоне, как в гистидине.На с другой стороны, pK a N-1 аденина (обычно 3,5) или N-3 цитозина (обычно 4,2) может смещаться вверх в пределах специального локального окружающая среда (13, 14). Фосфатные группы вдоль остова РНК могут взять на себя некоторые функции карбоксилатной группы глутаминовой кислоты кислоты, а внутренние 2′-гидроксилы и концевой 2 ‘, 3’-диол РНК могут можно рассматривать как частичную замену сульфгидрила цистеина.
Если РНК следует пожалеть из-за ее отсутствия химической функциональности, то что мы можем сказать о ДНК? Те, кто знаком с РНК-катализом и РНК третичную структуру пришли к пониманию важности 2′-гидроксильная группа.Таким образом, ожидается, что ДНК, лишенная 2′-гидроксила, будет далее помешал как катализатор. Тем не менее, ряд ферментов ДНК были описаны в последние годы. Возможно, у природы не было возможности или стимул для изобретения ферментов ДНК, но это было достигнуто в лаборатория через in vitro evolution (обзор см. исх. 15). Диапазон химических реакций, катализируемых ДНК все еще ограничена по сравнению с РНК (Таблица 1). Однако больше ДНК ферменты уже на подходе, и в настоящее время это ДНК, а не РНК фермент, который утверждает, что является ферментом нуклеиновой кислоты с высочайшая каталитическая эффективность (16).Кроме того, есть примеры Ферменты ДНК, которым не требуется металлический кофактор для их каталитического активность (17, 18). Последний пример независимой от металлов ДНК фермент, который вместо этого использует кофактор гистидина, сообщается в этом выпуск Труды (19).
Мы привыкли к тому, что ферменты не нужно включать аминокислот; нуклеотиды могут очень хорошо действовать. Мы пришли к пониманию что кофакторы металлов, хотя и полезны, не являются необходимыми для нуклеиновой кислотный катализ, а также 2′-гидроксильная группа, которая отличает РНК из ДНК.Что еще можно выбросить за борт? Действительно ли все четыре нуклеотида нужно? А что насчет фосфатов? Ясно, что наступит момент убывающей отдачи, за которой дальнейшее сокращение химических разнообразие несовместимо с эффективной каталитической функцией. Однако эффективность дарвиновской эволюции не должна быть недооценен. Независимо от того, работаете ли оно на природе или в лаборатории, эволюция — это мощная стратегия оптимизации, которая может стимулировать даже самый слабый гетерополимер для химического реакция.
Возможно, более интригующе будет подумать о проблеме в наоборот: как может быть химическое разнообразие нуклеиновых кислот? увеличились, чтобы увеличить их каталитический потенциал? Одна возможность было бы заменить один из стандартных нуклеотидов на нуклеотид аналог, обладающий расширенным функционалом. При разработке фермента РНК с активностью, образующей амидные связи, Итон и его коллеги (20) заменили уридина с 5-имидазольным производным уридина, тем самым захватывая аромат гистидина в нуклеиновой кислоте.Образовавшаяся амидсинтаза показали повышение каталитической скорости 10 4 — до 10 5 -кратно, в зависимости от выбора кофактора иона металла. Внутри каталитического нейтрализатора есть три остатка 5-имидазолуридина. домен фермента. Их роль в катализе не установлена. но замена этих остатков немодифицированными уридинами отменила каталитическая активность.
При разработке фермента РНК, который катализирует циклоприсоединение Дильса-Альдера В результате реакции Итон и его коллеги (21) заменили уридин на 5-пиридил производное уридина, ожидая плодотворного взаимодействия между пиридиновые «боковые цепи» и поставляемый кофактор Cu 2+ .Полученный катализатор, требующий обеих модификаций пиридина и Cu 2+ , является первым примером фермента нуклеиновой кислоты. с активностью образования углерод-углеродных связей. Это действие не могло быть полученный при использовании четырех стандартных нуклеотидов (21).
Использование транскрипционно включенных аналогов нуклеотидов является мощный подход для увеличения функционального разнообразия нуклеиновых кислоты. Разнообразие рибонуклеотидов (22) и дезоксирибонуклеотидов (К. Шакти и К.Ф. Барбас, личное сообщение) аналоги могут быть включенным таким образом. Однако этот подход сталкивается с тремя важные ограничения. Во-первых, в контексте in vitro эволюционные эксперименты, генетические свойства нуклеотида аналог необходимо сохранить. Таким образом, аналог, несущий 5′-трифосфат, должен быть включен полимеразой, и Полученный полимер должен служить шаблоном для копирования полимеразой. Во-вторых, замена аналога должна происходить глобально.Смешанный распределение, скажем, уридинов и 5-замещенных уридинов не могло быть поддерживаются в определенных местах вдоль полимера, потому что оба по шаблону аденозина. В-третьих, не более четырех аналогов нуклеотидов. можно использовать единовременно. Даже если бы была доступна третья пара оснований, можно было бы отличить от двух других (23), полимер будет вмещать не более шести различных субъединиц по сравнению с 20 субъединиц белков.
Другой подход к увеличению функционального разнообразия нуклеиновых кислот. кислоты — посттранскрипционная модификация.Это способ, которым модифицированные основания производятся внутри трансферных, рибосомных и других биологические РНК. Посттранскрипционные модификации могут быть выполнены либо химически или ферментативно. Если модификации производятся химическим способом, тогда их сложно ограничить конкретным нуклеотидом должность. Одно важное исключение — это модификация для конкретного сайта аналог нуклеотида, который был включен на 5′-конце in vitro РНК, транскрибируемая , или в праймерной части in vitro ДНК, полученная .Если изменения внесены ферментативно, то сайт модификации может быть специфическим, так как определяется распознающими свойствами модифицирующего фермента. В модифицирующий фермент может быть отдельным ферментом белка или нуклеиновой кислоты, но также может быть нуклеиновая кислота, которая сама подвергается модификации. Последний случай иллюстрируется рибозимом группы I, который катализирует самовключение никотинамидадениндинуклеотида (NAD + ) или дефосфорилированный кофермент A (CoA) в определенном расположение рядом с его активным участком (24).Но если один фермент нуклеиновой кислоты (или каталитический домен) требуется для повышения функциональности другой, затем третий может потребоваться для повышения активности модифицирующий фермент и т. д. К счастью, не для каждой задачи потребуется модифицированные нуклеотиды, и возможно, что единственный модифицирующий фермент может работать на семействе катализаторов нуклеиновых кислот.
Еще один подход к увеличению химического разнообразия нуклеиновых кислот. кислотные ферменты должны обеспечивать отдельную молекулу кофактора, которая связана ферментом и используется в катализе.Этот подход потенциально далеко идущие, потому что налагает мало ограничений на химическую природу кофактора. В верхней части списка желательных кофакторов стоит аминокислота гистидин, желанная за способность действовать как обычная кислота основание при pH, близком к нейтральному. В этом выпуске журнала Proceedings , Рот и Брейкер (19) сообщают о разработке фермента ДНК, который зависит от l-гистидина из-за его способности расщеплять цель Фосфоэфир РНК. Группа имидазола кофактора гистидина появляется функционировать в качестве общей основы для облегчения депротонирования 2 ‘ гидроксил, который находится рядом с расщепленным фосфоэфиром.Фермент не требует кофактора иона двухвалентного металла, и, таким образом, механически больше похож на белковый фермент рибонуклеазу А, чем к другим РНК-расщепляющим ферментам нуклеиновых кислот (рис. 1).
Рисунок 1Три подхода к каталитическому расщеплению Фосфоэфир РНК. ( A ) Рибонуклеаза A использует два гистидина остатки, один как общее основание (His-12), а другой как общее кислота (His-119) (25). ( B ) Ферменты нуклеиновой кислоты, такие как рибозим в форме головки молотка (26) и фермент ДНК 10–23 (16) используют Mg (OH) + в качестве общего основания.( C ) Рот и Фермент разрушающий ДНК (19) использует кофактор гистидина в качестве общей основы.
Исследование Рота и Брейкера открывает дверь к тому, что будет щедростью in vitro, ферменты нуклеиновых кислот, эволюционировавшие в , которым помогают неметаллические кофакторы. Развивающиеся популяции молекул РНК или ДНК могут столкнуться с проблемой использования различных кофакторов, в том числе биологических и небиологические аминокислоты, пептиды, небольшие органические молекулы и даже соединения, выбранные из библиотеки потенциально полезных лиганды.
Важный урок, который следует из исследования Рота и Брейкера. касается препятствия, которое необходимо преодолеть при разработке кофактора сайт связывания в ферменте нуклеиновой кислоты. В принципе, это может быть осуществлено посредством in vitro эволюции при условии, что связанный кофактор способствует пригодности фермента. Это может быть однако трудно добиться как плотного связывания кофактора, так и высокая каталитическая эффективность, потому что эти две задачи могут противоречивые требования к предпочтительной последовательности фермента.Исследования с участием in vitro отбора аптамеров (нуклеиновых кислот которые связывают целевой лиганд) ясно дали понять, что отбор для одно только связывание обычно приводит к развитию высокоаффинного сайт связывания (см. обзор 27). Но для катализа связанная кофактор должен быть правильно ориентирован по отношению к основанию, делает связывание с высоким сродством менее гарантированным. Гистидин-зависимая ДНК фермент Roth and Breaker имеет наблюдаемую скорость 0,2 min -1 в присутствии 100 мМ гистидина, что соответствует к увеличению каталитической скорости в ≈10 6 раз.Даже в при такой высокой концентрации кофактора сайт связывания гистидина остается ненасыщенный. Вариантные формы фермента с более высоким сродством для гистидина также имеют более низкую максимальную каталитическую скорость (19).
Совместная оптимизация связывания кофакторов и кофактор-зависимых катализ — проблема непреодолимая. Одним из решений было бы увеличить количество нуклеотидов в ферменте, чтобы в нем было достаточно сложность выполнения обеих задач. Другим решением было бы выберите кофакторы, которые, как известно, легко связываются с нуклеиновыми кислотами и ожидается, что они внесут значительный вклад в катализ.Какие кофакторы окажется самым выгодным? Опираясь на химическую интуицию и in vitro селекционных экспериментов, должна быть возможность очертить основной набор кофакторов, которые могут быть применены к широкому круг каталитических задач. Эти кофакторы можно было найти по одному время, но было бы предпочтительнее позволить развивающейся популяции нуклеиновых кислот, чтобы выбрать наиболее полезные кофакторы из библиотеки соединения.
Этот процесс открытия кофактора напоминает эксперимент по селекции на основе нуклеиновых кислот, который проводился на очень более грандиозных масштабов в раннюю историю жизни на Земле.Если принять понятие «мир РНК», наследственная генетическая система, основанная на геномах РНК и ферментах РНК, то нужно столкнуться с функциональные ограничения. В мире РНК люди, которые могли использовать соединения из окружающей среды в качестве каталитических кофакторов имели бы селективное преимущество. Они получили бы большее преимущество, если бы может синтезировать эти кофакторы из легкодоступных исходных материалы. По-видимому, особое преимущество имел пептид кофакторы, которые могут быть синтезированы РНК.Итак, что могло начаться поскольку увлечение аминокислотными кофакторами в конечном итоге привело к возникновению аппарат перевода и передача каталитических обязанностей от РНК к белкам.
Сноски
↵ * Кому следует обращаться с запросами на перепечатку. электронное письмо: gjoyce {at} scripps.edu.
Дополнение к этому комментарию опубликовано на страницах 6027–6031.
- Авторские права © 1998, Национальная академия наук
| 1 | Дезоксирибонуклеиновая кислота | Рибонуклеиновая кислота |
| Молекула сахарной кислоты | ||
| в ДНК — дезоксирибоза (сахар рибозы в ДНК дезоксигенирован в своем 2 ‘положении.2 ’область имеет — H). | Молекула сахара в РНК представляет собой рибозу (оксигенированную в ее 2 ’положении. 2’ область содержит -ОН). | |
| 3 | Обычно ДНК имеет двухцепочечную структуру (встречается также одноцепочечная ДНК). | Обычно РНК одноцепочечная (встречается двухцепочечная РНК). |
| 4 | ДНК имеет двойную спиральную конформацию. | Обычно встречается в виде неправильно сложенных структур. |
| 5 | Спираль в ДНК имеет форму B (формы A и Z встречаются). | Спираль в РНК имеет форму А. |
| 6 | ДНК — высокостабильная молекула. | Стабильность РНК меньше. |
| 7 | ДНК действует как носитель генетической информации. | Обычно действует как промежуточная молекула между генетическим материалом (ДНК) и его экспрессирующими молекулами (белками).В некоторых вирусах РНК также действует на генетический материал. |
| 8 | Азотные основания ДНК: Пурины-аденин и гуанин Пиримидины: тимин и цитозин. | Азотные основания РНК: Пурины: аденин и гуанин Пиримидины: урацил и цитозин. |
| 9 | Спаривание оснований в ДНК: A — T и G — C. | Спаривание оснований в РНК: A — U и G — C. |
| 10 | В ДНК количество пуринов всегда равно количеству пиримидина. | Количество пуринов никогда не будет равно пиримидину. |
| 11 | Отношение пурина к пиримидину в ДНК всегда 1: 1. | Отношение пурина к пиримидину сильно варьируется. |
| 12 | ДНК следует правилу Чаргаффа. | РНК не подчиняется правилу Чаргаффа. |
| 13 | ДНК очень редко содержит неестественные основания или основания, отличные от A, T, G, C. | Некоторые РНК содержат неприродные основания, такие как псевдоуридин и 4-тиуридин |
| 14 | ДНК обычно связывается с гистоновыми белками у эукариот. | РНК не связана с гистоновыми белками. |
| 15 | ДНК может взаимодействовать с нуклеопротеидами с образованием хроматина и хромосом. | Может взаимодействовать с множеством белков, но не может образовывать хроматин или хромосомы. |
| 16 | ДНК располагается преимущественно в ядре. ДНК также присутствует в клеточных органеллах, таких как митохондрии и хлоропласты. | РНК обнаружена в ядре, цитоплазме и органеллах клетки, таких как митохондрии и хлоропласты. |
| 17 | ДНК имеет сравнительно меньшие бороздки и, следовательно, они защищены от ферментативных атак. | РНК имеет сравнительно большие бороздки и, следовательно, они очень уязвимы для атаки гидролитических ферментов. |
| 18 | ДНК устарела в щелочных условиях, потому что в ней отсутствует положение -ОН группы 2 ’. | РНК нестабильна в щелочных условиях из-за присутствия -ОН в 2 ’части. Группа -ОН в положении 2 ’очень реактивна. |
| 19 | ДНК не обладают каталитической активностью | Некоторые молекулы РНК обладают каталитической активностью (рибозимы). Пример: пептидилтрансфераза. |
| 20 | ДНК чрезвычайно чувствительна к УФ-излучению. | РНК сравнительно устойчива к УФ-излучению. |
| 21 | Количество ДНК фиксируется в клетках. | Количество РНК не фиксировано; он сильно варьирует в разных состояниях клеточного цикла. |
| 22 | ДНК — это сравнительно длинные структуры с высокой молекулярной массой. ДНК содержит миллионы пар оснований. | РНК представляет собой сравнительно короткие структуры, обычно немногочисленные до 15000 нуклеотидов. |
| 23 | В зависимости от функции во всех организмах обнаружен только один тип ДНК. | Различные типы РНК обнаруживаются в клетках в зависимости от ее функций, таких как рРНК, тРНК, мРНК, миРНК, миРНК, мяРНК и т. Д. |
| 24 | ДНК не может находиться в цитоплазме в свободном состоянии. | РНК может находиться в цитоплазме в свободном состоянии |
| 25 | Остаток сахара дезоксирибозы в ДНК является C2 ’эндо формой. | Остаток сахара рибозы в РНК представляет собой C3 ’эндо-форму. |
| 26 | ДНК-краситель синий с азурофталатным красителем. | РНК красит в красный цвет азурофталатным красителем. |
| 27 | ДНК окрашивает зеленым красителем пиронин. | РНК красит красным пирониновым красителем. |
Проблемы и возможности для разработки аптамеров с малыми молекулами
Аптамеры представляют собой одноцепочечные олигонуклеотиды, которые связываются с мишенями с высокой аффинностью и селективностью. Их использование в качестве элементов молекулярного распознавания стало жизнеспособным подходом для биочувствительности, диагностики и терапии. Несмотря на этот потенциал, существует относительно немного аптамеров, которые связываются с небольшими молекулами. Небольшие молекулы являются важными мишенями для исследований из-за их разнообразных биологических функций, а также их клинического и коммерческого использования.Поэтому большой интерес представляют новые эффективные зонды молекулярного распознавания этих соединений. В этой статье будут освещены технические проблемы разработки аптамеров для мишеней из малых молекул, а также возможности, которые существуют для их применения в биодатчиках и химической биологии.
1. Аптамеры как элементы молекулярного распознавания
Исторически нуклеиновые кислоты были связаны с хранением и генетическим кодированием информации и долгое время считались менее сложными, чем белки [1].Однако, как и белки, нуклеиновые кислоты способны складываться в сложные третичные структуры, которые могут выполнять множество функций, включая генную регуляцию, каталитическую активность и связывание лиганда [2]. Интерес к этим так называемым «функциональным» нуклеиновым кислотам был вызван постоянно растущим числом открытий некодирующих рибонуклеиновых кислот (РНК), проявляющих каталитические или связывающие свойства [2].
Два десятилетия назад несколько исследователей произвели революцию в молекулярном распознавании, разработав синтетические мотивы РНК, которые специфически связываются с молекулярными мишенями [3–5].Эти структуры РНК, называемые аптамерами, были отобраны с использованием процедуры отбора in vitro , называемой систематической эволюцией лигандов путем экспоненциального обогащения (SELEX) [3]. Как и антитела, эти синтетические молекулярные зонды распознавания оказались селективными и способны связываться со своими мишенями с высокой аффинностью.
В настоящее время растет потребность в быстрых, надежных и недорогих методах измерения и диагностики [6]. Поскольку молекулярное распознавание является краеугольным камнем зондирования, все большее внимание уделяется разработке новых зондов молекулярного распознавания для сенсорных приложений [7].В то время как антитела долгое время считались стандартом в молекулярном распознавании, а использование антител в качестве зондов распознавания появилось еще до 1950-х годов, относительно новая технология аптамеров предлагает несколько преимуществ [8]. Во-первых, процесс отбора аптамера in vitro позволяет лучше контролировать условия связывания аптамера. Для успешного отбора можно использовать нефизиологические концентрации солей, температуры и pH [9]. Благодаря прочности фосфодиэфирного остова аптамеры могут демонстрировать улучшенную стабильность по сравнению с их аналогами на основе антител на основе белков.В частности, аптамеры могут быть обратимо денатурированы путем изменения окружающих условий. Например, изменение pH, температуры, ионной силы или использование денатурирующих веществ необратимо денатурирует антитела, в то время как аптамеры просто разворачиваются. Затем структура аптамера может восстановить функциональность после возврата к исходным условиям связывания [6]. Из-за нуклеиновой природы аптамеров они связываются с комплементарными нуклеиновыми кислотами, а также со своими мишенями, что может быть использовано в схемах зондирования или в качестве «антидотов» in vivo .Генерация аптамеров была достигнута для широкого круга мишеней, включая небольшие молекулы [10], белки [11], вирусы [12] и целые клетки [13]. В отличие от антител, аптамеры также могут быть созданы для мишеней, которые являются токсичными, а также для мишеней, которые не вызывают иммунный ответ in vivo [8]. После выбора аптамеры производятся с использованием хорошо зарекомендовавшего себя автоматизированного химического твердофазного синтеза [14, 15]. Точность и воспроизводимость этой процедуры позволяет относительно легко производить аптамеры в больших масштабах с очень небольшими вариациями активности от партии к партии [16].Кроме того, последовательности аптамеров могут быть модифицированы репортерными молекулами на протяжении всего твердофазного синтеза; это позволяет метить в разумно выбранные положения нуклеотидов, чтобы минимизировать любое влияние на функциональность аптамера [17, 18].
Аптамеры также обладают преимуществами по сравнению с другими синтетически созданными системами молекулярного распознавания, такими как молекулярные импринтированные полимеры (MIP). Хотя синтез MIP может быть простым и дешевым, а полученные MIP не подвержены изменениям температуры и pH [19], MIP обычно демонстрируют высокую перекрестную реактивность [20] и не особенно поддаются химическим модификациям.
Конечно, аптамеры не лишены недостатков. В отличие от антител или MIPS, их третичная структура сильно зависит от условий раствора, и они легко разлагаются в крови. Кроме того, антитела обладают значительно более высоким химическим разнообразием и содержат 20 аминокислот. Однако некоторые из этих проблем можно решить, например, с помощью химических модификаций для повышения устойчивости к нуклеазам или увеличения разнообразия пулов нуклеиновых кислот.
1.1. Систематическая эволюция лигандов путем экспоненциального обогащения (SELEX)
Концепция эволюции in vitro была впервые представлена в 1960-х годах, когда было обнаружено, что в бесклеточной системе геном РНК бактериофага Q β может быть изменен. эволюционировали во время репликации с образованием РНК, которые более эффективно копировались вирусной репликазой [21].Позже они смогли развить последовательности для других признаков, таких как устойчивость к бромистому этидию [22]. Однако, несмотря на важность этих ранних открытий, истинный потенциал эволюции in vitro был реализован лишь несколько десятилетий спустя, после внедрения современных биотехнологических достижений, таких как изобретение полимеразной цепной реакции (ПЦР), выделение обратного транскриптаза и способность генерировать длинные олигонуклеотиды, содержащие случайные нуклеотидные области, с использованием твердофазного синтеза.Оснащенные этими современными методами, в 1990 г. три отдельные группы сообщили о отборе и эволюции функциональных нуклеиновых кислот in vitro [23]. Tuerk и Gold [3] использовали термин SELEX для своего процесса выбора лигандов РНК против ДНК-полимеразы Т4; Эллингтон и Шостак [4] выполнили in vitro отбор для отбора лигандов РНК (для которых они придумали термин «аптамеры») против различных органических красителей; Робертсон и Джойс [5] разработали самосплайсинговый интрон Tetrahymena для осуществления реакции расщепления ДНК.
С момента его изобретения несколько исследователей выполнили SELEX для выделения нуклеиновых кислот с широким спектром функций. Несмотря на то, что различные группы внесли несколько модификаций процедуры, общий процесс SELEX остался прежним (рисунок 1 показывает процесс для ДНК-аптамеров). Обычно SELEX начинается с начальной библиотеки (часто называемой «пулом») случайных последовательностей нуклеиновых кислот (либо РНК, либо ДНК, в зависимости от характера исследования). В идеале библиотеки SELEX состоят из 30–80 случайных нуклеотидных положений, фланкированных сайтами связывания праймеров, необходимыми для амплификации ПЦР [24].Затем библиотеку инкубируют с интересующей мишенью и используют несколько этапов промывки для удаления нефункциональных последовательностей. Для низкомолекулярных мишеней мишень обычно иммобилизуют на твердой подложке, чтобы обеспечить разделение связывающих и несвязывающих последовательностей [25]. Следующие шаги в SELEX включают элюирование связывающих последовательностей из мишени и амплификацию с помощью полимеразной цепной реакции (ПЦР) (ПЦР с обратной транскрипцией для РНК-аптамеров) этих связывающих последовательностей для получения обогащенной библиотеки для последующих, более строгих, раундов отбора. [10].Поскольку взаимодействия, которые приводят к молекулярному распознаванию между связывающими последовательностями и мишенью, нековалентны по своей природе, можно использовать мягкие условия для разделения двух видов. Может быть выполнено элюирование с использованием тепла, высоких концентраций целевой молекулы или хаотропных агентов, таких как мочевина. Сила молекулярных взаимодействий внутри комплекса мишень-аптамер будет определять условия, необходимые для элюции [7].
После отделения от мишени несколько связывающих последовательностей ДНК амплифицируют с помощью ПЦР, чтобы получить практическое количество образца для продолжения процесса.Поскольку ПЦР генерирует двухцепочечную ДНК, а аптамеры являются одноцепочечными, последовательность ДНК-аптамера отделяется от ее комплемента с помощью одного из ряда методов, таких как гель-электрофорез или использование агарозной смолы [26, 27]. Аптамеры с одноцепочечной РНК генерируются из продуктов ПЦР с двухцепочечной ДНК посредством транскрипции in vitro [10], поэтому дальнейшая обработка не требуется перед повторным введением пула обогащенной РНК в следующий раунд SELEX.
Прогресс SELEX можно отслеживать, модифицируя нить аптамера с помощью отслеживаемой метки, чтобы определить, когда следует применять более строгие условия [28].Обогащенная библиотека, полученная в результате раунда отбора, подвергается дальнейшим раундам отбора, которые служат для увеличения сродства библиотеки к целевой молекуле (положительный отбор). После нескольких циклов обогащенную библиотеку клонируют, секвенируют и характеризуют для выделения аптамеров с желаемыми свойствами. Как только эти последовательности выяснены, твердофазный химический синтез используется для воспроизводимого синтеза аптамеров в больших количествах.
1.2. Адаптация к процессу SELEX
Огромным преимуществом SELEX является его гибкость в отношении методологии, условий привязки и дизайна библиотеки.Первые модификации SELEX вводили включение отрицательных или встречных шагов отбора для исключения последовательностей, демонстрирующих сродство либо к твердой подложке, либо к соединениям, имеющим структурное сходство с мишенью. Большинство более поздних модификаций SELEX включают изменение строгости, платформы, на которой выполняется отбор, или типа цели [29, 30]. Библиотека, используемая при отборе, также может быть модифицирована для включения фиксированных областей с известной функциональностью или увеличения разнообразия структур, доступных для отбора, либо посредством первоначального дизайна пула [28, 31, 32], либо путем включения мутагенной ПЦР для изменения пула с от раунда к раунду [33].Процесс SELEX также был автоматизирован несколькими группами [34–36]. В таблице 1 перечислены несколько модификаций исходного процесса SELEX. Независимо от того, включают ли перечисленные модификации SELEX изменения в иммобилизацию мишени, библиотеку нуклеиновых кислот, строгость отбора, амплификацию или мониторинг обогащения, целью этих изменений было либо создание улучшенных аптамеров, либо упрощение процедуры SELEX.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2. Цели SELEX
Как видно из рисунка 2, менее четверти существующих аптамеров были созданы для малых молекул-мишеней. После успеха первых экспериментов по селекции in vitro малых органических красителей [4] большая часть первоначального внимания SELEX была сосредоточена на разработке аптамеров для малых молекул. Однако, как только было обнаружено, что аптамеры можно легко отбирать для белков и клеток, новые аптамеры для малых молекул стали менее распространенными.Эти более крупные мишени, содержащие больше функциональных групп и структурных мотивов, дают более высокую вероятность обнаружения последовательностей, которые могут взаимодействовать с мишенью посредством водородных связей, электростатических взаимодействий и гидрофобных взаимодействий [6].
2.1. Аптамеры, связывающиеся с небольшими молекулами
Несмотря на эту тенденцию к более крупным мишеням, существует множество веских причин для поиска новых аптамеров, связывающихся с небольшими молекулами. Небольшие молекулы играют ключевую роль во многих биологических процессах из-за их способности диффундировать через клеточные мембраны [37].Эти мишени могут быть вредными, например, токсинами и канцерогенами, или полезными, например, лекарствами или питательными веществами. В клетках небольшие молекулы служат клеточными сигнальными молекулами, пигментами или частью защитных механизмов [38]. В молекулярной биологии они могут использоваться как антибиотики или другие важные лекарства [39]. В пищевой промышленности небольшие молекулы важны для хранения энергии или могут действовать как пестициды [40]. Аптамеры для малых молекул могут применяться в широком спектре приложений в медицине, сельском хозяйстве и анализе окружающей среды.В таблицах 2 и 3 перечислены небольшие молекулы-мишени, для которых были охарактеризованы аптамеры ДНК и РНК, соответственно.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
