Мутации у человека : Основы генетики : Все про гены!
Термин «мутация» ввел Г. де Фриз (1901) для характеристики случайных генетических изменений. Различают спонтанные и индуцированные мутационные процессы.
Индуцированный мутационный процесс — это возникновение наследственных изменений под влиянием направленного действия факторов внешней и внутренней среды. Возникновения мутаций без установленных причин принято называть спонтанным мутационным процессом.Мутационная изменчивость обусловлена как влиянием на организм факторов внешней среды, так и его физиологическим состоянием.
Частота возникновения мутаций зависит от:
• генотипа организма;
• фазы онтогенеза;
• стадии онтогенеза;
• стадии гаметогенеза;
• митотического и мейотического циклов хромосом;
• химического строения отдельных участков хромосом и др.

Свойства мутаций:
• мутации возникают внезапно, скачкообразно;
• мутации наследуются, т.е. передаются от поколения к поколению;
• мутации не направленные — подвергаться мутациям может любой локус (участок хромосомы), вызывая изменения как незначительных, так и жизненно важных признаков;
• одни и те же мутации могут возникать повторно;
• за проявлением мутации могут быть полезными и вредными, доминантными и рецессивными.
Классификация мутаций:
Мутации можно объединить в группы — классифицировать по характеру проявления, по месту или уровню их возникновения.
Мутации по характеру проявления — бывают доминантными и рецессивными. Большинство из них рецессивные и не проявляются в гетерозиготных организмах. Как правило, мутации вредны, ибо нарушают четко сбалансированную систему биохимических превращений.
Доминантные мутации проявляются сразу в гомо-и гетерозиготных организмах, преимущественно такие особи нежизнеспособны и гибнут на ранних стадиях онтогенеза. Мутации часто снижают жизнестойкость или плодовитость.
Мутации часто снижают жизнестойкость или плодовитость.
Мутации, которые резко влияют на жизнеспособность и частично или полностью останавливают развитие, называются полулетальными, а несовместимые с жизнью — летальными. У человека к таким мутациям относится рецессивный ген гемофилии.
Мутации по месту возникновения.
Мутации, возникающие в соматических тканях, получили название соматических мутаций. Соматические клетки составляют популяцию, образованную при бесполом размножении (делении) клеток. Соматические мутации обуславливают генотипическое разнообразие тканей, часто не передаются по наследству и ограниченные тем индивидуумом, в которого они возникли. Соматические мутации возникают в диплоидных клетках, поэтому проявляются только при доминантных генах или при рецессивных, но в гомозиготном состоянии. Чем раньше в эмбриогенезе человека возникла мутация, тем больший участок соматических клеток отклоняется от нормы.
Мутации, возникающие в гаметах или в клетках, с которых они образуются, получили название генеративных или терминальных мутаций. Чем раньше в половых клетках возникает мутация, тем больше будет доля половых клеток, которые будут нести новую мутацию. Верхний предел доли клеток, которые будут содержать индуцированную или спонтанную мутацию, составляет 50 процентов. Существует мнение, что наибольшее количество мутаций в половых клетках возникает в овоцитах. Поскольку сперматогонии подвергаются постоянному делению, то среди них может происходить отбор против мутаций, обуславливающих вредный эффект, и частота мутаций снижается до периода половой зрелости. Женщина, наоборот, рождается почти со всеми мутантными изменениями, в линии половых клеток нет параллельного митотического отбора. Овоциты не только не испытывают митоза, они остаются малоактивными на протяжении десятилетий, пока не станут яйцеклетками. За этот период овоциты стареют, становятся непропорционально чувствительными к спонтанной мутации. На половые клетки наибольшее влияние осуществляют цезий-137, стронций-90 и углерод-14.
Существует мнение, что наибольшее количество мутаций в половых клетках возникает в овоцитах. Поскольку сперматогонии подвергаются постоянному делению, то среди них может происходить отбор против мутаций, обуславливающих вредный эффект, и частота мутаций снижается до периода половой зрелости. Женщина, наоборот, рождается почти со всеми мутантными изменениями, в линии половых клеток нет параллельного митотического отбора. Овоциты не только не испытывают митоза, они остаются малоактивными на протяжении десятилетий, пока не станут яйцеклетками. За этот период овоциты стареют, становятся непропорционально чувствительными к спонтанной мутации. На половые клетки наибольшее влияние осуществляют цезий-137, стронций-90 и углерод-14.
Генеративные мутации при половом размножении передаются следующим поколениям. Доминантные мутации появляются уже в первом поколении, а рецессивные — только во втором и последующих поколениях, с переходом в гомозиготное состояние.
Мутации по характеру изменения наследственного материала:
1. Изменения, обусловленные заменой одного или нескольких нуклеотидов в пределах одного гена, называют генными или точечными мутациями. Они обусловливают изменения как в строении белков, так и функциональной активности молекулы.
Изменения, обусловленные заменой одного или нескольких нуклеотидов в пределах одного гена, называют генными или точечными мутациями. Они обусловливают изменения как в строении белков, так и функциональной активности молекулы.
2. Изменения структуры хромосом называют хромосомными мутациями или аберрациями. Такие мутации могут возникнуть в результате потери части хромосомы (делеция), удвоение части хромосомы (дупликации), отрыва и поворота части хромосомы на 180 ° (инверсия). Если изменение затрагивает жизненно важные участки гена, то такая мутация приведет к смерти. Так, потеря небольшого участка 21-й хромосомы у человека вызывает тяжелое заболевание крови — острый лейкоз. В отдельных случаях оторванный участок хромосомы может присоединиться к негомологичной хромосоме (транслокация), что приведет к новой комбинации генов и изменения их взаимодействия.
3. Изменения кариотипа, кратные или некратные гаплоидному числу хромосом называют геномными мутациями. Вследствии нарушения расхождения пары гомологичных хромосом во время мейоза в одной из образованных гамет содержится на одну хромосому меньше, а в другой на одну хромосому больше, чем при нормальном гаплоидном наборе. Слияние такой аномальной гаметы с нормальной гаплоидной гаметой при оплодотворении приводит к образованию зиготы с меньшим или большим количеством хромосом по сравнению с диплоидным набором, характерным для этого вида.
Вследствии нарушения расхождения пары гомологичных хромосом во время мейоза в одной из образованных гамет содержится на одну хромосому меньше, а в другой на одну хромосому больше, чем при нормальном гаплоидном наборе. Слияние такой аномальной гаметы с нормальной гаплоидной гаметой при оплодотворении приводит к образованию зиготы с меньшим или большим количеством хромосом по сравнению с диплоидным набором, характерным для этого вида.
Соматические мутации
• генные
• геномные
• хромосомные аберрации
Соматические мутации — это изменения наследственного характера в соматических клетках, возникающих на разных этапах развития особи. Они часто не передаются по наследству, а остаются, пока живет организм потерпевший мутационное воздействие.
Геномные, хромосомные и генные аберрации в соматических клетках являются следствием действия мутагенных факторов. У человека это этиологические факторы наследственных болезней. Заболевания, обусловленные геномными (изменение числа хромосом) и хромосомными (изменение структуры хромосом) мутациями, называются хромосомными болезнями. Изменение числа хромосом определяется удвоением или уменьшением всего набора хромосом. Это приводит к полиплоидии или гаплоидии (соответственно). Наличие лишних хромосом или удаление одной или нескольких хромосом приводит к гетероплоидии или анеуплоидии.
Заболевания, обусловленные геномными (изменение числа хромосом) и хромосомными (изменение структуры хромосом) мутациями, называются хромосомными болезнями. Изменение числа хромосом определяется удвоением или уменьшением всего набора хромосом. Это приводит к полиплоидии или гаплоидии (соответственно). Наличие лишних хромосом или удаление одной или нескольких хромосом приводит к гетероплоидии или анеуплоидии.
Изменение структуры хромосом — это перестройки или аберрации. При этом нарушается сбалансированность набора генов и нормальное развитие организма. Как следствие хромосомного дисбаланса происходит внутриутробная гибель эмбриона или плода, возникают врожденные пороки развития. Чем большее количество хромосомного материала подверглось мутационному эффекту, тем раньше заболевания появится в онтогенезе и тем весомее будут нарушения физического и психического развития особи. Характерная черта хромосомного дисбаланса — множественность пороков развития различных органов и систем.
Генные или точечные мутации — это результат молекулярных изменений на уровне ДНК. У человека они вызывают генные болезни. Для человека описаны следующие виды генных мутаций, приводящих к развитию наследственных болезней: нисенс, нонсенс, смещение рамки считывания, делеции, вставки (инсерции), нарушение сплайсинга, увеличение числа (экспансии) тринуклеотидних повторов. Мутации участков, что транскрибируются (которые определяют аминокислотную последовательность в молекуле белка, что синтезируется), приводят к синтезу аномального продукта и могут привести к уменьшению скорости синтеза белка.
Фенотипно генные мутации проявляются на молекулярном, клеточном, тканевом и органном уровнях. Число генных болезней составляет около 3500-4500. Генные мутации разделяют на односайтовые и багатосайтовые. Односайтовые — это такие, которые касаются изменений одного сайта (участка), багатосайтовые — охватывают несколько сайтов генного локуса.

Различают генные мутации прямые и обратные. Прямые мутации — это мутации, которые инактивируют гены дикого типа и предопределяют появление мутантного типа. Обратные мутации — изменения к исходной форме от мутантной.
Большинство генов устойчивы к мутациям, но отдельные гены подвергаются мутациям довольно часто.
Соматические мутации обусловливают генотипическое разнообразие тканей одной особи и обычно не передаются по наследству при половом размножении. При бесполом размножении, если организм развивается из одной клетки или группы клеток, в которых возникла мутация, такие изменения могут передаваться потомкам. Соматические мутации возникают у организмов, которые размножаются вегетативно и, поэтому составляют основу селекции культурных растений, в частности цитрусовых.
Мутация передается по наследству | Юре-Про
Вконтакте
Google+
Одноклассники
Здравствуйте, в этой статье мы постараемся ответить на вопрос: «Мутация передается по наследству». Также Вы можете бесплатно проконсультироваться у юристов онлайн прямо на сайте.
Также Вы можете бесплатно проконсультироваться у юристов онлайн прямо на сайте.
Прежде чем пить что-то, необходимо точно знать, что с вами и от чего не наступает беременность. Без назначения врача вы можете пить витамины, которые …
Инцест отрицательно влияет на репродуктивную систему как у мужчин, так и женщин. Мужчины, как уже было сказано, могут страдать от крипторхизма, а женщины — от неправильного строения матки или вагинального канала, дисфункции яичников.
Не все мутации передаются по наследству.
Геномные и хромосомные мутации как полиплоидия (кратное увеличение количества хромосом) и дупликации (удвоения определенных участков хромосом) играют особую роль в эволюции. Это связано с тем, что они увеличивают количество генетического материала и тем самым открывают возможность возникновения новых генов с новыми свойствами.
Но они возникают редко, это очень малый процент от всего количества, поэтому они незначительны, что практически не влияют на организм.
При таких факторах возможность передачи кариеса по наследству составляет до 90 процентов. С другой стороны, кариес всегда имеет причиной нарушение кислотно-щелочного баланса, и если ребенок ограничит сладкое и будет правильно ухаживать за зубами, вероятность кариеса снижается на те же 90 процентов.
Так или иначе, ученый мир сегодня увлечен именно теми пятью процентами генов, которые располагают всей наиболее актуальной информацией об индивидуальных признаках. Может быть, это и есть наказание, неизбежно следующее от той частицы Бога, которая всегда живет в нашей душе.
Норма реакции признака передается по наследству
Мутации возникают в половых клетках — гаметах (гаметические мутации) и клетках тела (соматические мутации).
Но большая часть мутаций нейтральна. Они представляют собой незначительные изменения в генетическом коде, передающиеся по наследству и не являющиеся характерными признаками того народа, к которому принадлежит данный индивидуум. Так, например, среди монголов, отличающихся темным цветом волос, когда-то родился мальчик с невероятными для тех мест огненно-рыжими волосами. Звали его Чингисхан.
Так, например, среди монголов, отличающихся темным цветом волос, когда-то родился мальчик с невероятными для тех мест огненно-рыжими волосами. Звали его Чингисхан.
По характеру изменений генетического аппарата различают мутации: геномные, обусловленные сменой числа полного набора хромосом.
- Хромосомные мутации связаны с изменением структуры хромосом или их числа.
- Полиплоидия — увеличение числа хромосом, кратные гаплоидному набору. Различают среди растений триплоиды (Зп), тетраплоиды (4п) и т. д. В растениеводстве известно более 500 полиплоидов (сахарная свекла, гречиха, мята и т. д.). Все они выделяются большой вегетативной массой н имеют большую ценность.
- Гетероплоидия — изменение числа хромосом ие кратное гаплоидному набору. Это мутации, связанные с избытком или недостатком одной хромосомы из пары гомологичных хромосом. Такие мутации возникают при нарушении мейоза, когда после конъюгации пара хромосом не расходится и в одну гамету попадают обе гомологичные хромосомы, а в другую ни одной.

- Гетероплоидия вредна для организма. Например, у человека появление лишней хромосомы в 21 паре вызывает синдром Дауна (слабоумие).
- Генные мутации — затрагивают структуру самого гена и влекут за собой изменения свойств организма (гемофилия, дальтонизм, альбинизм и др.).
- Точковые, или генные мутации, обусловлены заменой одного или нескольких нуклеотидов в пределах одного гена. Они влекут за собой изменение строения белков, заключающееся в появлении новой последовательности аминокислот в полипептидной цепи.
В древности женщин, рожавших детей-даунов или аутистов, обвиняли в колдовстве и связи с нечистыми силами. Таких женщин сжигали на кострах, а детей травили собаками.
Наследственная изменчивость связана с изменениями генотипа признаки и свойства, приобретенные вследствие этого, передаются следующим поколениям.
Характер мутаций не зависит от внешней среды, однако такие факторы, как ионизирующее излучение и некоторые химические вещества, увеличивают частоту мутаций. Воздействие на человека высоких доз коротковолновых излучений вызывает развитие лучевой болезни.
Воздействие на человека высоких доз коротковолновых излучений вызывает развитие лучевой болезни.
Мутации, резко снижающие жизнеспособность, частично или полностью останавливающие развитие, называют соответственно полулетальными и летальными. У человека к таким мутациям относят рецессивный ген гемофилии.
Каждая хромосома образуется из молекулы ДНК, которая содержит генетическую информацию и передаётся от родителей к детям.
Наши жизненные взгляды и принимаемые на их основании решения зависят не только от нас. Нередко в этом большую роль играет влияние семьи — в частности, воспитание, формирующее наше сознание. И все же очень часто в действие вступают силы, от человека совсем не зависящие.
Мутировавшие эритроциты достались им по наследству от предков. Такие эритроциты плохо переносят кислород, поэтому их обладатели хилые и страдают анемией. Но они невосприимчивы к малярии.
Этот закон справедлив и для случаев, когда родители обладают богатырским здоровьем. Даже с такой, казалось бы, идеальной наследственностью здоровье малыша можно подорвать, если не следить за его образом жизни.
Даже с такой, казалось бы, идеальной наследственностью здоровье малыша можно подорвать, если не следить за его образом жизни.
Мутации привели к появлению большого числа людей, невосприимчивых к опасным инфекционным заболеваниям, таким как чума и СПИД, эти люди не заболеют ими даже во время самой страшной эпидемии.
Благодаря достижениям геномики каждый человек может получить свой генетический паспорт, по сути — генетическую расшифровку своего организма. В таком паспорте может быть указна склонность к болезням, а также генетически обусловленное отношение к различным видам спорта, перечень вредных продуктов, неблагоприятных климатических условий, неприемлемых условий труда.
Предел проявления модификационной изменчивости организма при неизменном генотипе — норма реакции. Норма реакции обусловлена генотипом и различается у разных особей данного вида. Фактически норма реакции — спектр возможных уровней экспрессии генов, из которого выбирается уровень экспрессии, наиболее подходящий для данных условий окружающей среды.
Передается ли по наследству характер?
В таком случае человек становится носителем какой-либо характеристики, которая будет — также в «спящем» виде — передаваться по наследству от поколения к поколению до тех пор, пока одному из представителей династии не встретится партнер с похожим геном.
Фенотипическая изменчивость не затрагивает генотип, обеспечивая лишь то или иное проявление заложенных в нем признаков. Она обычно предсказуема и у разных особей одного вида проходит однонаправленно. Например, если пшеничное поле не получает достаточно влаги, то у всех его растений плохо формируется колос.
Первых болезней существует примерно 600. Они меняют аминокислотный, углеводный и липидный состав клеток.
Яркий пример — появление на ветках черной смородины красных ягод или гетерохромия — явление разного цвета глаз у человека.
Это может быть изменение или даже выпадение целого участка хромосомы, изменение последовательности, перенос негомологичного участка с одной хромосомы на другую и т. д. Из-за такой перестройки может меняться функции генов. Зачастую это приводит к меньшей жизнеспособности организма.
д. Из-за такой перестройки может меняться функции генов. Зачастую это приводит к меньшей жизнеспособности организма.
Редкое наследственное заболевание, связанное с нарушением процесса свертывания крови. Самой известной носительницей гемофилии в истории была королева Виктория, этой же болезнью страдал один из ее сыновей, а также несколько внуков и правнуков, включая российского царевича Алексея Николаевича.
При выведении новых сортов растений и штаммов микроорганизмов используют индуцированные мутации (искусственно вызываемые различными мутагенными факторами: химическими веществами, рентгеновскими или ультрафиолетовыми лучами). Затем проводят отбор полученных мутантов, сохраняя наиболее продуктивные.
Как происходят мутации? ДНК каждого человека состоит всего лишь из четырёх азотистых оснований – A,T,G,C. Но молекула ДНК очень большая и они повторяются в ней многократно в разных последовательностях. Характеристика каждой нашей клетки зависит от того, в какой последовательности расположены эти азотистые основания.
Даже самая маленькая генная мутация резко увеличивает вероятность врождённых дефектов. Мутации могут стать причиной отклонений в развитии плода. Они возникают в процессе оплодотворения, когда сперматозоид встречается с яйцеклеткой. Что-то может пойти не так при смешении геномов или проблема может уже присутствовать в родительских генах. Это ведёт к рождению детей с генетическими отклонениями.
Мутации в генах у мужчин способствуют, развитию кистозного фиброза, приводящий к отсутствию семявыводящего протока. Эта аномалия присутствует у 5% мужчин, она также передается по наследству. 75% отпрысков будут иметь данную патологию.
Могут ли мутации вызвать положительные изменения в человеческом организме? Да, могут. А создать из него настоящего, интеллектуального, холодного монстра? Не известно. Это вопрос, скорее, философский. Проблемы духовности первичны и мало зависят от генетического кода. Наша фантазия нередко заставляет нас искать и ожидать появления неких человекообразных монстров.
При патологиях эндокринной и кровеносной систем назначаются лекарственные препараты, направленные на коррекцию заболевания. При повышенной свертываемости крови у женщины, врач-гематолог назначает разжижающие препараты за несколько месяцев до зачатия и в период беременности.
Эта мутация характеризуется врожденным отсутствием пигмента меланина, который придает окраску коже, волосам, радужной и пигментной оболочкам глаза.
Вопрос 6. Назовите основные группы мутагенных факторов. Приведите примеры мутагенов, относящихся к каждой группе.
Интересно, но есть заболевания, передающиеся по женской линии, но страдают ими только мужчины. Следует сказать, что в некоторых случаях лишь знания генетики помогут людям понять, что это за болезнь. Владение людей с генетическими отклонениями, которые не передаются по наследству, информацией о том, что им детям не грозит болезнь является путеводной звездой.
Они возникают в результате нарушения расхождения гомологичных хромосом. Примером может служить синдром Дауна, который возникает при появлении лишней 21-й хромосомы. При этом общее число хромосом становится равным 47. Другим примером геномных мутаций является формирование полиплоидных растений (чаще всего тетраплоидных).
Примером может служить синдром Дауна, который возникает при появлении лишней 21-й хромосомы. При этом общее число хромосом становится равным 47. Другим примером геномных мутаций является формирование полиплоидных растений (чаще всего тетраплоидных).
Цитогенетические исследования проверяют состояние хромосом. Самое распространенное – кариотипирование (изучение количественного состава и структуры хромосом) и метод FISH (определяет аномалии в конкретной хромосоме или ее части).
Изменчивость — способность живых организмов приобретать новые признаки и свойства. Благодаря изменчивости, организмы могут приспосабливаться к изменяющимся условиям среды обитания. Наследственная . или генотипическая .
Организм не может знать, какие мутации будут полезны в следующем поколении. Нет и не может быть механизма, который бы обеспечивал направленное появление полезных для организма мутаций.
Исследование: Аутизм может передаваться по наследству
Они изучают гены, хранящие информацию о человеческом организме. Если природа закладывает в них неправильную информацию, происходит сбой. Поэтому пришло время приступить к рассмотрению основных видов наследственных дефектов.
Если природа закладывает в них неправильную информацию, происходит сбой. Поэтому пришло время приступить к рассмотрению основных видов наследственных дефектов.
Тем не менее, для некоторых количественных признаков характерна узкая норма реакции (жирность молока, число пальцев на ногах у морских свинок), а для некоторых качественных признаков — широкая (например, сезонные изменения окраски у многих видов животных северных широт).
Дети, рожденные в инцестуальном союзе, лишены разнообразия аллелей, поэтому их организм не может эффективно бороться с болезнями.
Вконтакте
Google+
Одноклассники
Похожие записи:
Ген — все статьи и новости
Ген (от греч. genos — «род», «происхождение») — участок молекулы дезоксирибонуклеиновой кислоты (ДНК), отвечающий за формирование единственного признака. В органоидах (постоянных компонентах клетки, необходимых для ее существования; также органеллы) клеточных ядер — хромосомах — гены кодируют информацию о строении белка живой клетки. Участки молекул ДНК могут быть представлены в одной или большем числе форм, называемых аллелями. Практически все клетки живого организма содержат по два аллеля каждого гена и поэтому называются диплоидными. Исключение составляют только гаметы (клетки, участвующие в половом размножении): они гаплоидны, то есть содержат один аллель.
Участки молекул ДНК могут быть представлены в одной или большем числе форм, называемых аллелями. Практически все клетки живого организма содержат по два аллеля каждого гена и поэтому называются диплоидными. Исключение составляют только гаметы (клетки, участвующие в половом размножении): они гаплоидны, то есть содержат один аллель.
Гены, формирующие основные признаки организма, передаются по наследству. У человека 23 пары хромосом. В каждой паре одна хромосома наследуется от матери, другая — от отца. При передаче гены могут мутировать. Мутации представляют собой целенаправленные изменения последовательности нуклеотидов (структурных элементов ДНК, составляющих каждую из цепей ДНК и представляющих собой сложные органические соединения, включающие в себя азотистые основания: аденин (А), тимин (Т), цитозин (Ц), гуанин (Г), пятиатомный сахар (пентозу) дезоксирибозу, по имени которой и получила название сама ДНК, а также остаток фосфорной кислоты). Мутации приводят к изменению последовательности гена и соответственно изменяют характеристики белка и особенности функционирования организма. Такие мутации являются патогенными и вызывают различные заболевания.
Такие мутации являются патогенными и вызывают различные заболевания.
Впервые термин «ген» был употреблен в 1909 году Вильгельмом Иогансеном. Ему же принадлежит и другой термин, «генотип», обозначающий совокупность генов данного организма, введенный в противовес «фенотипу» — совокупности внешних характеристик, присущих индивиду. Однако история генетики началась значительно раньше: в 1865 году монах Грегор Мендель представил результаты опытов по скрещиванию различных видов гороха, открыв законы наследственности. У истоков же отечественной генетики стояли трое ученых: Николай Вавилов, Николай Дубинин и Николай Кольцов.
Источник картинки: http://bit.ly/2d8X2HM
Чернобыльские мутации не передаются по наследству
Дети родителей-чернобыльцев получали мутаций не больше обычного – но только если ребёнок был зачат уже вне досягаемости чернобыльского излучения.
Радиоактивное излучение повреждает ДНК, и клетка не всегда может эти повреждения исправить. Мутации могут либо просто убить клетку, либо превратить её в злокачественную. Наконец, если мутация случится в половых клетках, она перейдёт по наследству в следующее поколение. Собственно, когда нас пугают какими-нибудь двухголовыми телятами и прочими страшными «радиомутантами», то как раз это и имеется в виду: мутации в родительских сперматозоидах и яйцеклетках привели к аномалиям развития у эмбриона, который в результате недосчитался пальцев или, наоборот, получил лишние да ещё и второй хвост в придачу.
Мутации могут либо просто убить клетку, либо превратить её в злокачественную. Наконец, если мутация случится в половых клетках, она перейдёт по наследству в следующее поколение. Собственно, когда нас пугают какими-нибудь двухголовыми телятами и прочими страшными «радиомутантами», то как раз это и имеется в виду: мутации в родительских сперматозоидах и яйцеклетках привели к аномалиям развития у эмбриона, который в результате недосчитался пальцев или, наоборот, получил лишние да ещё и второй хвост в придачу.
‹
›
Есть ряд исследований на животных, которые показали, что «радиомутации» действительно наследуются. Но одно дело – животные в лаборатории, и другое дело – люди в реальной жизни, которые попали под последствия какой-то техногенной катастрофы. Сотрудники Национального института рака (США) вместе с коллегами из Национальной академии медицинских наук Украины, российского Федерального медицинского биофизического центра им А. И. Бурназяна и других научных центров США, Японии и Великобритании проанализировали геномы 130 человек, родившихся между 1987 и 2002 гг. Это были люди, родившиеся либо в семьях ликвидаторов аварии на Чернобыльской АЭС, либо те, чьи родители жили рядом с ней в момент катастрофы. Для каждого родителя была известна приблизительная доза облучения; родительские геномы тоже полностью прочитали.
И. Бурназяна и других научных центров США, Японии и Великобритании проанализировали геномы 130 человек, родившихся между 1987 и 2002 гг. Это были люди, родившиеся либо в семьях ликвидаторов аварии на Чернобыльской АЭС, либо те, чьи родители жили рядом с ней в момент катастрофы. Для каждого родителя была известна приблизительная доза облучения; родительские геномы тоже полностью прочитали.
Напомним, что авария произошла 26 апреля 1986 года. Людей из зоны загрязнения эвакуировали, так что те, кто родился в 87 году, во время внутриутробного развития не облучались. То есть «радиомутации» могли появиться у них только от родительских половых клеток. Причём такие мутации у детей должны были быть в любой клетке тела – ведь все наши клетки берут начало от одной-единственной оплодотворённой яйцеклетки.
У родителей же такие мутации должны были быть ограничены только сперматозоидами и яйцеклетками, и ни в коже, ни в мышцах, ни где-то ещё их быть не должно. То есть в клетках кожи, мышц и т. д. тоже могли быть мутации, но другие – дефекты в ДНК от радиоактивного излучения, как и от других мутагенов, можно узнать, но дефекты эти будут встречаться в разных участках генома. Например, под одной и той же порцией излучения у клеток кожи промутировали одни гены, а в половых клетках – другие.
То есть в клетках кожи, мышц и т. д. тоже могли быть мутации, но другие – дефекты в ДНК от радиоактивного излучения, как и от других мутагенов, можно узнать, но дефекты эти будут встречаться в разных участках генома. Например, под одной и той же порцией излучения у клеток кожи промутировали одни гены, а в половых клетках – другие.
Разные люди из зоны аварии получили, конечно, разные дозы облучения. Но вне зависимости от дозы, как говорится в статье в Science, их дети рождались без каких-либо добавочных мутаций. То есть какие-то новые мутации у детей были, но их число было таким же, как в среднем по популяции. То есть чернобыльские мутации не перешли по наследству, хотя, строго говоря, мы не знаем, были ли в половых клетках родителей вообще какие-то мутации. Может быть, ДНК сперматозоидов и яйцеклеток вообще не затронуло. Возможно, что мутации были, но их исправили системы ремонта ДНК, которые у клеток-предшественников сперматозоидов и яйцеклеток могут работать как-то особенно хорошо. Так или иначе, в случае катастроф, подобных аварии на Чернобыльской АЭС, можно не бояться, что генетический вред перейдёт в следующие поколения – во всяком случае, если следующее поколение зачиналось вне зоны радиоактивного загрязнения.
Так или иначе, в случае катастроф, подобных аварии на Чернобыльской АЭС, можно не бояться, что генетический вред перейдёт в следующие поколения – во всяком случае, если следующее поколение зачиналось вне зоны радиоактивного загрязнения.
В то же время, если человек подвергся облучению во время эмбрионального развития, у него вырастает вероятность онкологических проблем в будущем. То, что радиация связана с онкозаболеваниями, давно известно, и другая статья в Science от тех же авторов это лишний раз подтверждает. Во второй работе анализировали ДНК более 350 людей с раковыми опухолями щитовидной железы. В момент Чернобыльской аварии они были либо детьми, либо ещё развивались в материнской утробе. Кстати сказать, образцы тканей, которые использовали в первом и втором исследовании, собрали и законсервировали много лет назад в надежде, что когда-нибудь научные методы позволят изучить их более тщательно, чем это было возможно тогда – и вот такой момент настал.
ДНК больных сравнивали с ДНК нескольких десятков людей, которые родились более чем через девять месяцев после аварии (то есть под облучение не попали). В ДНК опухолей обнаружились следы двойных разрывов, когда рвутся обе цепи, образующие молекулу ДНК. Сильнее всего связь между двойными разрывами и облучением была видна у тех, кого авария застала совсем маленькими.
Набор генов, которых коснулись опухолевые мутации, большей частью совпадал с тем, что было известно из более ранних исследований рака щитовидной железы. Отличались только разновидности мутаций. У тех людей, которые получили большую дозу облучения, мутации выглядели как разрывы ДНК с последующим сшиванием неправильных кусков – в результате получались неправильные гены-химеры. У тех, кто получил небольшую дозу радиации, или же у тех, у кого мутации возникли без радиации, они выглядели как точечные замены нуклеотидов генетических «букв» в последовательности гена. (Вообще, мутации, которые попали в уже развивающийся эмбрион, теоретически могут привести не только к онкологическим проблемам, но и каким-нибудь порокам развития, вроде пресловутых лишних пальцев. Но причиной тому будет не тяжёлое мутационное наследство, а собственные мутации эмбриона.)
Но причиной тому будет не тяжёлое мутационное наследство, а собственные мутации эмбриона.)
Вряд ли из полученных данных можно получить мгновенные клинические результаты. Но, по крайней мере, так мы лучше представляем, какие генетические изменения запускают развитие онкозаболеваний радиационного происхождения. И в перспективе эти знания вполне могут пригодиться в разработке специальных методов лечения, направленных против «радиоопухолей».
Что такое наследственные заболевания и как с ними быть?
Наследственные заболевания передаются от одного или обоих родителей детям. Они вызываются генетическими мутациями, но далеко не все генетические заболевания являются наследственными. Как в этом разобраться, какие виды заболеваний бывают, как их лечить и как диагностировать — рассказываем в нашей статье.
Содержание
Что такое наследственные заболевания?
Наследственные заболевания — это заболевания, обусловленные генными или хромосомными мутациями.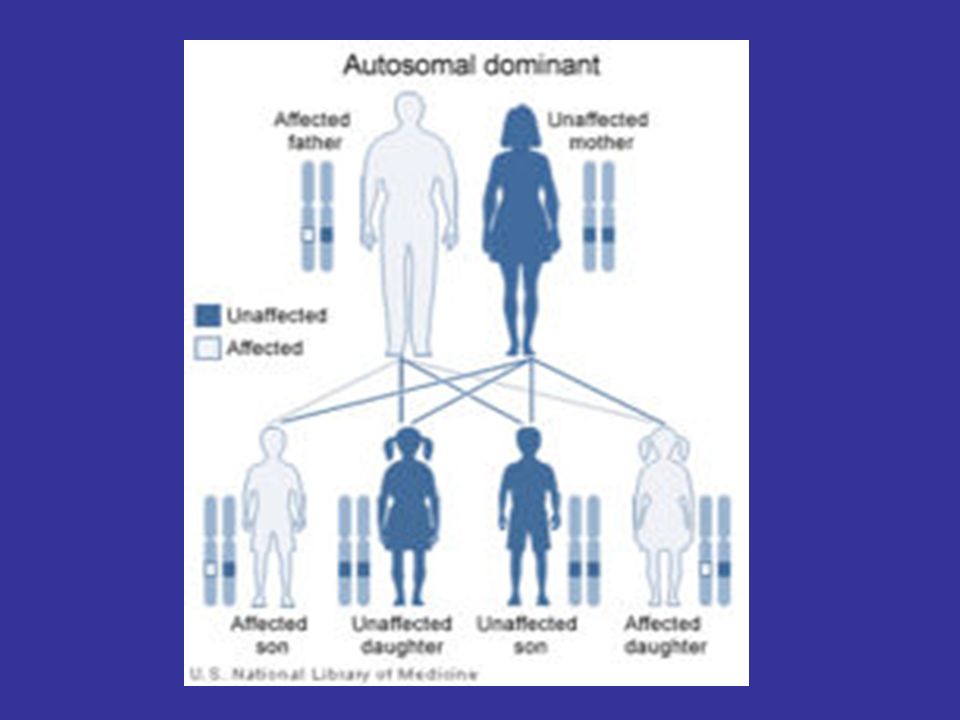 У людей от 20 000 до 25 000 генов. Генетическая мутация возникает, когда изменяется один или несколько генов. Если это генетическое изменение передается детям, то это наследственное генетическое заболевание.
У людей от 20 000 до 25 000 генов. Генетическая мутация возникает, когда изменяется один или несколько генов. Если это генетическое изменение передается детям, то это наследственное генетическое заболевание.
При совпадении у партнеров статусов носительства определенных болезней есть высокий риск рождения ребенка с наследственным заболеванием. Если у вас не проявляются симптомы заболевания, вы по-прежнему можете быть носителем и передать мутации своим детям.
Многие генетически обусловленные заболевания проявляются не сразу после рождения, а спустя некоторое время. От наследственных заболеваний следует отличать врожденные заболевания, вызванные внутриутробными повреждениями, например, инфекцией или внешними воздействиями.
Чем отличаются наследственные заболевания от врожденных нарушений?
Генетические заболевания являются результатом изменения одного или нескольких генов и могут передаваться в поколениях или нет.
Все наследственные заболевания имеют генетическое происхождение, т. е. являются результатом изменения одного или нескольких генов и передаются из поколения в поколение. Симптомы могут не проявляться с самого рождения.
е. являются результатом изменения одного или нескольких генов и передаются из поколения в поколение. Симптомы могут не проявляться с самого рождения.
Врожденные нарушения могут быть наследственными или нет, а симптомы могут проявляться с рождения. Но их появление не обязательно связано с генетикой.
Виды наследственных заболеваний
Наследственные заболевания разделяются на хромосомные, генные и митохондриальные.
Хромосомные заболевания
В настоящее время описано около 1000 форм хромосомных заболеваний. Хромосомные заболевания возникают в результате изменения числа или структуры хромосом. Они характеризуются общими признаками: маленькая масса и длина тела при рождении, отставание в умственном и физическом развитии, задержка и аномалии полового развития и прочее.
Хромосомные заболевания наследуются редко. И более чем в 95% случаев риск повторного рождения в семье ребенка с хромосомной патологией не превышает общепопуляционного уровня. Хромосомные заболевания с аномалиями числа хромосом включают: синдром Патау, синдром Эдвардса, синдром трисомии хромосомы 8. А хромосомные заболевания с аномалиями структуры хромосом — синдром Ди Джорджи, синдром Вольфа-Хиршхорна, синдром «кошачьего крика», синдром Альфи, синдром Орбели.
А хромосомные заболевания с аномалиями структуры хромосом — синдром Ди Джорджи, синдром Вольфа-Хиршхорна, синдром «кошачьего крика», синдром Альфи, синдром Орбели.
Моногенные заболевания
Моногенные заболевания возникают в результате повреждения ДНК на уровне гена. Количество моногенных заболеваний по некоторым оценкам достигает 5000.
Среди признаков моногенных болезней можно выделить: различные формы умственной отсталости, дефекты органов слуха, зрения, скелетные дисплазии, болезни нервной, эндокринной, иммунной и других систем. К числу наиболее известных моногенных болезней относятся муковисцидоз, гемофилия А и В, болезнь Гоше, миодистрофия Дюшенна/Беккера, спинальная мышечная атрофия, дальтонизм.
Выявить тяжелые моногенные заболевания можно с помощью пренатальной диагностики, а также, определив наличие мутаций у родителей с помощью генетического теста.
Митохондриальные заболевания
Митохондриальные заболевания обусловлены генетическими, структурными, биохимическими дефектами в функционировании митохондрий, которые приводят к нарушению тканевого дыхания.
Митохондрии содержат свою собственную ДНК. А болезни, вызванные мутациями в митохондриальной ДНК, наследуются исключительно по материнской линии. Если именно таким образом было унаследовано митохондриальное заболевание, существует 100% вероятность того, что каждый ребенок в семье его унаследует.
Симптомы могут включать в себя: нарушение роста, слабость мышц, аутизм, ментальные расстройства, проблемы с дыханием, слухом и зрением. Примеры митохондриальных заболеваний: синдром Лея, синдром Вольфа-Паркинсона-Уайта, наследственная оптическая нейропатия Лебера и другие.
Полигенные или мультифакториальные заболевания
Существуют также болезни с наследственной предрасположенностью, которые называют мультифакториальными или полигенными заболеваниями.
Мультифакториальные заболевания обусловлены наследственными факторами риска, и в значительной степени — неблагоприятным воздействием среды. К мультифакториальным заболеваниям относятся большинство хронических заболеваний, включая сердечно-сосудистые, эндокринные, иммунные, нервно-психические, онкологические и др. Например, бронхиальная астма, сахарный диабет, ревматоидный артрит, гипертоническая болезнь сердца и т.д.
Например, бронхиальная астма, сахарный диабет, ревматоидный артрит, гипертоническая болезнь сердца и т.д.
Как передаются наследственные заболевания?
Организм человека состоит из триллионов клеток. Каждая клетка имеет ядро, которое содержит хромосомы. Каждая хромосома состоит из плотно свернутых нитей дезоксирибонуклеиновой кислоты (ДНК).
Гены — это инструкции по сборке белков в нашем организме, которые определяют специфические черты каждого человека, например, цвет глаз или волос. Большинство клеток в организме обычно содержат 46 хромосом, организованных в 23 пары. В каждой из этих 23 пар есть одна унаследованная хромосома от отца и одна — от матери. Из 23 пар 22 пары одинаковые у женских и мужских организмов, а одна оставшаяся определяет, являетесь вы мужчиной (XY) или женщиной (XX).
Мутации, из-за которых возникают наследственные заболевания, могут иметь доминантный или рецессивный характер наследования.
Доминантное наследование означает, что только одна копия гена — от матери или отца — должна иметь мутацию (или патогенный вариант гена) для проявления признака или заболевания. А при рецессивном типе человек наследует две измененные копии одного и того же гена.
А при рецессивном типе человек наследует две измененные копии одного и того же гена.
Аутосомно-доминантный паттерн наследования
При аутосомно-доминантном наследовании заболеваний генетически обусловленная болезнь проявляется в том случае, если у человека есть хотя бы один мутированный ген, и этот ген не расположен на половых (Х и Y) хромосомах.
Болезнь Хантингтона и синдром Марфана — два примера аутосомно-доминантных болезней. Мутации в генах BRCA1 и BRCA2, которые также связаны с раком молочной железы, передаются по этой схеме.
Аутосомно-рецессивный паттерн наследования
При аутосомно-рецессивном наследовании мутируют обе копии генов. Чтобы унаследовать аутосомно — рецессивное заболевание, такое как муковисцидоз, спинальная мышечная атрофия, или фенилкетонурия (ФКУ), оба родителя должны быть носителями. Ребенок наследует две копии дефектного гена — по одной от каждого родителя. Например, люди, имеющие одну копию гена с мутацией, а вторую — без мутации, называются носителями, потому что сами они здоровы.
Х-сцепленное рецессивное наследование
В Х-сцепленном рецессивном наследовании мутированный ген находится на Х-хромосоме. Болезнь проявляется только в случае, если другой Х-хромосомы с нормальной копией того же гена у человека нет.
Мышечная дистрофия Дюшенна, некоторые виды дальтонизма и гемофилия А — примеры рецессивных заболеваний, связанных с X-хромосомой. Мужчина с рецессивным заболеванием, связанным с X-хромосомой, передаст свою нетронутую Y-хромосому сыновьям, и ни один из них не пострадает. Если он передаст свою Х-хромосому (с дефектным геном) своим дочерям, то все они будут носителями болезни. У его дочерей может не быть симптомов или только легкие признаки заболевания, но они могут передать мутированный ген своим детям.
Женщины-носители рецессивного заболевания, связанного с X-хромосомой, часто имеют лёгкие признаки заболевания или вообще не имеют симптомов. Это связано с тем, что у женщин-носителей есть одна нормальная копия гена и одна мутированная копия. Нормальная копия обычно компенсирует дефектную копию в женском организме, в отличие от мужчин, у которых только одна X-хромосома.
Нормальная копия обычно компенсирует дефектную копию в женском организме, в отличие от мужчин, у которых только одна X-хромосома.
Женщины, имеющие только один патологический ген, передают заболевание в среднем половине своих детей вне зависимости от пола. Женщины же, имеющие два патологических гена, передают заболевание всем своим детям. К таким заболеваниям относятся гемофилия А и дальтонизм.
Если вы знаете или предполагаете, что у вас или вашего партнера в семейной истории есть какое-либо генетическое заболевание, вы можете определить это с помощью Генетического теста Атлас. Генетическое консультирование поможет вам узнать о методах лечения, профилактических мерах и репродуктивных возможностях.
Как лечить наследственные заболевания и как с ними жить?
Раньше наследственные заболевания были неизлечимы. Сейчас это по-прежнему остаётся проблемой для многих заболеваний, но для некоторых из них методы лечения уже найдены. Например, это касается болезней, связанных с нарушением метаболизма.
При большинстве наследственных нарушений обмена веществ один фермент либо вообще не вырабатывается организмом, либо вырабатывается в форме, которая не работает. Например, при отсутствии какого-либо фермента в организме могут накапливаться токсичные вещества или может не синтезироваться необходимый продукт — как при гемохроматозе 1 типа.
При этом заболевании организм поглощает слишком много железа из пищи и не может естественным образом избавиться от избытка. Это может привести к чрезмерному накоплению железа в сердце, поджелудочной железе и печени.
Лечение генетических нарушений обмена веществ следует двум общим принципам:
- Необходимо сократить или исключить прием любой пищи или лекарств, которые не усваиваются организмом.
- Заменить или восполнить отсутствующий или неактивный фермент для восстановления метаболизма с помощью диеты и/или лекарств.
Есть более серьезные и распространенные наследственные заболевания, которые не лечатся. Например, мековисцидоз — скопление слизи в лёгких и в пищеварительной системе. От муковисцидоза нет лекарства, но разные методы контроля симптомов помогают предотвращать или уменьшать осложнения и облегчать жизнь с этим заболеванием.
От муковисцидоза нет лекарства, но разные методы контроля симптомов помогают предотвращать или уменьшать осложнения и облегчать жизнь с этим заболеванием.
Со временем муковисцидоз прогрессирует и может привести к летальному исходу, особенно при наличии сопутствующих инфекций. Сегодня благодаря достижениям медицины около половины людей с муковисцидозом доживают до 40 лет. Дети, рожденные с этим заболеванием в наши дни, смогут прожить ещё дольше.
Одно из самых тяжелых наследственных заболеваний, спинальная мышечная атрофия, также с недавнего времени поддается лечению с помощью генной терапии. Но доступен этот метод далеко не каждому. Препарат для лечения СМА — самый дорогой лекарственный препарат в мире.
Лечение или купирование генетических заболеваний стало возможным благодаря международному проекту «Геном человека» по изучению и картированию генов человека, произошел прорыв в диагностике и лечении наследственных заболеваний. Результаты проекта помогают не только находить гены, мутации в которых приводят к заболеваниям, но и диагностировать их с максимальной точностью.
Как я могу узнать, что являюсь носителем генетического заболевания?
Наши гены содержат инструкции, которые сообщают организму, как правильно функционировать. При изменении этих инструкций развиваются различные заболевания. Во многих случаях симптомы впервые проявляются в зрелом возрасте, поэтому иногда мы не знаем, что являемся носителями. Предупредить риски развития и передачи наследственного заболевания можно с помощью Генетического теста Атлас.
На заметку:
- Наследственные заболевания — это заболевания, обусловленные генными или хромосомными мутациями.
- При совпадении у партнеров статусов носительства определенных болезней есть высокий риск рождения ребенка с наследственным заболеванием. Поэтому при планировании беременности важно пройти генетическое тестирование.
- Мутации, из-за которых возникают наследственные заболевания, могут иметь доминантный или рецессивный характер наследования. При доминантном наследовании только одна копия гена — от матери или отца — должна иметь мутацию для проявления признака или заболевания.
 А при рецессивном типе человек наследует две измененные копии одного и того же гена.
А при рецессивном типе человек наследует две измененные копии одного и того же гена. - Большинство наследственных заболеваний неизлечимы. Течение некоторых из них можно контролировать с помощью лекарств и диеты.
- Определить наличие и риск развития наследственного заболевания можно с помощью Генетического теста Атлас.
Что передается по наследству?
Вся информация о человеке — его внешности, характере, талантах и склонностях — заключена в нити ДНК, которая присутствует в ядре каждой клетки организма. Данные закодированы в 46 хромосомах: от отца и матери человек получает в наследство по 23 хромосомы. Они содержат 50 000–100 000 генов, определяющих такие особенности человека, как цвет кожи, глаз, волос, характер и т. д.
Что и как передается по наследству?
Большинство генов обладает двумя вариациями, называемыми аллелями, которые могут быть доминантными и рецессивными. Если в паре оказываются разные гены, то один из них «побеждает». Он называется доминантным, тогда как «подавленный» ген носит имя рецессивного. Когда и у отца, и у матери имеется рецессивный ген, тогда он не только передается по наследству ребенку, но и проявляется у него.
Если в паре оказываются разные гены, то один из них «побеждает». Он называется доминантным, тогда как «подавленный» ген носит имя рецессивного. Когда и у отца, и у матери имеется рецессивный ген, тогда он не только передается по наследству ребенку, но и проявляется у него.
Доминантными считаются гены, отвечающие:
- за темный цвет глаз;
- темные жесткие вьющиеся волосы;
- полные губы;
- смуглую кожу;
- большой нос с горбинкой;
- широкий подбородок.
Рецессивные гены, передающиеся по наследству, несут в себе такие особенности внешности, как:
- светлые глаза;
- светлые мягкие прямые волосы;
- тонкие губы;
- светлая кожа;
- узкий нос с маленькими ноздрями;
- узкий подбородок.
Например, светлый цвет глаз является мутацией гена OCA2, синий и зеленый оттенок обеспечивает ген EYCL1 хромосомы 19, карий — EYCL2. В целом, цвет глаз определяют такие гены, как OCA2, SLC24A4, TYR.
В целом, цвет глаз определяют такие гены, как OCA2, SLC24A4, TYR.
Мы подготовили для Вас список исследований, которые помогут разобраться с данной проблемой:
5 рабочиx дней
Анализ полиморфизмов в генах фолатного цикла
4900 ₽
Подробнее10 рабочиx дней
Скрининг на носительство наследственных заболеваний «Базовый»
7000 ₽
Подробнее45 рабочиx дней
Скрининг на наследственные заболевания «Экспертный»
30000 ₽
ПодробнееЧерты характера и привычки, передающиеся по наследству
Гены, полученные от родителей, определяют не только внешность ребенка. Ученые считают, что интеллектуальные способности также могут передаваться по наследству. Конечно же, в этом играют большую роль воспитание и обучение ребенка. Художественный вкус, творческие способности, музыкальность и другие качества также переходят от родителей к детям. Что еще передается по наследству: темперамент, мимика, тембр голоса.
Художественный вкус, творческие способности, музыкальность и другие качества также переходят от родителей к детям. Что еще передается по наследству: темперамент, мимика, тембр голоса.
К сожалению, наследование касается не только положительных черт характера. Считается, что в наследство от папы и мамы малыш может получить склонность к алкоголизму, агрессии, фобиям, страхам, суицидальным наклонностям. Правильное воспитание, благоприятная атмосфера, в которой растет ребенок, и забота родителей позволяют нивелировать генетические склонности негативного характера.
Здоровье «по наследству»
Описано более 3500 заболеваний человека, обусловленных наследственностью. Ученым известны конкретные гены, «виновные» в развитии болезни, их мутации и типы нарушений, ведущих к развитию патологии. От родителей наследуются: дальтонизм, сахарный диабет первого типа, витилиго, наследственная кардиомиопатия, фенилкетонурия, бронхиальная астма, муковисцидоз, шизофрения и т. д. Наследственность определяет обмен веществ человека, особенности работы иммунной системы, уровень стрессоустойчивости и т. д.
д.
Как узнать, что передается по наследству?
Современная наука и медицина позволяют получить информацию о генетическом наборе любого человека. Это означает, что родители могут заранее узнать, какие гены они могут передать по наследству своему ребенку. Особенно это касается генетических заболеваний и отклонений.
Кариотипирование — исследование, в ходе которого составляется карта хромосом человека. Она позволяет обнаружить перестройки и аномалии в хромосомном наборе родителей, которые могут передаться ребенку. Когда пара знает, что может передаваться по наследству, то более ответственно подходит к вопросу планирования беременности. Зная о рисках, будущая мама с готовностью проходит дородовой скрининг, чтобы убедиться в отсутствии аномалий и генетических нарушений у будущего ребенка.
В медико-генетическом центре «Геномед» проводится кариотипирование и другие исследования хромосомного набора родителей и будущего малыша. В центре также можно пройти неинвазивную и инвазивную пренатальную диагностику плода.
В центре также можно пройти неинвазивную и инвазивную пренатальную диагностику плода.
Найден способ избежать передачи генетических болезней по наследству | Новости | Известия
Митохондриальная ДНК передается без изменений от матери к ребенку, а потому наличие в ней негативных мутаций не может быть компенсировано доминантными генами отца.
Мутации мтДНК могут приводить к большому количеству разнообразных тяжелых нарушений работы организма — мышечной и сердечной недостаточности, нарушениям функций печени, слепоте, нарушениям умственного развития и так далее.
По этой причине молодые женщины, знающие о своей плохой наследственности, вынуждены принимать тяжелое решение — иметь ли собственных детей, и потенциально обрекать их на пожизненные проблемы со здоровьем, или не иметь своих детей вовсе.
Группа ученых под руководством Дугласа Тарнбелла из Университета Ньюкасла в Великобритании показала, что в будущем этого непростого выбора можно будет избежать благодаря методу отделения ядерной ДНК от мтДНК в яйцеклетке и ее переносу в новую здоровую донорскую яйцеклетку, имеющую нормально функционирующую мтДНК.
В процессе оплодотворения женская яйцеклетка, имеющая мтДНК полностью унаследованную от матери, а также половину всех материнских генов в ядерной ДНК, получает вторую половину необходимых будущему ребенку генов от оплодотворяющей ее отцовской половой клетки. В течение некоторого времени эти две половины ДНК существую раздельно, после чего сливаются в единое ядро. На этой стадии начинается рост и развитие зародыша.
Группа Тарнбелла на примере 80 человеческих яйцеклеток показала, что на той стадии, когда два набора генов в уже оплодотворенной яйцеклетке существуют еще отдельно друг от друга, их можно отделить от остального содержимого яйцеклетки и перенести в новую донорскую клетку, освобожденную от собственной ядерной ДНК.
При этом будущий плод сохраняет все гены, передавшиеся ему от родителей, которые определяют уникальность и характерные черты каждого человека, живущего на планете, сообщает РИА «Новости».
В то же самое время, новая яйцеклетка уже не содержит мутантной мтДНК, а потому и развитие зародыша и рост будущего ребенка должны протекать без отклонений и осложнений.
В своей работе ученые доказали это, дав новым зародышам развиться в течение шести-восьми дней. После этого, согласно действующему британскому законодательству, ученым пришлось их уничтожить.
«У нас нет методов лечения болезней, связанных с мутациями мтДНК на настоящий момент, однако разработанная технология может позволить в будущем избежать развития и проявления этих болезней. Мы помогаем семьям, имеющим плохую наследственность, иметь здоровых детей — то, к чему многие люди относятся как к самому собой разумеющемуся», — прокомментировал работу Тарнбелл, слова которого приводит The Daily Telegraph.
Мутация | Национальное географическое общество
Мутация — это изменение структуры гена, единицы наследственности. Гены состоят из дезоксирибонуклеиновой кислоты (ДНК), длинной молекулы, состоящей из строительных блоков, называемых нуклеотидами. Каждый нуклеотид построен вокруг одной из четырех различных субъединиц, называемых основаниями. Эти основания известны как гуанин, цитозин, аденин и тимин.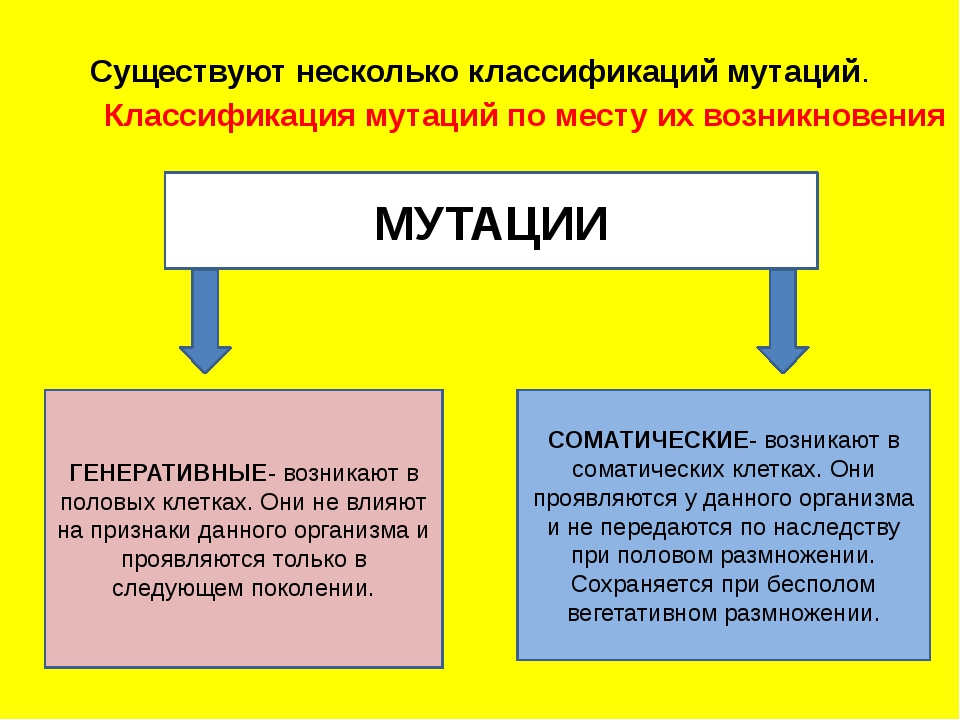 Ген несет информацию в последовательности своих нуклеотидов, так же как предложение несет информацию в последовательности своих букв.
Ген несет информацию в последовательности своих нуклеотидов, так же как предложение несет информацию в последовательности своих букв.
Одним из видов мутации является изменение основания. Это называется точечной мутацией и похоже на изменение одной буквы в слове. Большинство генов несут инструкции по созданию белков. При замене основания в гене возможны разные результаты в зависимости от того, какое основание заменяется и во что оно превращается. Ген может продуцировать измененный белок, он может не продуцировать белок или может продуцировать обычный белок. Большинство мутаций не вредны, но некоторые могут быть. Вредная мутация может привести к генетическому заболеванию или даже к раку.
Другим видом мутации являются хромосомные мутации. Хромосомы, расположенные в ядре клетки, представляют собой крошечные нитевидные структуры, несущие гены. Хромосома состоит из молекулы ДНК вместе с белками. Иногда длинный сегмент ДНК вставляется в хромосому, удаляется из хромосомы, переворачивается внутри хромосомы, дублируется или перемещается из одной хромосомы в другую. Такие изменения обычно очень вредны.
Такие изменения обычно очень вредны.
Одним из примеров хромосомной мутации является состояние, называемое синдромом Дауна.В каждой клетке человека обычно содержится сорок шесть хромосом, состоящих из двух копий двадцати трех видов хромосом. Синдром Дауна обычно возникает в результате наличия одной дополнительной копии определенной хромосомы или дополнительной части этой хромосомы. Наличие этой дополнительной хромосомы приводит к проблемам с некоторыми органами тела, такими как сердце. Это также может привести к лейкемии — раку кроветворных клеток — и вызвать умственную отсталость. Многие люди с синдромом Дауна также имеют отличительные черты лица.
Мутации могут быть унаследованы или приобретены в течение жизни человека. Мутации, которые человек наследует от своих родителей, называются наследственными мутациями. Они присутствуют во всех клетках организма и могут передаваться новым поколениям. Приобретенные мутации происходят в течение жизни человека. Если приобретенная мутация происходит в яйцеклетке или сперматозоиде, она может быть передана потомству человека. Как только приобретенная мутация передается по наследству, она становится наследственной мутацией. Приобретенные мутации не передаются по наследству, если они происходят в соматических клетках, т.е. в клетках организма, отличных от сперматозоидов и яйцеклеток.Некоторые приобретенные мутации возникают спонтанно и случайным образом в генах. Другие мутации вызваны факторами окружающей среды, такими как воздействие определенных химических веществ или радиация.
Как только приобретенная мутация передается по наследству, она становится наследственной мутацией. Приобретенные мутации не передаются по наследству, если они происходят в соматических клетках, т.е. в клетках организма, отличных от сперматозоидов и яйцеклеток.Некоторые приобретенные мутации возникают спонтанно и случайным образом в генах. Другие мутации вызваны факторами окружающей среды, такими как воздействие определенных химических веществ или радиация.
Мутации происходят повсюду в мире природы. Некоторые мутации полезны и увеличивают вероятность того, что организм будет процветать и передавать свои гены следующему поколению. Когда мутации улучшают выживаемость или размножение, процесс естественного отбора приводит к тому, что мутация со временем становится более распространенной.Когда мутации вредны, со временем они становятся менее распространенными. Следовательно, мутация — это сила, которая помогает управлять эволюцией.
Что такое вариант гена и как возникают варианты?: MedlinePlus Genetics
Вариант гена — это необратимое изменение в последовательности ДНК, из которой состоит ген. Этот тип генетического изменения раньше был известен как генная мутация, но поскольку изменения в ДНК не всегда вызывают заболевание, считается, что вариант гена является более точным термином. Варианты могут затрагивать один или несколько строительных блоков ДНК (нуклеотидов) в гене.
Этот тип генетического изменения раньше был известен как генная мутация, но поскольку изменения в ДНК не всегда вызывают заболевание, считается, что вариант гена является более точным термином. Варианты могут затрагивать один или несколько строительных блоков ДНК (нуклеотидов) в гене.
Генные варианты могут быть унаследованы от родителей или возникать в течение жизни человека:
- Унаследованные (или наследственные) варианты передаются от родителей к детям и присутствуют на протяжении всей жизни человека практически в каждой клетке тела. Эти варианты также называются вариантами зародышевой линии, потому что они присутствуют в родительских яйцеклетках или сперматозоидах, которые также называются зародышевыми клетками. Когда яйцеклетка и сперматозоид объединяются, образующаяся оплодотворенная яйцеклетка содержит ДНК обоих родителей.Любые варианты, присутствующие в этой ДНК, будут присутствовать в клетках ребенка, вырастающего из оплодотворенной яйцеклетки.
- Ненаследуемые варианты возникают в какой-то момент жизни человека и присутствуют только в определенных клетках, а не в каждой клетке организма.
 Поскольку ненаследуемые варианты обычно встречаются в соматических клетках (клетках, отличных от сперматозоидов и яйцеклеток), их часто называют соматическими вариантами. Эти варианты не могут быть переданы следующему поколению. Ненаследуемые варианты могут быть вызваны факторами окружающей среды, такими как ультрафиолетовое излучение солнца, или могут возникнуть, если допущена ошибка, когда ДНК копирует себя во время клеточного деления.
Поскольку ненаследуемые варианты обычно встречаются в соматических клетках (клетках, отличных от сперматозоидов и яйцеклеток), их часто называют соматическими вариантами. Эти варианты не могут быть переданы следующему поколению. Ненаследуемые варианты могут быть вызваны факторами окружающей среды, такими как ультрафиолетовое излучение солнца, или могут возникнуть, если допущена ошибка, когда ДНК копирует себя во время клеточного деления.
Некоторые генетические изменения описываются как новые (de novo) варианты; эти варианты распознаются у ребенка, но не у одного из родителей. В некоторых случаях вариант встречается в яйцеклетке или сперматозоиде родителей, но не присутствует ни в одной из их других клеток. В других случаях вариант возникает в оплодотворенной яйцеклетке вскоре после объединения яйцеклетки и сперматозоида. (Часто невозможно точно сказать, когда возник вариант de novo.) По мере деления оплодотворенной яйцеклетки каждая полученная клетка в растущем эмбрионе будет иметь вариант.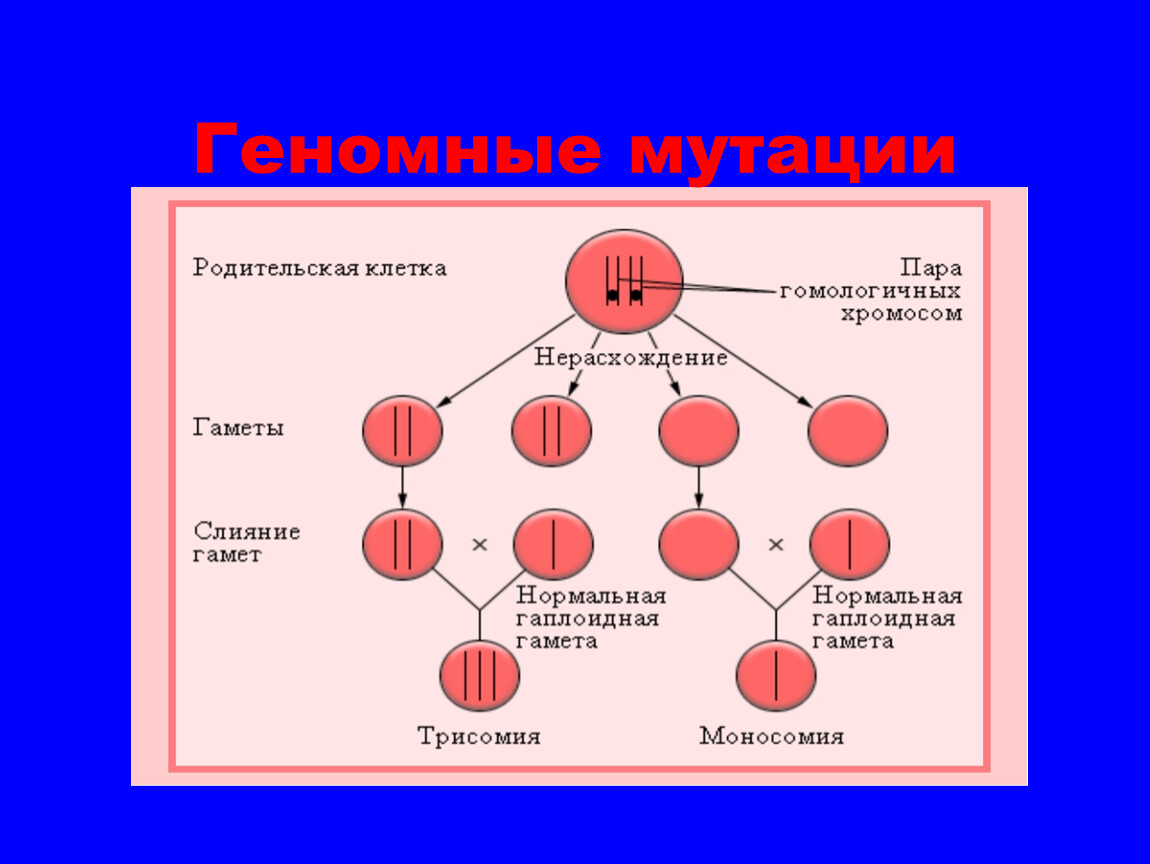 Варианты de novo — это одно из объяснений генетических нарушений, при которых у больного ребенка есть вариант в каждой клетке тела, а у родителей — нет, и в семейном анамнезе этого расстройства нет.
Варианты de novo — это одно из объяснений генетических нарушений, при которых у больного ребенка есть вариант в каждой клетке тела, а у родителей — нет, и в семейном анамнезе этого расстройства нет.
Варианты, приобретенные в процессе развития, могут привести к ситуации, называемой мозаицизмом, при которой набор клеток в организме имеет генетический состав, отличный от других. При мозаицизме генетические изменения отсутствуют в родительской яйцеклетке или сперматозоидах или в оплодотворенной яйцеклетке, а происходят позже, в любое время от эмбрионального развития до взрослой жизни.По мере роста и деления клеток клетки, возникающие из клетки с измененным геном, будут иметь вариант, а другие клетки — нет. Когда часть соматических клеток имеет вариант гена, а другие нет, это называется соматическим мозаицизмом. В зависимости от варианта и количества пораженных клеток соматический мозаицизм может вызывать или не вызывать проблемы со здоровьем. Когда часть яйцеклеток или сперматозоидов имеют вариант, а другие нет, это называется мозаицизмом зародышевой линии. В этой ситуации незатронутый родитель может передать генетическое заболевание своему ребенку.
В этой ситуации незатронутый родитель может передать генетическое заболевание своему ребенку.
Большинство вариантов не приводят к развитию заболевания, а те, которые вызывают, редко встречаются среди населения в целом. Некоторые варианты встречаются в популяции достаточно часто, чтобы их можно было считать обычной генетической вариацией. Несколько таких вариантов отвечают за различия между людьми, такие как цвет глаз, цвет волос и группа крови. Хотя многие из этих распространенных вариаций ДНК не оказывают негативного влияния на здоровье человека, некоторые из них могут влиять на риск развития определенных заболеваний.
Генетика рака | Рак.Net
Гены находятся в ДНК каждой клетки вашего тела. Они контролируют работу клетки, в том числе:
Как быстро растет
Как часто делится
Как долго он живет
По оценкам исследователей, каждая клетка содержит 30 000 различных генов. Внутри каждой клетки гены расположены на хромосомах.
О хромосомах
Хромосомы представляют собой нитевидные структуры в клетках, содержащие гены.Имеется 46 хромосом, расположенных в 2 набора по 23.
Вы унаследовали один комплект от матери и один от отца. Одна хромосома в каждом наборе определяет, мужчина вы или женщина. Остальные 22 пары хромосом определяют другие физические характеристики. Эти пары хромосом называются аутосомами.
Как работают гены
Гены контролируют работу ваших клеток, производя белки. Белки имеют определенные функции и действуют как мессенджеры для клетки.
Каждый ген должен иметь правильные инструкции для создания своего белка.Это позволяет белку выполнять правильную функцию для клетки.
Все виды рака начинаются, когда один или несколько генов в клетке мутируют. Мутация – это изменение. Он создает аномальный белок. Или это может предотвратить образование белка.
Аномальный белок предоставляет другую информацию, чем нормальный белок. Это может привести к бесконтрольному размножению клеток и стать раковыми.
О генетических мутациях
Существует 2 основных типа генетических мутаций:
Приобретенные мутации. Это наиболее частая причина рака. Они возникают из-за повреждения генов в той или иной клетке в течение жизни человека. Например, это может быть клетка молочной железы или клетка толстой кишки, которая затем многократно делится и образует опухоль. Опухоль представляет собой аномальное образование. Рак, который возникает из-за приобретенных мутаций, называется спорадическим раком. Приобретенные мутации не обнаруживаются в каждой клетке организма и не передаются от родителей к детям.
К факторам, вызывающим эти мутации, относятся:
Мутации зародышевой линии. Встречаются реже. Мутация зародышевой линии происходит в сперматозоиде или яйцеклетке. Он переходит непосредственно от родителя к ребенку во время зачатия. Когда эмбрион превращается в ребенка, мутация исходного сперматозоида или яйцеклетки копируется в каждую клетку тела. Поскольку мутация затрагивает репродуктивные клетки, она может передаваться из поколения в поколение.
Рак, вызванный мутациями зародышевой линии, называется наследственным раком. На его долю приходится от 5% до 20% всех видов рака.
Мутации и рак
Мутации происходят часто.Мутация может быть полезной, вредной или нейтральной. Это зависит от того, где в гене происходит изменение. Как правило, организм корректирует большинство мутаций.
Одна мутация, скорее всего, не вызовет рак. Обычно рак возникает в результате множественных мутаций в течение жизни. Вот почему рак чаще возникает у пожилых людей. У них было больше возможностей для накопления мутаций.
Типы генов, связанные с раком
Многие гены, влияющие на развитие рака, делятся на широкие категории:
Гены-супрессоры опухолей. Это защитные гены. В норме они ограничивают рост клеток на:
При мутации гена-супрессора опухоли клетки растут бесконтрольно. И они могут в конечном итоге сформировать опухоль.
Примеры генов-супрессоров опухолей включают BRCA1 , BRCA2 и p53 или TP53 .
в генах BRCA1 или BRCA2 повышают риск развития наследственного рака молочной железы или яичников у женщин и риск развития наследственного рака предстательной железы или молочной железы у мужчин.Они также увеличивают риск рака поджелудочной железы и меланомы у женщин и мужчин.
Наиболее часто у больных раком мутируют гены p53 или TP53 . Более 50% случаев рака связаны с отсутствием или повреждением гена p53 . Большинство мутаций генов p53 являются приобретенными. Мутации зародышевой линии p53 встречаются редко, но пациенты, которые их несут, подвергаются более высокому риску развития многих различных типов рака.
Онкогены. Они превращают здоровую клетку в раковую.Известно, что мутации в этих генах не передаются по наследству.
Два распространенных онкогена:
HER2, специализированный белок, контролирующий рост и распространение рака. Встречается в некоторых раковых клетках.
 Например, клетки рака молочной железы и яичников.
Например, клетки рака молочной железы и яичников.Семейство генов RAS , которое создает белки, участвующие в путях клеточной коммуникации, росте и гибели клеток.
Гены репарации ДНК. Исправление ошибок при копировании ДНК.Многие из них функционируют как гены-супрессоры опухолей. BRCA1 , BRCA2 и p53 являются генами репарации ДНК.
Если у человека есть ошибка в гене репарации ДНК, ошибки остаются неисправленными. Затем ошибки становятся мутациями. Эти мутации могут в конечном итоге привести к раку, особенно мутации в генах-супрессорах опухолей или онкогенах.
Мутации в генах репарации ДНК могут передаваться по наследству или приобретаться. Синдром Линча является примером наследственного типа.Мутации BRCA1 , BRCA2 и p53 и связанные с ними синдромы также наследуются.
Проблемы понимания генетики рака
Исследователи многое узнали о том, как работают гены рака. Но многие виды рака не связаны с конкретным геном. Рак, вероятно, связан с множественными генными мутациями. Более того, некоторые данные свидетельствуют о том, что гены взаимодействуют с окружающей средой. Это еще больше усложняет наше понимание роли генов в развитии рака.
Но многие виды рака не связаны с конкретным геном. Рак, вероятно, связан с множественными генными мутациями. Более того, некоторые данные свидетельствуют о том, что гены взаимодействуют с окружающей средой. Это еще больше усложняет наше понимание роли генов в развитии рака.
Исследователи продолжают изучать влияние генетических изменений на развитие рака. Эти знания привели к улучшению лечения рака, включая раннее выявление, снижение риска, использование таргетной терапии и выживаемость.
Дальнейшее изучение генетики рака может помочь врачам найти лучшие способы:
Связанные ресурсы
Генетическое тестирование на риск рака
Понимание риска рака
Наследственные синдромы, связанные с раком
Что такое персонализированная медицина рака?
Как геномное тестирование дало мне чувство контроля над метастатическим раком молочной железы
Дополнительная информация
Национальный институт рака (NCI): Генетика рака
NCI: как генетические изменения приводят к раку (инфографика)
Унаследованные мутации и рак
Большинство генов идут парами. Люди наследуют одну копию каждого гена от матери и одну копию от отца. Иногда родитель может передать своим детям ген с повреждением, который называется «мутация». Дети могут передать одну и ту же мутацию каждому из своих детей. Если вы родились с генной мутацией, полученной от вашей матери или отца, у вас есть «унаследованная генная мутация». Вы можете просмотреть наше видео о том, как мутации вызывают рак, и узнать больше на нашей странице Как мутации наследуются?
Люди наследуют одну копию каждого гена от матери и одну копию от отца. Иногда родитель может передать своим детям ген с повреждением, который называется «мутация». Дети могут передать одну и ту же мутацию каждому из своих детей. Если вы родились с генной мутацией, полученной от вашей матери или отца, у вас есть «унаследованная генная мутация». Вы можете просмотреть наше видео о том, как мутации вызывают рак, и узнать больше на нашей странице Как мутации наследуются?
Унаследованная генная мутация не всегда вызывает рак.Если вы унаследовали поврежденный ген от отца, у вас все еще есть нормальная копия того же гена от матери.
Также можно получить Повреждения клеток. «Приобретенные» мутации — это повреждения генов, которые происходят после рождения человека. Они вызваны «износом» генов с течением времени. Старение, воздействие гормонов, токсинов окружающей среды и некоторых вирусов могут вызывать генные мутации. Повреждения, которые накапливаются в клетках, могут привести к раку.
Люди с унаследованными мутациями рождаются с одним уже поврежденным геном во всех клетках тела.Это означает, что для развития рака их клеткам требуется меньше шагов.
Восстановление повреждений ДНК
Клетки имеют инструменты для восстановления </li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> повреждений ДНК . Если это невозможно восстановить, у организма есть способы удалить поврежденную клетку, чтобы она не могла делиться и создавать новые поврежденные клетки. Эта система не всегда идеальна, и в клетках могут накапливаться повреждения ДНК и генные мутации. Со временем это может привести к раку.
- Рак у людей, у которых нет наследственной мутации, называется «спорадическим» раком.
- Рак у людей с унаследованной мутацией называется «наследственным» раком.
Гены репарации повреждений ДНК
Определенные гены важны для восстановления DNA contains instructions for the cells in your body on how they should function, grow, divide and die. Most cells in your body have the same DNA code. DNA has the following features:</p> <ul> <li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li> <li>DNA chains are organized into bundles known as genes.</li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> ДНК повреждений. Эти гены иногда называют « Most cells in your body have the same DNA code. DNA has the following features:</p> <ul> <li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li> <li>DNA chains are organized into bundles known as genes.</li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> генами восстановления ДНК » или генами «DDR».
- В нормальных клетках мутации в Most cells in your body have the same DNA code. DNA has the following features:</p> <ul> <li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li> <li>DNA chains are organized into bundles known as genes.</li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> ДНК генов репарации повреждений увеличивают вероятность того, что клетка станет раковой.Вот почему унаследованные мутации в генах, которые Most cells in your body have the same DNA code. DNA has the following features:</p> <ul> <li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li> <li>DNA chains are organized into bundles known as genes.</li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> восстанавливают повреждения ДНК, повышают риск развития рака.
- В клетках, которые уже являются раковыми, мутации в Most cells in your body have the same DNA code. DNA has the following features:</p> <ul> <li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li> <li>DNA chains are organized into bundles known as genes.</li> <li>DNA is used to make the proteins that allow your cells to work normally</li> </ul> »> ДНК генов восстановления повреждений могут препятствовать восстановлению клеток после лечения. Это означает, что раковые клетки с мутациями в этих генах могут быть более чувствительными к определенным видам лечения.
Как наследуются наследственные раковые мутации?
Мужчины и женщины могут передать наследственную генную мутацию своим сыновьям или дочерям через сперму или яйцеклетку. Когда у человека с генной мутацией есть дети, каждый ребенок имеет 50-процентную вероятность унаследовать ту же мутацию.
Когда у человека с генной мутацией есть дети, каждый ребенок имеет 50-процентную вероятность унаследовать ту же мутацию.
Эксперты-генетики внимательно изучают историю болезни семьи на наличие признаков </p> »> наследственного рака . Вы можете помочь им, собрав медицинскую информацию от родственников с обеих сторон вашей семьи.
Как правило, эксперт-генетик изучает три или более поколений истории болезни семьи, чтобы предсказать, могут ли члены семьи иметь наследственную мутацию.Они будут использовать эту информацию для создания медицинского генеалогического древа, известного как родословная.
Степени родства
Говоря о генеалогическом древе, эксперты используют термин «степень родства», чтобы описать, насколько близко один член семьи связан с другим. «Родственники первой степени родства» имеют половину своей Most cells in your body have the same DNA code. DNA has the following features:</p>
<ul>
<li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li>
<li>DNA chains are organized into bundles known as genes.</li>
<li>DNA is used to make the proteins that allow your cells to work normally</li>
</ul>
»> ДНК . Если у человека есть унаследованная мутация, каждый из его родственников первой степени родства имеет 50-процентный шанс получить положительный результат теста на ту же мутацию. Родственники второй степени родства имеют одну четвертую ДНК , родственники третьей степени разделяют одну восьмую ДНК DNA is a chemical shaped like a very long ladder. DNA contains instructions for the cells in your body on how they should function, grow, divide and die. Most cells in your body have the same DNA code. DNA has the following features:</p>
<ul>
<li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li>
<li>DNA chains are organized into bundles known as genes.</li>
<li>DNA is used to make the proteins that allow your cells to work normally</li>
</ul>
»> , и так далее.
Родственники второй степени родства имеют одну четвертую ДНК , родственники третьей степени разделяют одну восьмую ДНК DNA is a chemical shaped like a very long ladder. DNA contains instructions for the cells in your body on how they should function, grow, divide and die. Most cells in your body have the same DNA code. DNA has the following features:</p>
<ul>
<li>it can make exact copies of itself. Before a cell divides into two cells, the DNA is copied so that new cells have the same DNA as their parent cell. </li>
<li>DNA chains are organized into bundles known as genes.</li>
<li>DNA is used to make the proteins that allow your cells to work normally</li>
</ul>
»> , и так далее.
- Ближайшие родственники
- Братья и сестры
- Дети
- Родители
- Родственники второй степени родства Сводные братья и сестры
- Дяди и тети
- Бабушки и дедушки
- Внуки
- Племянницы и племянники
- Родственники третьей степени родства
- Кузены
- Прабабушка и дедушка
- Двоюродные бабушки и двоюродные дедушки
Наследственные мутации в генах репарации ДНК и риск рака
Обзор
. июль-август 2017 г.; 41(4):251-264.
doi: 10.1016/j.currproblcancer.2017.02.009.
Epub 2017 22 марта.
июль-август 2017 г.; 41(4):251-264.
doi: 10.1016/j.currproblcancer.2017.02.009.
Epub 2017 22 марта.Принадлежности Расширять
Принадлежности
- 1 HM Hospitales, Centro Integral Oncológico HM Clara Campal, Мадрид, Испания.
- 2 HM Hospitales, Centro Integral Oncológico HM Clara Campal, Мадрид, Испания. Электронный адрес: [email protected].
Элемент в буфере обмена
Обзор
Нурия Ромеро-Лаорден и соавт. Текущая проблема Рак.июль-август 2017.
Текущая проблема Рак.июль-август 2017.
Показать варианты
Формат АннотацияPubMedPMID
. июль-август 2017 г.; 41(4):251-264. дои: 10.1016/j.currproblcancer.2017.02.009. Epub 2017 22 марта.Принадлежности
- 1 HM Hospitales, Centro Integral Oncológico HM Clara Campal, Мадрид, Испания.

- 2 HM Hospitales, Centro Integral Oncológico HM Clara Campal, Мадрид, Испания.Электронный адрес: [email protected].
Элемент в буфере обмена
Полнотекстовые ссылки Параметры отображения цитированияПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
Хотя большинство случаев рака связано с соматическими мутациями, до 10% случаев связаны с мутациями зародышевой линии.Эта наследственная предрасположенность к раку в основном связана с потерей функции генов-супрессоров, а не с активацией онкогенов. Дефекты в генах репарации ДНК являются генетическими событиями, наиболее часто связанными с наследственным раком. Внедрение высокопроизводительного секвенирования в диагностическом тестировании открыло новые гены предрасположенности. Кроме того, для некоторых типов опухолей эти методы секвенирования также выявили значительно более высокую распространенность мутаций зародышевой линии, чем предыдущие оценки.Клинические последствия многих из этих дефектов репарации еще предстоит определить. Необходимо будет провести дальнейшие исследования, чтобы установить наиболее подходящее лечение незатронутых носителей, число которых, вероятно, будет расти. Наоборот, наличие дефектов репарации ДНК предоставляет уникальную возможность для разработки методов лечения, использующих особенности опухоли. В этой обзорной статье мы суммируем не только наиболее распространенные синдромы, связанные с дефектами репарации ДНК, но и менее известные состояния.Мы рассматриваем лежащую в основе генетику и клинические последствия каждого дефекта репарации ДНК, а также текущие рекомендации по наблюдению за раком.
Внедрение высокопроизводительного секвенирования в диагностическом тестировании открыло новые гены предрасположенности. Кроме того, для некоторых типов опухолей эти методы секвенирования также выявили значительно более высокую распространенность мутаций зародышевой линии, чем предыдущие оценки.Клинические последствия многих из этих дефектов репарации еще предстоит определить. Необходимо будет провести дальнейшие исследования, чтобы установить наиболее подходящее лечение незатронутых носителей, число которых, вероятно, будет расти. Наоборот, наличие дефектов репарации ДНК предоставляет уникальную возможность для разработки методов лечения, использующих особенности опухоли. В этой обзорной статье мы суммируем не только наиболее распространенные синдромы, связанные с дефектами репарации ДНК, но и менее известные состояния.Мы рассматриваем лежащую в основе генетику и клинические последствия каждого дефекта репарации ДНК, а также текущие рекомендации по наблюдению за раком.
Ключевые слова: восстановление ДНК; Мутации зародышевой линии; Синдром наследственного рака молочной железы и яичников; Наследственные раковые синдромы; Синдром Линча.
Авторское право © 2017 Elsevier Inc.Все права защищены.
Похожие статьи
- Выявление зародышевых генетических мутаций у больных раком поджелудочной железы.
Сало-Маллен Э.Э., О’Рейли Э.М., Келсен Д.П., Ашраф А.М., Лоури М.А., Ю К.Х., Рейди Д.Л., Эпштейн А.С., Линкольн А., Салдиа А., Джейкобс Л.М., Рау-Мерти Р., Чжан Л., Курц Р.К., Зальц Л. , Оффит К., Робсон М.Е., Стадлер З.К. Salo-Mullen EE, et al.Рак. 2015 15 декабря; 121 (24): 4382-8. doi: 10.1002/cncr.29664. Epub 2015 6 октября. Рак. 2015. PMID: 26440929 Бесплатная статья ЧВК.
- Генетическое тестирование по локализации рака: желудок.
Чун Н., Форд Дж.М. Чун Н. и др. Рак Дж. 2012 июль-август; 18 (4): 355-63.
 doi: 10.1097/PPO.0b013e31826246dc.
Рак Дж. 2012.
PMID: 22846738
Обзор.
doi: 10.1097/PPO.0b013e31826246dc.
Рак Дж. 2012.
PMID: 22846738
Обзор. - Идентификация полного спектра генетических факторов наследственного рака молочной железы у китайской популяции с помощью секвенирования следующего поколения.
Yang X, Wu J, Lu J, Liu G, Di G, Chen C, Hou Y, Sun M, Yang W, Xu X, Zhao Y, Hu X, Li D, Cao Z, Zhou X, Huang X, Liu Z , Chen H, Gu Y, Chi Y, Yan X, Han Q, Shen Z, Shao Z, Hu Z. Ян X и др. ПЛОС Один. 30 апреля 2015 г.; 10(4):e0125571. doi: 10.1371/journal.pone.0125571. Электронная коллекция 2015. ПЛОС Один. 2015. PMID: 25927356 Бесплатная статья ЧВК.
- Профилактическая оофорэктомия: уменьшение U.S. Смертность от эпителиального рака яичников. Продолжающаяся дискуссия.
Пивер МС. Пивер МС. Онколог.
 1996;1(5):326-330.
Онколог. 1996.
PMID: 10388011
1996;1(5):326-330.
Онколог. 1996.
PMID: 10388011 - Наследственный рак яичников: не только гены BRCA 1 и 2.
Тосс А, Томаселло К, Раззабони Э, Конту Г, Гранди Г, Каньяччи А, Шильдер Р.Дж., Кортези Л. Тосс А и др.Биомед Рез Инт. 2015;2015:341723. дои: 10.1155/2015/341723. Epub 2015 17 мая. Биомед Рез Инт. 2015. PMID: 26075229 Бесплатная статья ЧВК. Обзор.
Цитируется
16 статьи- Damage-Net: Программа метаанализа восстановления ДНК идентифицирует сеть новых генов восстановления, которые способствуют эволюции рака.
Бадер А.С., Бушелл М. Бадер А.С. и соавт. Восстановление ДНК (Amst). 2021 сен;105:103158.
 doi: 10.1016/j.dnarep.2021.103158. Epub 2021 10 июня.
Восстановление ДНК (Amst). 2021.
PMID: 34147942
Бесплатная статья ЧВК.
doi: 10.1016/j.dnarep.2021.103158. Epub 2021 10 июня.
Восстановление ДНК (Amst). 2021.
PMID: 34147942
Бесплатная статья ЧВК. - Геномная нестабильность при множественной миеломе: точка зрения «некодирующей РНК».
Taiana E, Gallo Cantafio ME, Favasuli VK, Bandini C, Viglietto G, Piva R, Neri A, Amodio N.Тайана Э. и др. Раков (Базель). 2021 28 апреля; 13 (9): 2127. doi: 10.3390/раки13092127. Раков (Базель). 2021. PMID: 33924959 Бесплатная статья ЧВК. Обзор.
- Биохимическая и структурная характеристика аналогов мутанта F237C, ассоциированного с раком молочной железы MRE11.
Рахман С., Бейкзаде М., Латам М.П. Рахман С. и др. Научный представитель 2021 г. 29 марта; 11 (1): 7089.doi: 10.1038/s41598-021-86552-0.
 Научный представитель 2021.
PMID: 33782469
Бесплатная статья ЧВК.
Научный представитель 2021.
PMID: 33782469
Бесплатная статья ЧВК. - Создание интегрированного биобанка для точной медицины и персонализированного здравоохранения: проект медицинского мегабанка Тохоку.
Фьюз Н., Сакураи-Ягета М., Кацуока Ф., Данджох И., Симидзу Р., Тамия Г., Нагами Ф., Каваме Х., Хигучи С., Киношита К., Куре С., Ямамото М. Фьюз Н и др.JMA J. 4 сентября 2019 г .; 2 (2): 113–122. doi: 10.31662/jmaj.2019-0014. Epub 2019 6 августа. JMA Дж. 2019. PMID: 33615021 Бесплатная статья ЧВК.
- Открытие лекарств на основе фрагментов и структур для разработки терапевтических средств, направленных на реакцию на повреждение ДНК.
Уилсон Д.М. 3-й, Дикон А.М., Данктон М.Дж., Пеллисена П., Георгиадис М.М., Йех А.
 П., Арваи А.С., Мойани Д., Тайнер Д.А., Дас Д.Уилсон Д.М. 3-й и др.
Прог Биофиз Мол Биол. 2021 авг; 163: 130-142. doi: 10.1016/j.pbiomolbio.2020.10.005. Epub 2020 25 октября.
Прог Биофиз Мол Биол. 2021.
PMID: 33115610
Бесплатная статья ЧВК.
П., Арваи А.С., Мойани Д., Тайнер Д.А., Дас Д.Уилсон Д.М. 3-й и др.
Прог Биофиз Мол Биол. 2021 авг; 163: 130-142. doi: 10.1016/j.pbiomolbio.2020.10.005. Epub 2020 25 октября.
Прог Биофиз Мол Биол. 2021.
PMID: 33115610
Бесплатная статья ЧВК.
LinkOut — больше ресурсов
Полнотекстовые источники
Прочие литературные источники
Укажите
КопироватьФормат: ААД АПА МДА НЛМ
News Feature: Генетические мутации, которые вам нужны
Чтобы вылечить болезнь, исследователи начинают рыскать по геномам ненормально здоровых людей.
В 2009 году исследователи из Института Броуда в Бостоне под руководством генетика Дэвида Альтшулера начали набор пожилых людей с избыточным весом, у которых, по общему мнению, должен был быть диабет 2 типа, но его не было. Ученые не искали генетические мутации, вызывающие диабет, а скорее надеялись найти мутации, предотвращающие его. Их поиски окупились; В прошлом году группа сообщила в журнале Nature Genetics , что люди с определенными мутациями в гене под названием SLC30A8 (семейство носителей растворенных веществ 30, член 8) на 65% реже болеют диабетом, даже если у них есть такие факторы риска, как ожирение. (1).
Ученые не искали генетические мутации, вызывающие диабет, а скорее надеялись найти мутации, предотвращающие его. Их поиски окупились; В прошлом году группа сообщила в журнале Nature Genetics , что люди с определенными мутациями в гене под названием SLC30A8 (семейство носителей растворенных веществ 30, член 8) на 65% реже болеют диабетом, даже если у них есть такие факторы риска, как ожирение. (1).
Полезные мутации, обнаруженные у «здоровых» или выживших после болезни, могут указать путь к терапии. Изображение предоставлено Дэйвом Катлером.
Этот ген малозаметно влияет на инсулин, и у немногих счастливчиков мутации, нарушающие его функцию, похоже, компенсируют силы, которые для остальных из нас, скорее всего, приведут к диабету. Точно так же защитные мутации, которые отключают ген, но приносят пользу, а не проблему, были обнаружены в прошлом несколько случайно.Например, в настоящее время известно, что один процент жителей Северной Европы является носителем мутации в гене под названием CCR-5 , которая приводит к дефекту клеточного рецептора и обеспечивает полный иммунитет от ВИЧ-инфекции (2).
И есть доказательства более удачливых мутаций, скрывающихся в геномах человека, в виде людей, которые, кажется, бросают вызов шансам — курильщиков-долгожителей (3) или людей, которые остаются невредимыми в разгар вспышки инфекционного заболевания. Особенно интригуют те, у кого есть генные мутации, о которых известно, что они вызывают заболевание, но у которых нет признаков болезни.
Теперь более дешевое секвенирование позволяет охотиться за этими мутациями феи-крестной и прокладывает более прямой путь к превращению открытий в потенциальные лекарства или даже цели для новых методов редактирования генов. Это потенциально плодотворная стратегия. Выяснить, как имитировать эффекты полезной мутации, часто бывает проще, чем определить, как обратить вспять последствия вредной мутации, говорит кардиолог и генетик Секар Катиресан, также из Института Броуда.«Самые полезные генетические открытия — это те, которые снижают функцию гена и защищают от болезней», — говорит он. «Это сразу говорит вам, что если вы можете разработать лекарство, имитирующее мутацию, оно должно работать на людях».
Однако найти эти полезные мутации может быть сложнее, чем найти изменения ДНК, связанные с болезнью. Одним из препятствий является набор людей, которые редко пользуются системой здравоохранения. Другая заключается в том, что существующие генетические базы данных обычно не предназначены для определения отсутствия болезни.Но продвигаться вперед, несмотря на эти проблемы, стоит, говорит Лесли Бизекер из Национального исследовательского института генома человека (NHGRI). По его словам, ученые давно изучают однонуклеотидные полиморфизмы (SNP), связанные с болезнями, и изучение противоположного явления прольет свет на основы биологии того, как гены взаимодействуют друг с другом.
«Мы давно изучаем когорты больных и многому научились. Но если вы действительно хотите понять весь спектр взаимосвязей между генами и болезнями, вам нужно изучить как можно больше разных людей», — говорит Бизекер.«Вы должны изучать больных людей, но вы также должны изучать здоровых людей».
Необычайно здоровые
Поскольку очень многие хронические заболевания проявляются только в более позднем возрасте, необычайно здоровые пожилые люди являются хорошей отправной точкой для поиска защитных мутаций. Было несколько гипотез о том, почему некоторые люди живут такой долгой и здоровой жизнью, говорит Нир Барзилай из Медицинского колледжа Альберта Эйнштейна. «Во-первых, у этих парней идеальный геном; у них просто нет мутаций, связанных с болезнью», — говорит он.«Другая причина заключалась в том, что все они худощавые некурящие вегетарианцы».
Было несколько гипотез о том, почему некоторые люди живут такой долгой и здоровой жизнью, говорит Нир Барзилай из Медицинского колледжа Альберта Эйнштейна. «Во-первых, у этих парней идеальный геном; у них просто нет мутаций, связанных с болезнью», — говорит он.«Другая причина заключалась в том, что все они худощавые некурящие вегетарианцы».
Последние исследования опровергают обе эти теории. В прошлом году группа Барзилая проанализировала 44 полных геномных последовательности долгожителей. Всего у группы было 250 мутаций, связанных с болезнью Паркинсона, Альцгеймера, сердечно-сосудистыми заболеваниями и другими хроническими заболеваниями, сообщили ученые в Molecular Genetics and Genomic Medicine (4). Более того, некоторые из столетних страдали ожирением, другие всю жизнь курили, а многие никогда не занимались спортом регулярно.Однако все они прожили столетие, и ни у кого не было признаков хронического заболевания. «Это оставляет нас с фактом, что у них должны быть какие-то геномные причины — помимо отсутствия генов болезней — для их долголетия», — говорит Барзилай.
Вскоре после публикации исследования Барзилаи исследователи NHGRI под руководством Бизекера проанализировали гены, кодирующие белок, или экзомы, у 951 здорового взрослого человека и обнаружили, что у 1 из 10 были мутации, связанные, среди прочего, с болезнью Паркинсона, пороками сердца и заболеваниями крови. .Это были варианты генов, которые не только увеличивают риск заболевания, но и всегда вызывают заболевание. Но половина из этих людей не были больны (5).
Несмотря на такие дразнящие подсказки, поиски защитных мутаций, которые могли бы компенсировать эффекты связанных с болезнью генов и факторов образа жизни, до сих пор терпели неудачу. В 2007 году Эрик Тополь из Института Скриппса и его коллеги, стремясь изучить концентрированную коллекцию здоровых геномов, начали набирать людей старше 80 лет, не страдающих хроническими заболеваниями и не принимающих лекарства, в рамках исследования. Проект Скриппса Велдерли.В течение следующих 7 лет они сформировали когорту из 1400 так называемых вельдерли. В 2014 году они опубликовали полные геномы 454 участников в базе данных с открытым доступом для использования исследователями в любой точке мира. Пока никаких защитных мутаций обнаружено не было. Но «охота идет», — говорит Тополь.
В 2014 году они опубликовали полные геномы 454 участников в базе данных с открытым доступом для использования исследователями в любой точке мира. Пока никаких защитных мутаций обнаружено не было. Но «охота идет», — говорит Тополь.
В тот же период Барзилай, стремясь сосредоточиться на относительно однородном населении, чтобы облегчить обнаружение генетических вариантов, изучал евреев-ашкенази старше 95 лет. а также 700 их потомков.Еще до того, как они завершили полные геномы своих долгожителей, Барзилай и его коллеги обнаружили два многообещающих варианта генов. Они обнаружили, что делеция в гене адипонектина ADIPOQ защищает от воспаления артерий (6). А мутация в гене белка-переносчика эфира холестерина CETP чаще наблюдалась в старшей когорте и была связана с защитой как от высокого уровня холестерина, так и от когнитивных расстройств (7).
Другие исследователи вместо того, чтобы набирать свои собственные здоровые когорты, просмотрели существующие базы данных, такие как база данных Национального института сердца, легких и крови, продолжающийся проект секвенирования экзома Grand Opportunity (GO). Он включает образцы около 200 000 участников крупных исследований здоровья населения, таких как Framingham Heart Study с участием нескольких поколений. Группа Катерисан изучила сто тысяч экзомов из коллекции GO, чтобы обнаружить варианты генов, связанные с низким уровнем холестерина (8). А ученые из коммерческой компании по секвенированию генома 23andMe объявили, что они использовали свою растущую базу данных, чтобы обнаружить, что люди с мутациями в гене SGK1 менее склонны к развитию болезни Паркинсона, чем большинство, даже если у них есть факторы риска этого заболевания.
Он включает образцы около 200 000 участников крупных исследований здоровья населения, таких как Framingham Heart Study с участием нескольких поколений. Группа Катерисан изучила сто тысяч экзомов из коллекции GO, чтобы обнаружить варианты генов, связанные с низким уровнем холестерина (8). А ученые из коммерческой компании по секвенированию генома 23andMe объявили, что они использовали свою растущую базу данных, чтобы обнаружить, что люди с мутациями в гене SGK1 менее склонны к развитию болезни Паркинсона, чем большинство, даже если у них есть факторы риска этого заболевания.
Один из примеров полезных мутаций. ( Left ) В мозге посмертных мышей обнаруживаются аномальные отложения прионов, особенно в гиппокампе ( i ) и таламусе ( ii ). ( Right ) Однако мыши с защитными генами демонстрируют лишь слабые уровни отложения прионов, в том числе в таламусе ( ii ). Адаптировано из исх. 13 с разрешения Macmillan Publishers Ltd: Nature , авторское право 2015 г.
Pathways to Therapeutics
Wellderly не единственные, у кого есть потенциальные генетические жемчужины; обследование выживших после инфекционных заболеваний предлагает еще одно многообещающее направление.«Везде, где было серьезное инфекционное заболевание, заразившее сообщество, просмотр выживших позволяет вам искать гены устойчивости, которые могут пролить огромный свет на этиологию болезни и потенциально привести к новому лечению», — говорит невролог Джон Коллиндж из Университетского колледжа Лондона. .
Исследователи, например, изучают препараты для борьбы с вирусом Эбола, нацеленные на белок, известный как тип C Нимана Пика (NPC). Ген, который его кодирует, при мутации вызывает редкую версию болезни Нимана-Пика, которая обычно приводит к летальному исходу в детстве у людей с двумя копиями.Но в исследованиях на животных люди с только одной мутировавшей копией гена сопротивляются инфекции Эбола, потому что вирусу нужна рабочая версия белка для заражения клеток-хозяев (9).
В другом недавнем исследовании исследователи искали генные мутации, которые защищают от инфекций или тяжелых заболеваний, вызванных гриппом и другими патогенами (10). В октябре исследователи из международного консорциума MalariaGEN идентифицировали вариант гена, который влияет на рецептор поверхности клеток крови и защищает от тяжелых случаев малярии (11).
Коллиндж и его коллеги изучали выживших после более экзотической эпидемии: куру, смертельного неврологического заболевания, похожего на болезнь Крейтцфельда-Якоба (БКЯ). Как и CJD, куру передается деформированными белками, называемыми прионами, и в 1950-х и 1960-х годах он быстро распространился среди членов племени каннибалов в Папа-Новой Гвинее. Когда кто-то умирал от куру, ритуальное поедание его тела означало, что те, кто участвовал в церемонии, тоже заражались этой болезнью. В некоторых деревнях погибли почти все женщины детородного возраста.
Но спустя десятилетия были и выжившие — люди, которые принимали участие в пирах и никогда не болели. В начале 1990-х Коллиндж начал секвенировать их геномы. За последние два десятилетия он обнаружил мутации в их гене прионного белка, PRNP , которые защищают их от куру (12).
В начале 1990-х Коллиндж начал секвенировать их геномы. За последние два десятилетия он обнаружил мутации в их гене прионного белка, PRNP , которые защищают их от куру (12).
«В семьях с полиморфизмом почти нет куру, несмотря на очень высокий уровень воздействия», — говорит Коллиндж. В этом году Коллиндж и его коллеги сообщили в Nature , что мыши с одной из мутаций были защищены от 18 различных видов прионных болезней (13).«Это конкретное открытие невероятно мощное», — говорит Коллиндж. «Мы перешли от 100 процентов гибели мышей к 0 процентам». Теперь исследователи работают над определением структуры защитного Риск и защита на самом деле просто обратные стороны одной медали.
— Прионные белки Sekar Kathiresan
, которые могут пролить свет на то, как имитировать мутацию в остальной части человеческой популяции, что, возможно, приведет к лечению не только куру, но и различных прионных заболеваний.
В идеале открытие защитной мутации может дать информацию для разработки лекарства, которое имитирует его молекулярные эффекты в организме. Ингибиторы CETP, изученные Барзилаи, были исследованы в качестве лекарств от холестерина, хотя ни одно из них не поступило на рынок. А за открытием 23andMe, что некоторые мутации SGK1 защищают от болезни Паркинсона, последовало фундаментальное исследование, показывающее, что блокирование SGK1, белка, который, как известно, опосредует реакцию клеток на стресс, может отключить пути, участвующие в нейродегенерации (14). Появление технологии редактирования гена кластерных регулярно расположенных коротких палиндромных повторов (CRISPR)/Cas9 предлагает еще больше возможностей для разработки методов лечения, основанных на полезных генных мутациях.Спорный метод может однажды дать способ изменить гены взрослых к лучшему. «Вполне возможно, что в дополнение к исправлению мутаций, вызывающих болезни, CRISPR/Cas9 будет использоваться для внесения изменений в гены, которые снижают риск заболевания», — говорит биолог Джонатан Вайсман из Калифорнийского университета в Сан-Франциско, чьи исследования включают CRISPR.
Ингибиторы CETP, изученные Барзилаи, были исследованы в качестве лекарств от холестерина, хотя ни одно из них не поступило на рынок. А за открытием 23andMe, что некоторые мутации SGK1 защищают от болезни Паркинсона, последовало фундаментальное исследование, показывающее, что блокирование SGK1, белка, который, как известно, опосредует реакцию клеток на стресс, может отключить пути, участвующие в нейродегенерации (14). Появление технологии редактирования гена кластерных регулярно расположенных коротких палиндромных повторов (CRISPR)/Cas9 предлагает еще больше возможностей для разработки методов лечения, основанных на полезных генных мутациях.Спорный метод может однажды дать способ изменить гены взрослых к лучшему. «Вполне возможно, что в дополнение к исправлению мутаций, вызывающих болезни, CRISPR/Cas9 будет использоваться для внесения изменений в гены, которые снижают риск заболевания», — говорит биолог Джонатан Вайсман из Калифорнийского университета в Сан-Франциско, чьи исследования включают CRISPR. Приложения.
Приложения.
Возможность находить естественные защитные мутации может даже ускорить процесс тестирования на наркотики — процесс, который обычно медленный и дорогостоящий, — помогая проверять целевые лекарственные препараты.Такие подсказки могли бы, в принципе, помочь фармацевтическим компаниям выбрать наиболее эффективные препараты. В эксперименте, чтобы предсказать, будет ли соединение иметь желаемый эффект, Катиресан и его коллеги решили выяснить, может ли препарат под названием эзетимиб, разработанный для снижения уровня холестерина, также предотвращать сердечные приступы. Поскольку эзетимиб блокирует белок NPC1L1, команда искала людей с мутациями в гене NPC1L1 , чтобы изучить их частоту сердечных приступов: «Если бы мы могли найти этих людей, это было бы так, как если бы им давали препарат на всю жизнь. жизни», — говорит Катиресан.
Возвращаясь к подмножеству сотен тысяч экзомов NHLBI, команда Катиресана обнаружила горстку — примерно одного из 650 человек — у которых была любая из 15 мутаций NPC1L1 , и действительно, у этих людей риск сердечного приступа был на 53% ниже, чем у люди без мутаций. Через несколько месяцев пришли результаты клинического испытания; У пациентов с прогрессирующим заболеванием сердца, принимающих эзетимиб, наблюдалось небольшое снижение частоты сердечных приступов и инсультов (15). Это было доказательством того, что полезные мутации могут помочь предсказать действие лекарства.
Через несколько месяцев пришли результаты клинического испытания; У пациентов с прогрессирующим заболеванием сердца, принимающих эзетимиб, наблюдалось небольшое снижение частоты сердечных приступов и инсультов (15). Это было доказательством того, что полезные мутации могут помочь предсказать действие лекарства.
Борьба со статистикой
Эксперимент Катиресана зависел от огромной базы данных экзомов NHLBI, потому что полезные мутации трудно найти и трудно доказать. Для его плана по прогнозированию эффективности лекарств в ходе испытаний, как и для любых попыток выследить защитные мутации, исследователям нужны очень большие группы людей и множество данных об их здоровье.
Если несколько человек с редким заболеванием также имеют редкую генетическую мутацию, есть большая вероятность, что эта мутация связана с их заболеванием.Но если у горстки здоровых людей есть одна и та же генетическая мутация, это, скорее всего, совпадение, и более сложно — со статистической точки зрения — продемонстрировать причинно-следственную связь.
«Риск и защита — это две стороны одной медали, — говорит Катиресан. «Если у вас есть мутация, которая увеличивает риск у 5 процентов людей, вы действительно можете сказать, что 95 процентов людей имеют защитную версию гена». Когда он и его команда искали мутации, связанные с низким уровнем триглицеридов в крови, они решили, что их добыча должна одновременно отключать или препятствовать функции белка и снижать риск ниже нормы.Среди 100 000 экзомов им удалось найти четыре варианта в APOC3, каждый из которых встречается примерно у 1 из 1000 человек.
Исследование ClinSeq Бизекера, в котором приняли участие менее 1000 человек, даже не предназначено для поиска защитных мутаций, а только для документирования примеров людей с болезнетворными вариантами генов, но без болезней. Это потому, что собрать достаточно людей для поиска генов, предотвращающих болезни, очень сложно, говорит Бизекер. Ситуация усложняется тем, что обширные сети родственных генов могут способствовать развитию данного заболевания или набора симптомов.
«Мы давно знаем, что между генами могут возникать взаимодействия и что один вариант гена может компенсировать другой. Но эти вещи статистически и математически сложны для изучения, потому что комбинаторные возможности здесь огромны», — говорит он. «Это вопрос количества и мощности. Нам понадобятся миллионы людей в когорте, чтобы иметь возможность статистически выявлять эти вещи».
Предпринимаются усилия по созданию огромных баз данных, которые можно будет использовать для поиска защитных мутаций.Возможно, самым амбициозным является проект Resilience Project, возглавляемый исследователями из Медицинской школы Икана на горе Синай в Нью-Йорке и Sage Bionetworks в Сиэтле. Они пытаются привлечь 1 миллион добровольцев для пожертвования образцов ДНК (16). Целью проекта является поиск людей в этой огромной случайной выборке, у которых есть генные мутации, которые, как известно, вызывают редкие и тяжелые расстройства, когда присутствует одна копия гена, такие как синдром Костелло и сердечно-кожный синдром, но которые могут даже не знать, что у них есть заболевание.
Потенциальная ценность такой базы данных, особенно перспектива включения подробных историй болезни для выявления наличия или отсутствия болезни, иллюстрируется удачным случаем, когда группа Альтшулера в группе Броуда сосредоточилась на одном варианте . Ген SLC30A8 . У команды были данные, предполагающие, что SLC30A8 могут быть защитными, но они не могли придумать статистическую мощность, необходимую им для доказательства эффекта гена. Однако в Исландии невролог Кари Стефанссон и его компания генетики deCODE потратили два десятилетия на сбор генетических данных и данных о здоровье полумиллиона человек, в том числе более трети исландцев.Находка включает 10 000 последовательностей полного генома, 2600 из которых были описаны в статье Nature Genetics в прошлом году (17). Когда один из ученых Broad упомянул о своих подозрениях относительно SLC30A8 Стефанссону во время телефонного разговора, генеральный директор deCODE провел быстрый поиск в своей базе данных людей, у которых была мутация, и сведений об их состоянии здоровья.
